Содержание
- 2. Нахождение в природе Хром является довольно распространённым элементом в земной коре (0,03 % по массе) Основные
- 3. Физические свойства Хрома Металл обладает достаточной твердостью и хрупкостью одновременно. По шкале Мооса твердость хрома оценивается
- 4. Строение хрома представляет собой объемно-центрированную решетку, благодаря которой металл характеризуется температурой хрупко-вязкого периода. Однако, в случае
- 6. Химические свойства Хрома Атом имеет следующую внешнюю конфигурацию: 3d54s1. Как правило, в соединениях хром имеет следующие
- 7. Во время нагревания металлического хрома, он взаимодействует с галогенами, серой, кремнием, бором, углеродом, а также некоторыми
- 8. Хром не обладает токсичностью, чего нельзя сказать о некоторых его соединениях. Как известно, пыль данного металла,
- 9. Соединения, в котором участвует шестивалентный металл, являются крайне токсичными. Вероятность их попадания в человеческий организм появляется
- 10. Применение Хрома Производство нержавеющей стали Хром нашел широкий спектр применения благодаря своей твердости и устойчивости к
- 11. Сохранение древесины и дубление кож Соли хрома (VI) являются токсичными, поэтому они используются для сохранения древесины
- 13. Скачать презентацию
Слайд 2Нахождение в природе
Хром является довольно распространённым элементом в земной коре (0,03 % по
Нахождение в природе
Хром является довольно распространённым элементом в земной коре (0,03 % по

Основные соединения хрома — хромистый железняк (хромит) FeO·Cr2O3. Вторым по значимости минералом является крокоит PbCrO4
Слайд 3Физические свойства Хрома
Металл обладает достаточной твердостью и хрупкостью одновременно. По шкале Мооса
Физические свойства Хрома
Металл обладает достаточной твердостью и хрупкостью одновременно. По шкале Мооса

Хром является уникальным металлом благодаря своим магнитным свойствам. В условиях комнатной температуры ему присуще антиферромагнитное упорядочение, в то время, как другие металлы обладают им в условиях исключительно пониженных температур. Однако, если хром нагреть выше 370С, физические свойства хрома изменяются. Так, существенно меняется электросопротивление и коэффициент линейного расширения, модуль упругости достигает минимального значения, а внутреннее трение значительно увеличивается. Такое явление связано с прохождением точки Нееля, при которой антиферромагнитные свойства материала способны изменяться на парамагнитные. Это означает, что первый уровень пройден, и вещество резко увеличилось в объеме.
Слайд 4Строение хрома представляет собой объемно-центрированную решетку, благодаря которой металл характеризуется температурой хрупко-вязкого
Строение хрома представляет собой объемно-центрированную решетку, благодаря которой металл характеризуется температурой хрупко-вязкого

Металл легко поддается плавке при температуре 19070С . При температуре в 26720С – закипает. Атомная масса металла составляет 51,996 г/моль.
Слайд 6Химические свойства Хрома
Атом имеет следующую внешнюю конфигурацию: 3d54s1. Как правило, в соединениях
Химические свойства Хрома
Атом имеет следующую внешнюю конфигурацию: 3d54s1. Как правило, в соединениях

Металл не отличается особой химической активностью. Во время нахождения хрома в обычных условиях, металл проявляет устойчивость к влаге и кислороду. Однако, данная характеристика не относится к соединению хрома и фтора – CrF3, которое при воздействии температур, превышающих 6000С, взаимодействует с парами воды, образуя в результате реакции Сr2О3, а также азотом, углеродом и серой.
Слайд 7Во время нагревания металлического хрома, он взаимодействует с галогенами, серой, кремнием, бором,
Во время нагревания металлического хрома, он взаимодействует с галогенами, серой, кремнием, бором,

Cr + 2F2 = CrF4 (с примесью CrF5)
2Cr + 3Cl2 = 2CrCl3
2Cr + 3S = Cr2S3
Хроматы можно получить, если нагреть хром с расплавленной содой на воздухе, нитратами или хлоратами щелочных металлов:
2Cr + 2Na2CO3 + 3O2 = 2Na2CrO4 + 2CO2.
Слайд 8Хром не обладает токсичностью, чего нельзя сказать о некоторых его соединениях. Как
Хром не обладает токсичностью, чего нельзя сказать о некоторых его соединениях. Как

Трехвалентный хром попадает в окружающую среду во время добычи и переработки хромовой руды. В человеческий организм попадание хрома вероятно в виде пищевой добавки, используемой в программах по похудению. Хром с валентностью, равной +3, является активным участником синтеза глюкозы. Ученые установили, что излишнее употребление хрома особого вреда человеческому организму не наносит, поскольку не происходит его всасывание, однако, он способен накапливаться в организме.
Слайд 9Соединения, в котором участвует шестивалентный металл, являются крайне токсичными. Вероятность их попадания
Соединения, в котором участвует шестивалентный металл, являются крайне токсичными. Вероятность их попадания

В зависимости от качества хрома, которое необходимо получить на выходе, существует несколько способов производства металла: электролизом концентрированных водных растворов оксида хрома, электролизом сульфатов, а также восстановлением оксидом кремния. Однако, последний способ не очень популярен, так как при нем на выходе получается хром с огромным количеством примесей. Кроме того, он также является экономически невыгодным.
Слайд 10Применение Хрома
Производство нержавеющей стали
Хром нашел широкий спектр применения благодаря своей твердости и
Применение Хрома
Производство нержавеющей стали
Хром нашел широкий спектр применения благодаря своей твердости и

Покрытие поверхностей
Кислый хромат или дихромат используется также для покрытия поверхностей. Обычно это делается с помощью метода гальваники, в котором тонкий слой хрома наносится на металлическую поверхность. Другой способ - это хромирование деталей, через который хроматы используются для нанесения защитного слоя на определенные металлы, такие как алюминий (Al), кадмий (CD), цинк (Zn), серебро, а также магний (MG).
Слайд 11Сохранение древесины и дубление кож
Соли хрома (VI) являются токсичными, поэтому они используются
Сохранение древесины и дубление кож
Соли хрома (VI) являются токсичными, поэтому они используются

Красители и пигменты
Хром также используется для изготовления пигментов или красителей. Желтый хром и хромат свинца, широко использовались в качестве пигмента в прошлом. Из-за экологических проблем, его использование существенно снизилось, а затем, наконец, его заменили свинец и хромовые пигменты. Другие пигменты на основе хрома, красного хрома, оксида зеленого хрома, которые является смесью желтой и Берлинской лазури. Окись хрома используется для придания зеленоватого цвета стекла.
Синтез искусственных рубинов
Изумруды обязаны своим зеленым оттенком хрому. Окись хрома применяется также для производства синтетических рубинов. Естественные рубины корунды или кристаллы оксида алюминия, которые обретают красный оттенок из-за присутствия хрома. Синтетические или искусственные рубины сделаны легированием хрома (III) на синтетических кристаллах корунда.

 Органические соединения
Органические соединения Презентация по Химии "Соединения алюминия"
Презентация по Химии "Соединения алюминия"  Строение вещества. Эксперименты
Строение вещества. Эксперименты Применение алкенов
Применение алкенов Fyzikálne a chemické deje
Fyzikálne a chemické deje Кислоты
Кислоты Галогеналканы и реакции отщепления
Галогеналканы и реакции отщепления Элементы, названные в честь исследователей
Элементы, названные в честь исследователей Применение центрифугирования
Применение центрифугирования Проблемы и меры по защите окружающей среды ПМР
Проблемы и меры по защите окружающей среды ПМР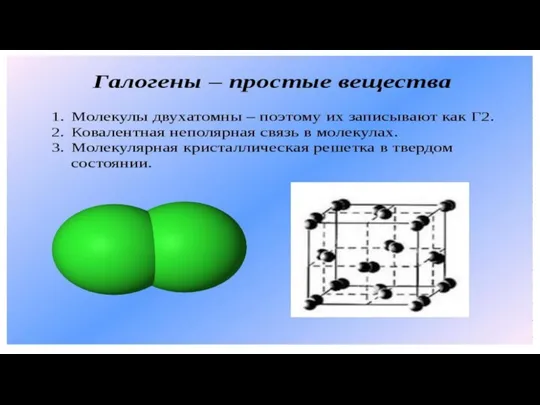 Галогены - простые вещества
Галогены - простые вещества Химические элементы
Химические элементы Учебно-познавательные задачи на уроках химии
Учебно-познавательные задачи на уроках химии 9-12 Гидролиз солей -
9-12 Гидролиз солей - Гидроксикарбоновые кислоты
Гидроксикарбоновые кислоты Электролиз
Электролиз Расчет константы равновестия для реакции
Расчет константы равновестия для реакции Вуглеводні. Метан як представник насичених вуглеводнів
Вуглеводні. Метан як представник насичених вуглеводнів Подготовка выпускников к ГИА по химии: опыт, проблемы, перспективы
Подготовка выпускников к ГИА по химии: опыт, проблемы, перспективы Природные источники углеводородов
Природные источники углеводородов Получение и примененипе радиоактивные изотопы
Получение и примененипе радиоактивные изотопы Презентация на тему Природный и попутный газ
Презентация на тему Природный и попутный газ  Удивительный мир металлов
Удивительный мир металлов Металлы и их соединения
Металлы и их соединения Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Основные классы неорганических соединений. Общие формулы оксидов, оснований, кислот, солей. 8 класс
Основные классы неорганических соединений. Общие формулы оксидов, оснований, кислот, солей. 8 класс Тест для подготовки к ГИА по химии
Тест для подготовки к ГИА по химии Химический элемент кислород
Химический элемент кислород