Содержание
- 2. О ЧЁМ ИДЕТ РЕЧЬ? 1 №3 №2 №1 1) Я, конечно, очень нужен, Без меня не
- 3. 2 Предложите способы получения с солей? Изучите химические свойства солей ( выполните их в виде презентации
- 4. НАЗВАНИЯ СОЛЕЙ 3 Соли безкислородных кислот Соли кислородсодержащих кислот
- 5. МЕДНАЯ ЗЕЛЕНЬ- ? 4
- 6. НАХОЖДЕНИЕ В ПРИРОДЕ 5 Приведите примеры известных вам солей в природе и их использование человеком?
- 7. Д / З РАСПРЕДЕЛИТЕ ВЕЩЕСТВА ПО ОСНОВНЫМ КЛАССАМ И ДАЙТЕ ИМ НАЗВАНИЯ 6 1) NaCl, 2)
- 8. ОТВЕТ 1 Класс: Соли Формула: NaCl
- 9. ОТВЕТ 2 1. кислота + металл 2. кислота + основный оксид 3. кислота + основание 4.
- 10. СОЛИ БЕЗКИСЛОРОДНЫХ КИСЛОТ
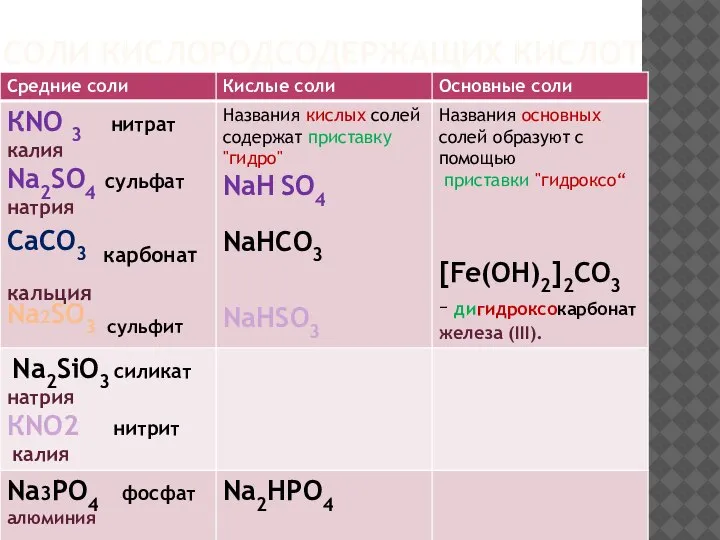
- 11. СОЛИ КИСЛОРОДСОДЕРЖАЩИХ КИСЛОТ
- 12. КЛАСС: КАРБОНАТЫ. ФОРМУЛА: CUCO3 . CU(OH)2 ! 4 дигидроксокарбонат меди Состоит из 71.9% CuO оксид меди
- 13. ! 4 При нагревании в колбе выделяет воду, углекислый газ и становится чёрным: (CuOH)2CO3 =2CuO +CO2
- 15. Скачать презентацию











 Разнообразие веществ. 3 класс
Разнообразие веществ. 3 класс Водопроводная вода и её фильтрация
Водопроводная вода и её фильтрация Введение в аналитическую химию
Введение в аналитическую химию Технология растворов на неводных растворителях
Технология растворов на неводных растворителях Zirconium Dioxide
Zirconium Dioxide Вещества молекулярного и немолекулярного строения
Вещества молекулярного и немолекулярного строения Презентация на тему Химия и повседневная жизнь человека
Презентация на тему Химия и повседневная жизнь человека  Металлы 9 класс
Металлы 9 класс Здравствуйте, химия! Что изучает химия
Здравствуйте, химия! Что изучает химия Кислоты. Кислоты, вокруг нас
Кислоты. Кислоты, вокруг нас Презентация на тему: Чистые вещества и смеси
Презентация на тему: Чистые вещества и смеси Сера и ее соединения
Сера и ее соединения Фенолы. Классификация
Фенолы. Классификация Презентация на тему Количество вещества. Молярная масса
Презентация на тему Количество вещества. Молярная масса  Элемент протактиний
Элемент протактиний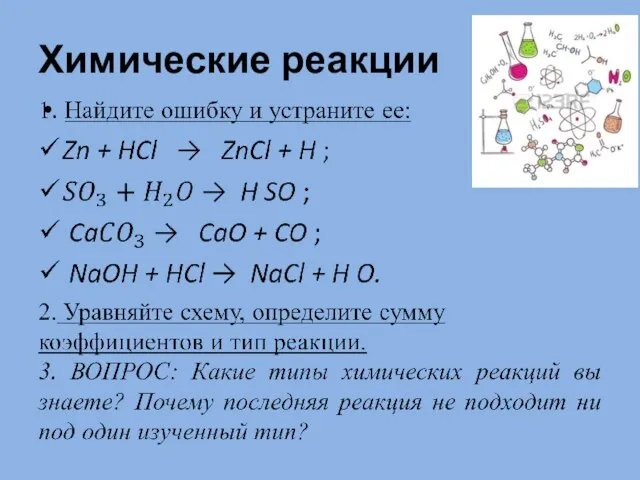 Химические реакции
Химические реакции Аттестационная работа. Углеводы
Аттестационная работа. Углеводы Типы химических связей
Типы химических связей Классификация неорганических веществ
Классификация неорганических веществ Презентация на тему Волокна
Презентация на тему Волокна  Плотность вещества
Плотность вещества Квантовая химия
Квантовая химия Презентация на тему Состав, строение и свойства стекла и хрусталя
Презентация на тему Состав, строение и свойства стекла и хрусталя  Акцепторы катионов и анионов. Хиральные краунэфиры. Гетерокрауны, гетерокриптанды, циклофаны
Акцепторы катионов и анионов. Хиральные краунэфиры. Гетерокрауны, гетерокриптанды, циклофаны Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Получение и применение аренов
Получение и применение аренов Презентация на тему Щавелевая кислота
Презентация на тему Щавелевая кислота