Содержание
- 2. B
- 3. (атом кислорода)
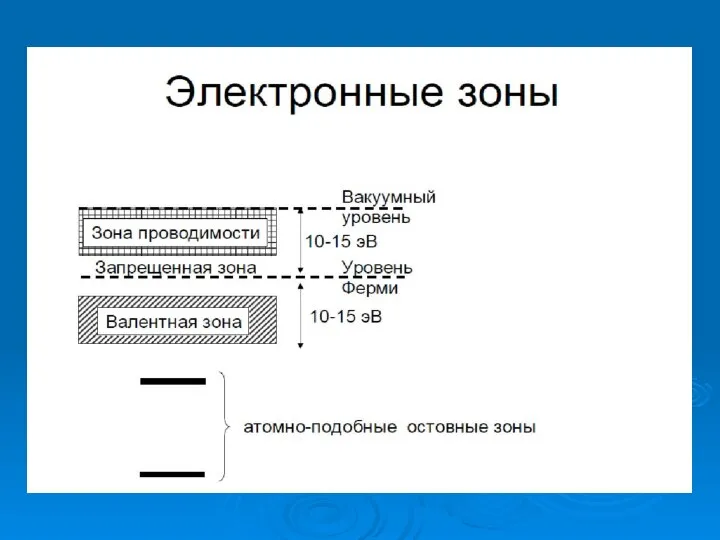
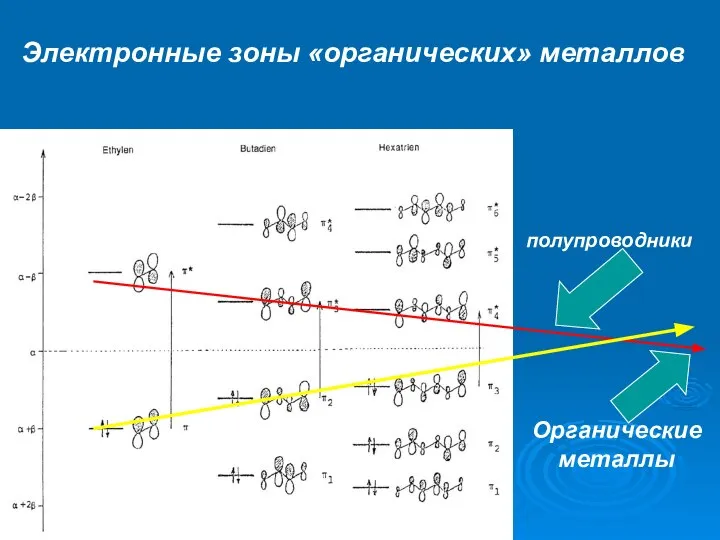
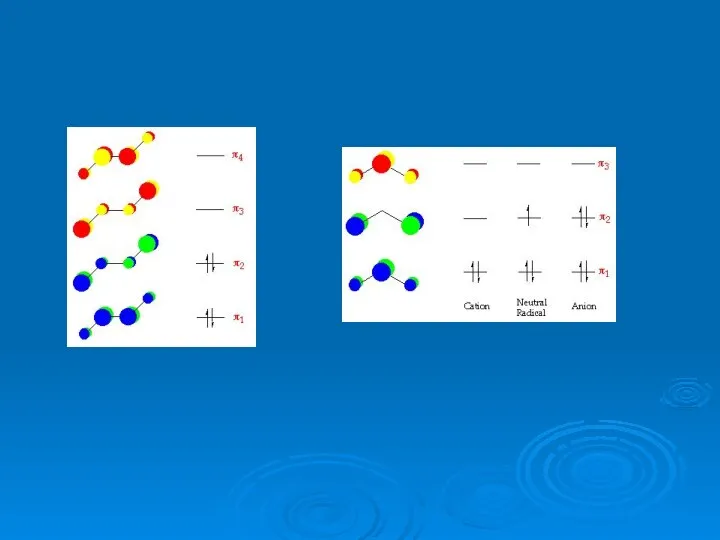
- 7. Органические металлы полупроводники Электронные зоны «органических» металлов
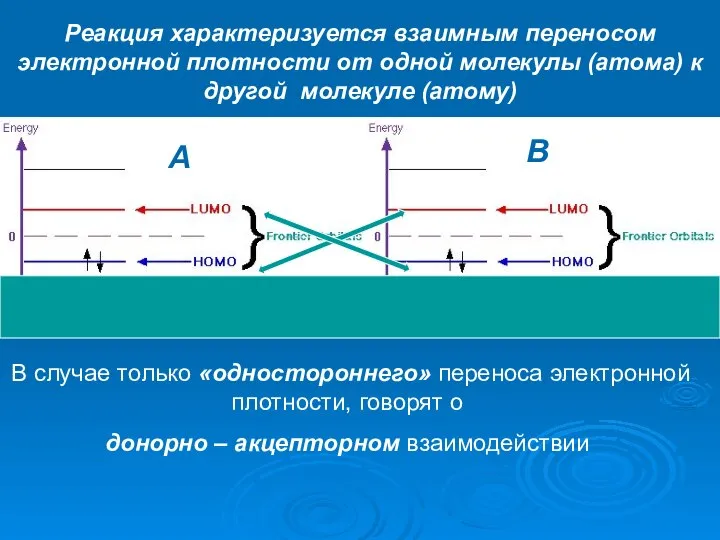
- 8. A B Реакция характеризуется взаимным переносом электронной плотности от одной молекулы (атома) к другой молекуле (атому)
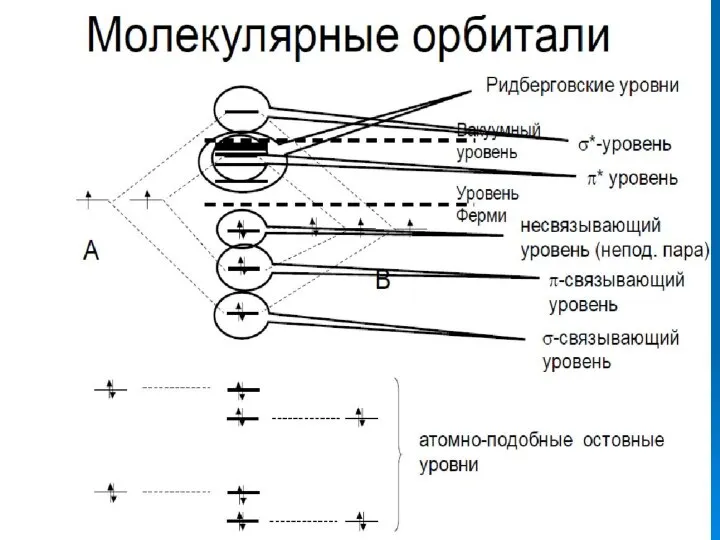
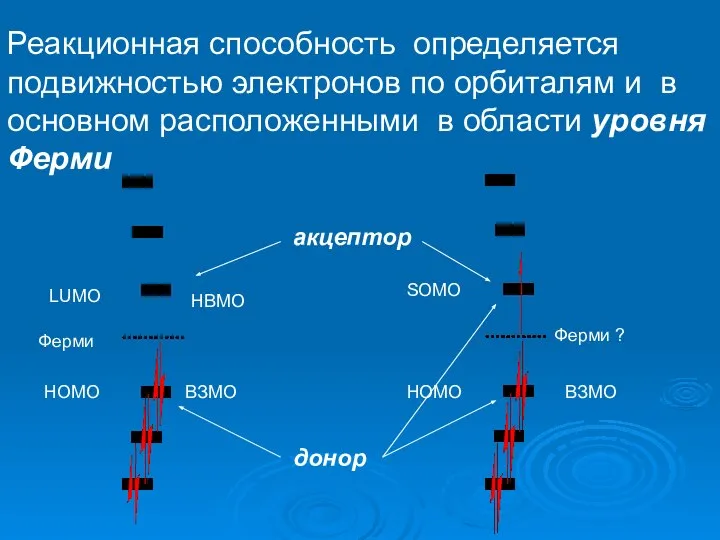
- 9. B Реакционная способность определяется подвижностью электронов по орбиталям и в основном расположенными в области уровня Ферми
- 10. Свойства валентных электронных уровней (10 – 15 эВ ниже уровня Ферми) и вакантных электронных уровней (10
- 11. Очевидно, что реакционная способность молекул зависит от расположения (т.е. энергии) МО надо только освободить молекулу, «отпустить»
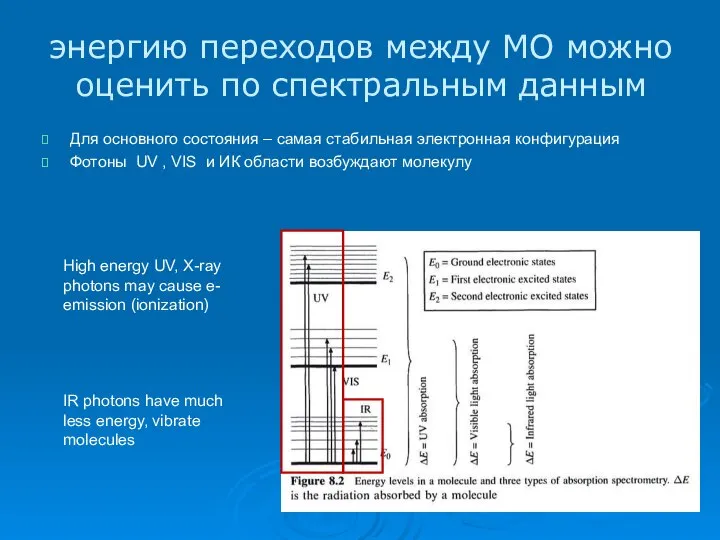
- 12. энергию переходов между МО можно оценить по спектральным данным Для основного состояния – самая стабильная электронная
- 13. UV-Visible + IR Spectroscopic Methods Introduction to the Principles of Spectroscopy
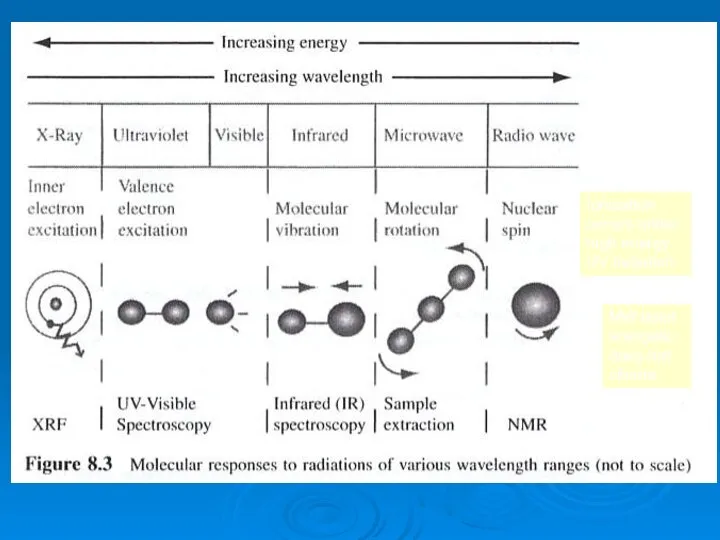
- 14. UV-Visible + IR Spectroscopic Methods Introduction to the Principles of Spectroscopy Ionization occurs under high energy
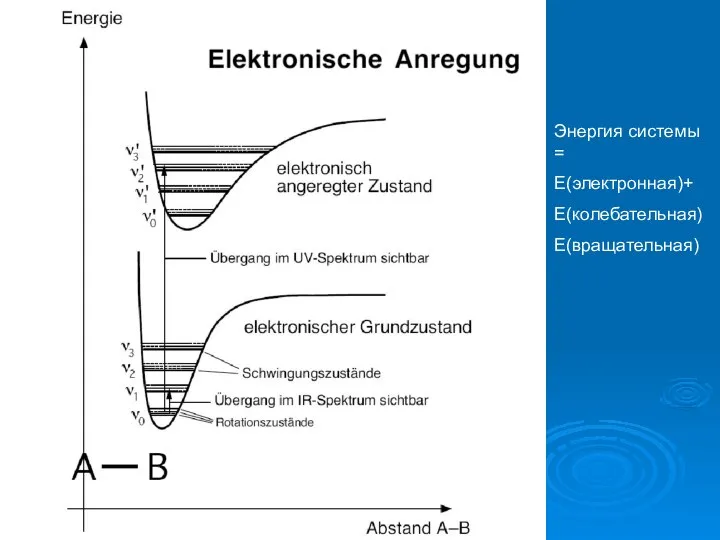
- 15. Энергия системы = Е(электронная)+ Е(колебательная) Е(вращательная)
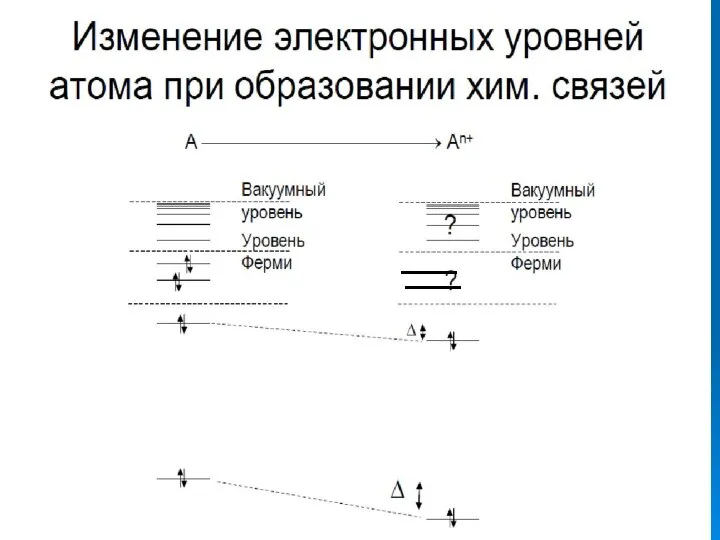
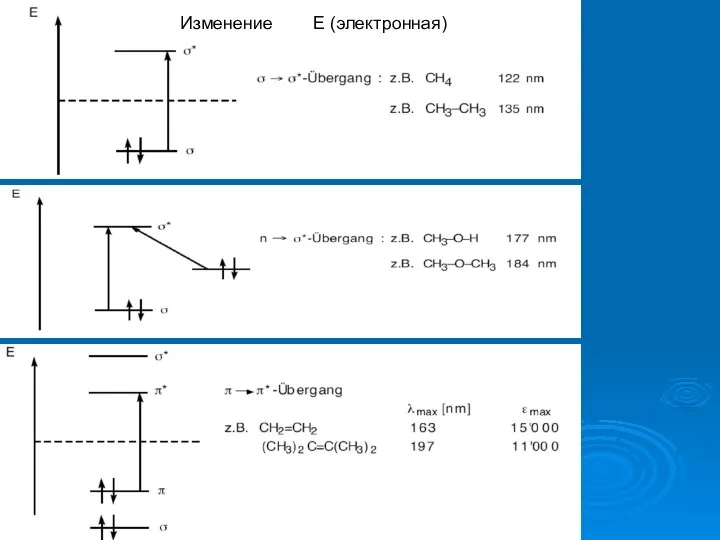
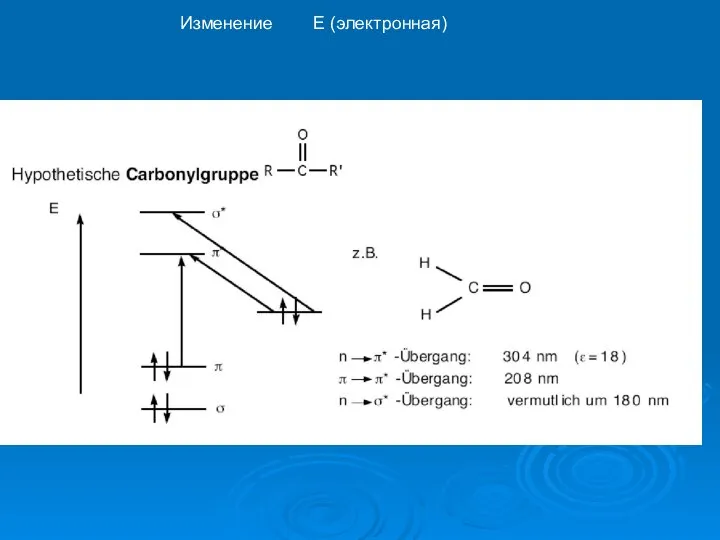
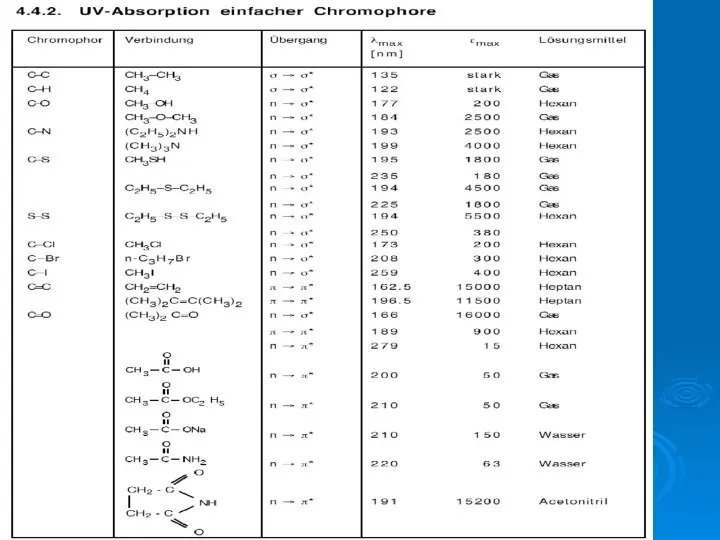
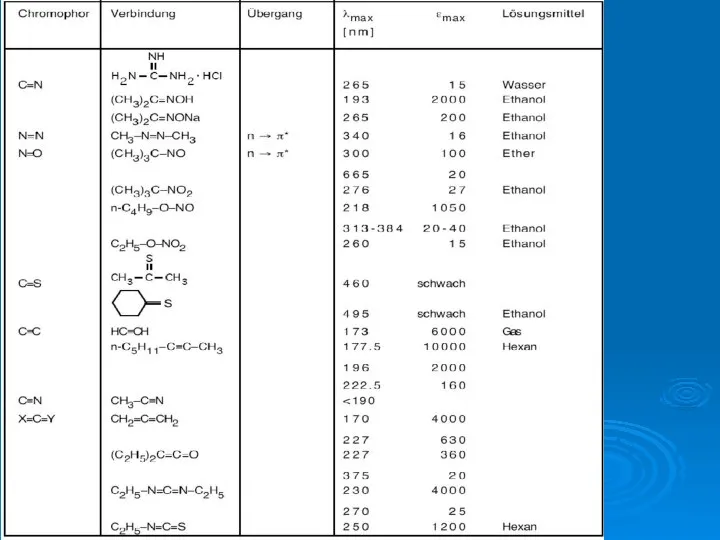
- 16. Изменение Е (электронная)
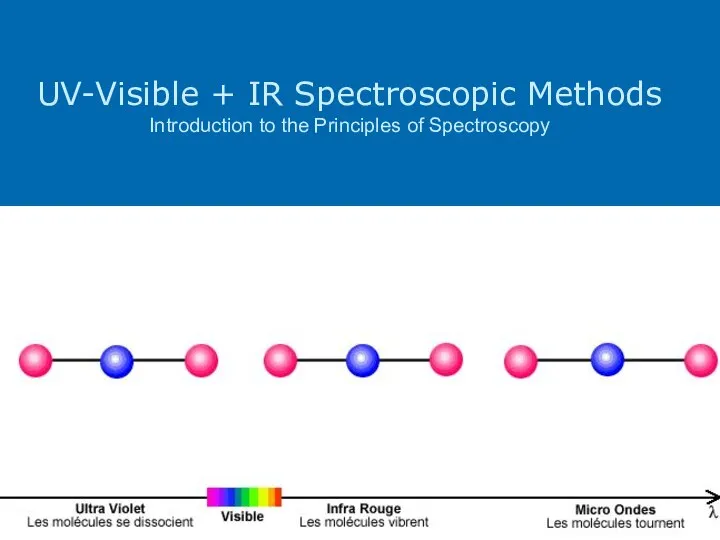
- 17. Изменение Е (электронная)
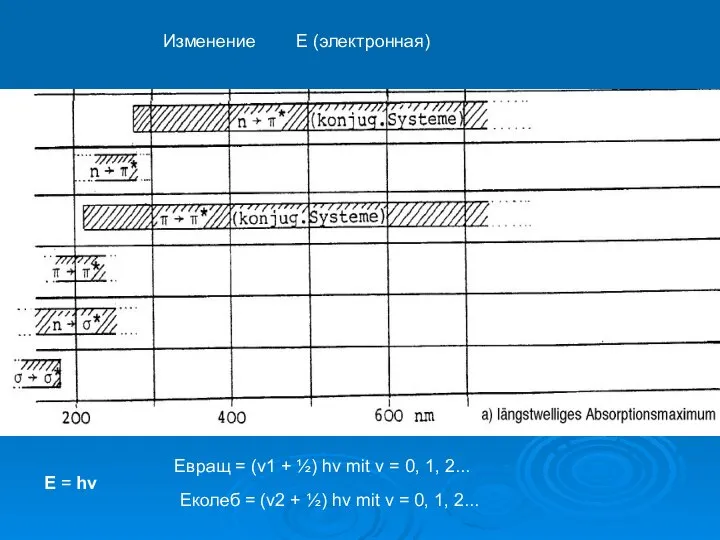
- 20. Изменение Е (электронная) E = hν Eвращ = (v1 + ½) hν mit v = 0,
- 21. 3. Inversion in an SN2 Reaction
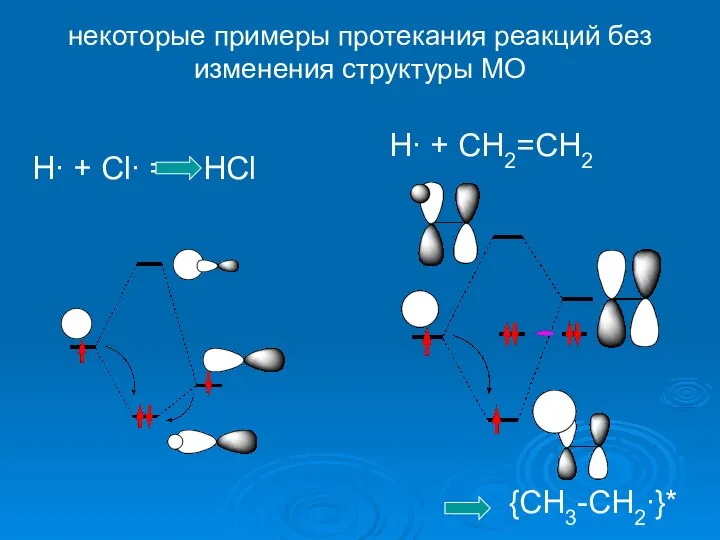
- 22. некоторые примеры протекания реакций без изменения структуры МО H∙ + Cl∙ = HCl H∙ + CH2=CH2
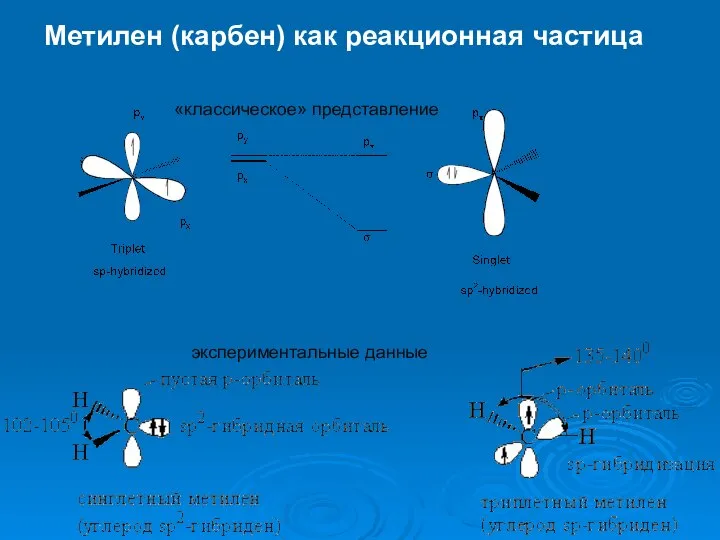
- 23. Метилен (карбен) как реакционная частица «классическое» представление экспериментальные данные
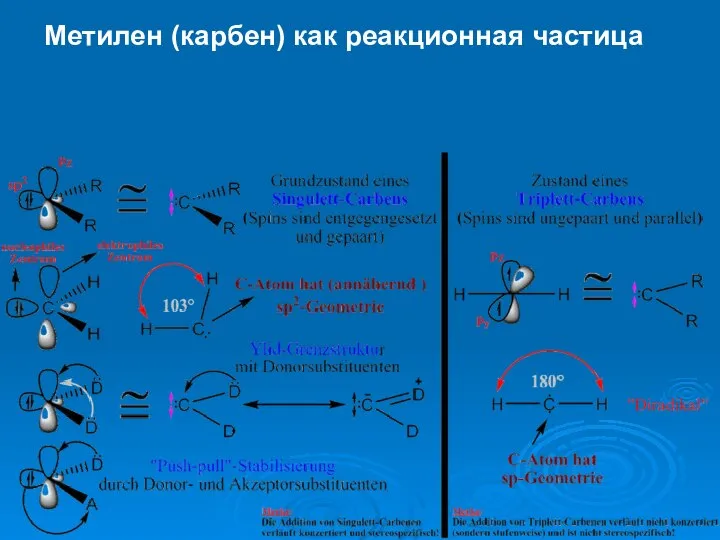
- 24. Метилен (карбен) как реакционная частица
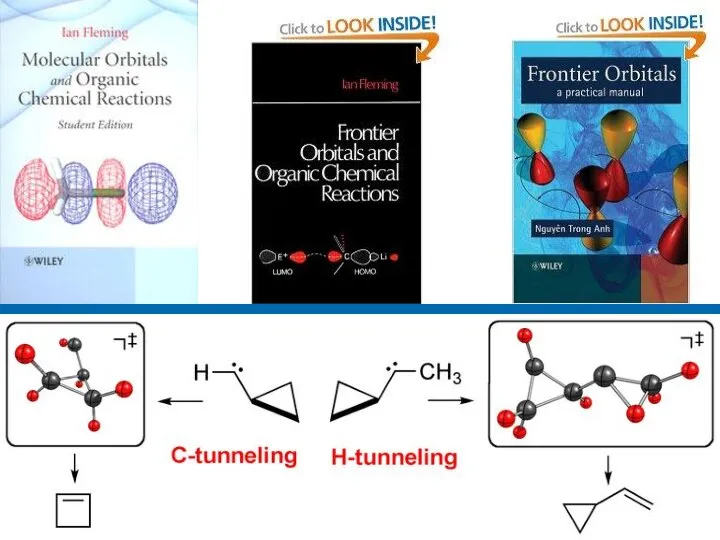
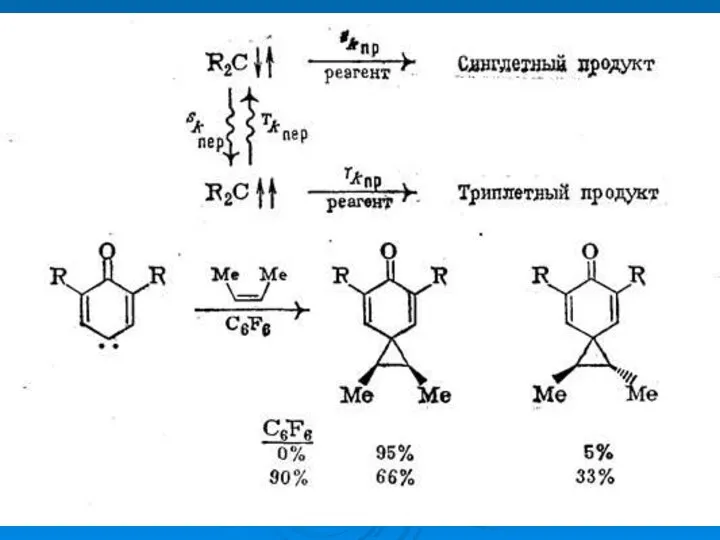
- 25. Присоединение синглетной формы карбена по двойной связи происходит, строго стереоспецифично.
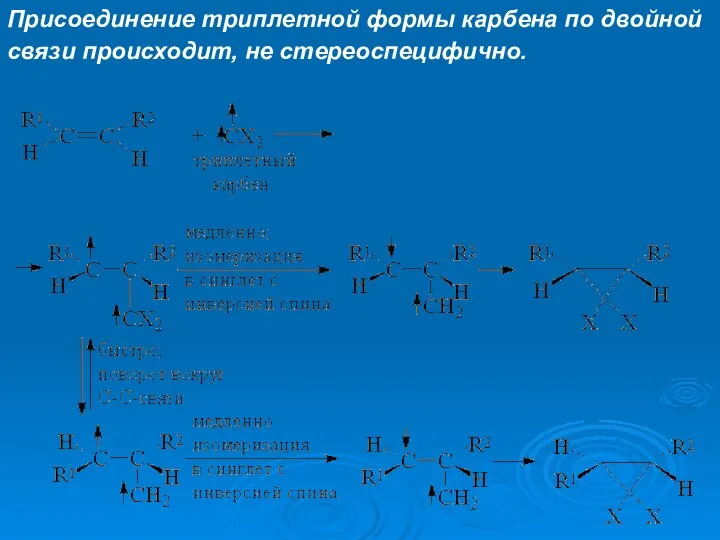
- 26. Присоединение триплетной формы карбена по двойной связи происходит, не стереоспецифично.
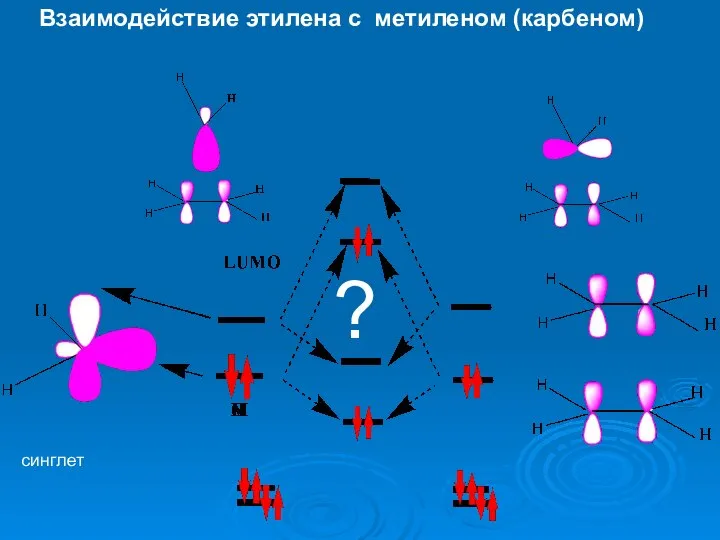
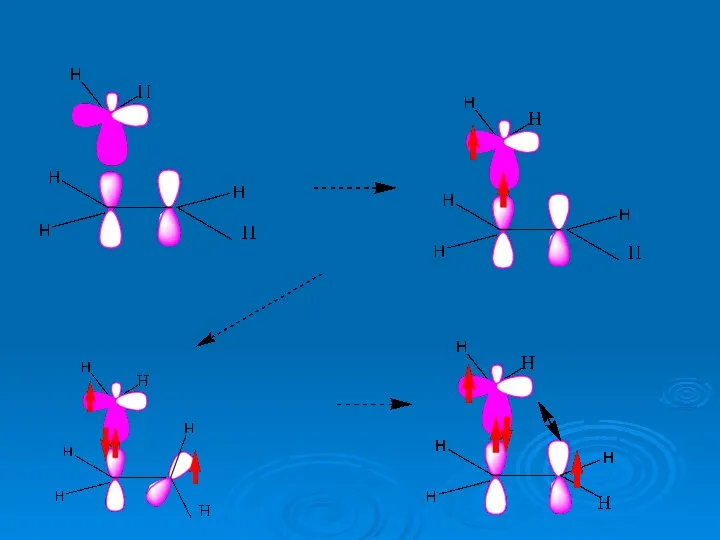
- 28. Взаимодействие этилена с метиленом (карбеном) синглет ?
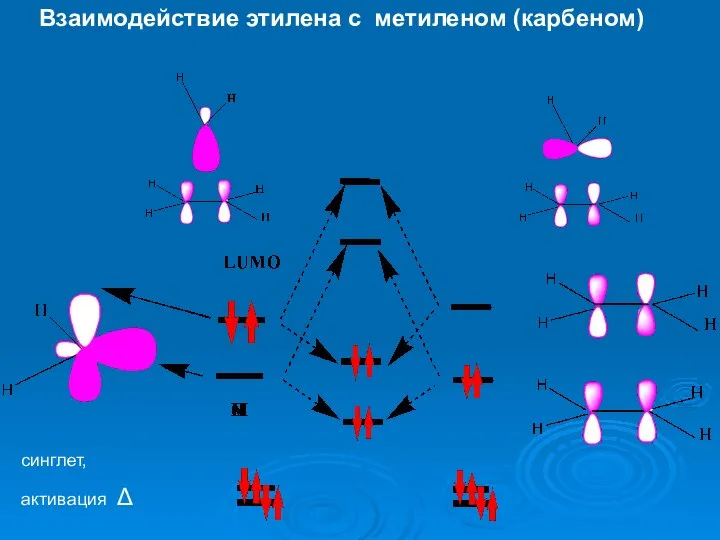
- 29. Взаимодействие этилена с метиленом (карбеном) синглет, активация Δ
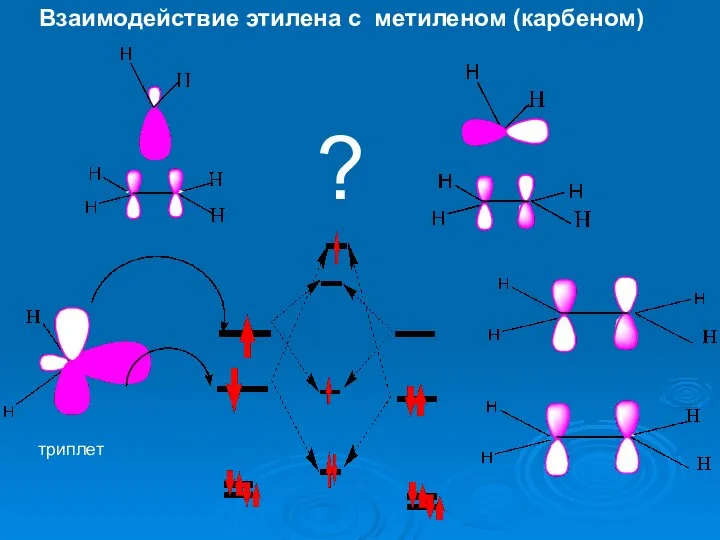
- 30. Взаимодействие этилена с метиленом (карбеном) триплет ?
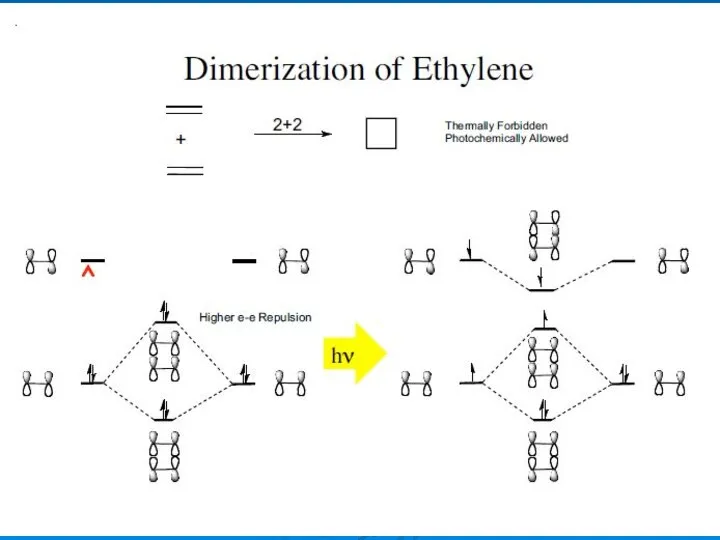
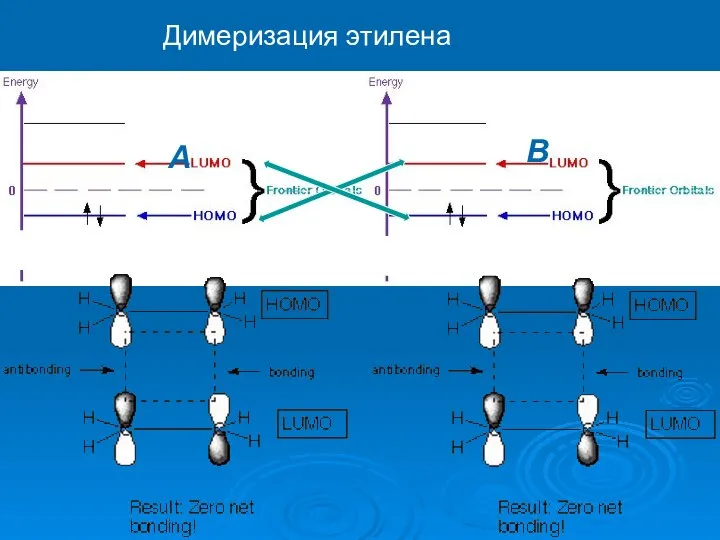
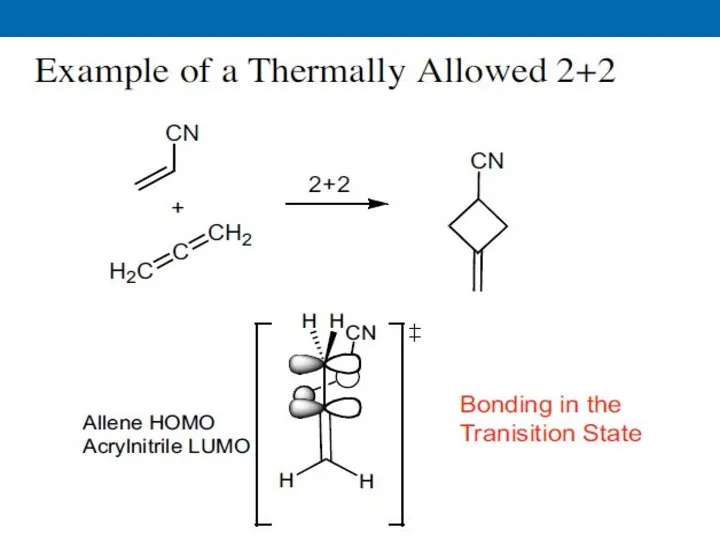
- 33. A B Димеризация этилена
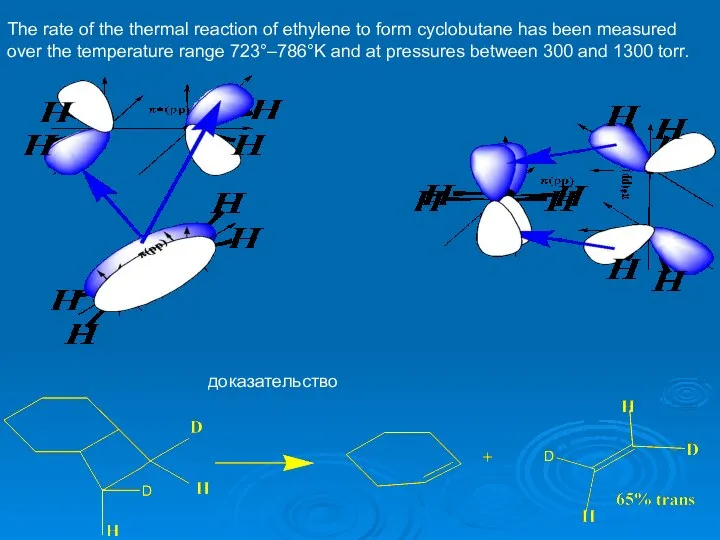
- 34. The rate of the thermal reaction of ethylene to form cyclobutane has been measured over the
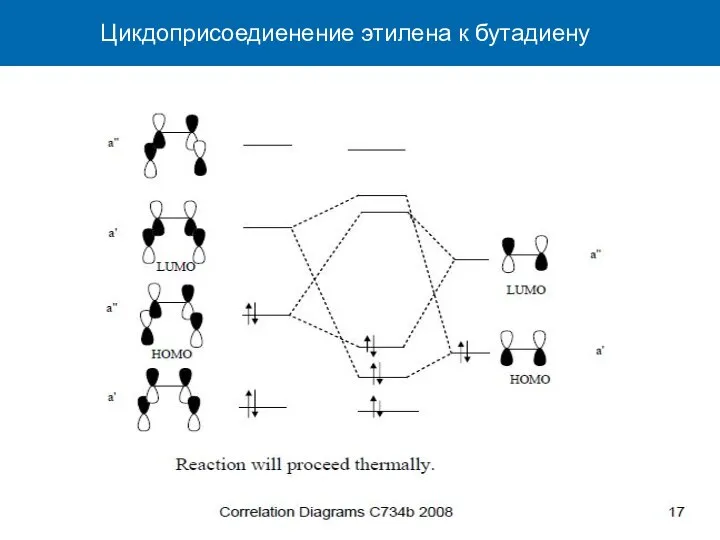
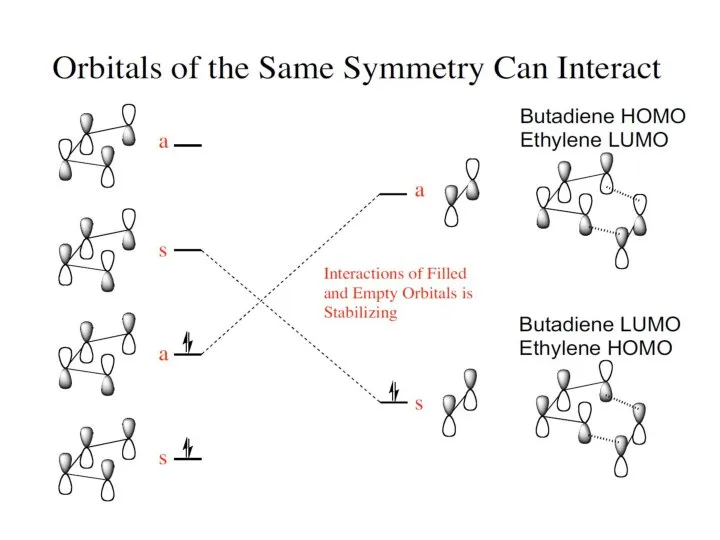
- 36. Цикдоприсоедиенение этилена к бутадиену
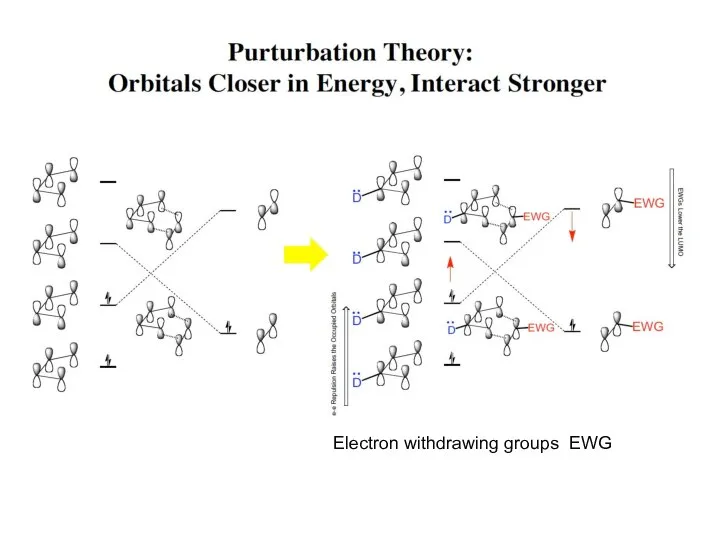
- 38. Electron withdrawing groups EWG
- 39. реакционная способность молекул зависит не только от расположения МО, но и от их строения Однако, необходимо
- 40. некоторые примеры протекания реакций с изменением структуры МО
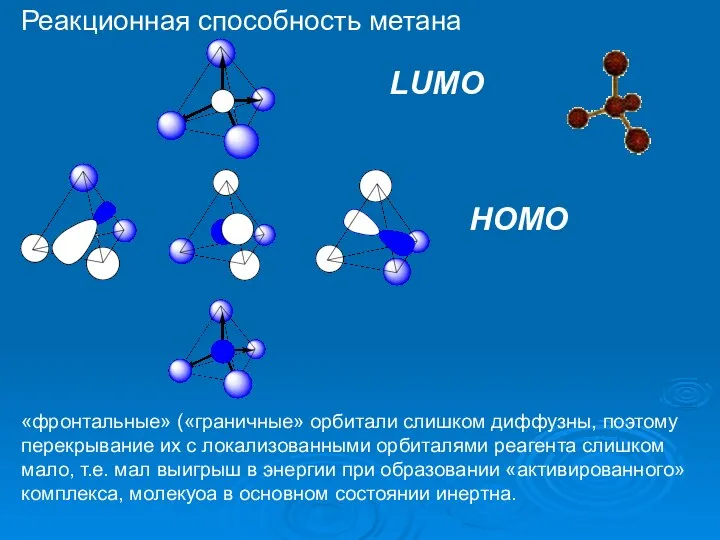
- 41. LUMO HOMO «фронтальные» («граничные» орбитали слишком диффузны, поэтому перекрывание их с локализованными орбиталями реагента слишком мало,
- 42. Реакционная способность метана Вращение молекулы не может вызвать изменение геометрии орбиталей (в данном случае – изменение
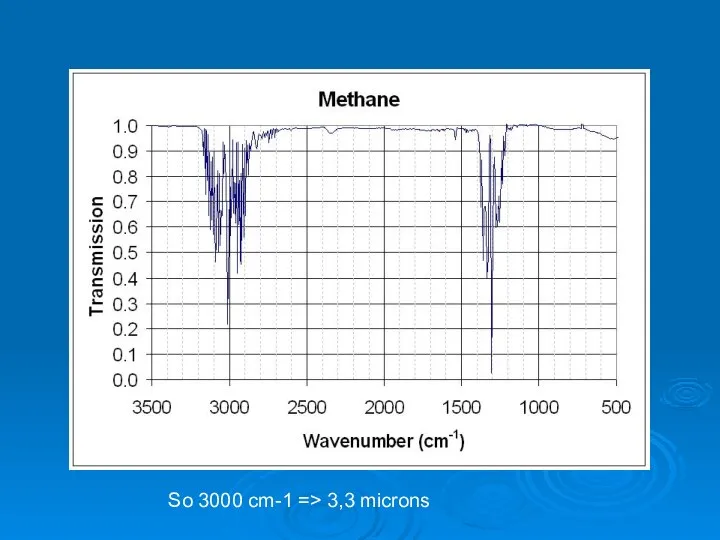
- 43. So 3000 cm-1 => 3,3 microns
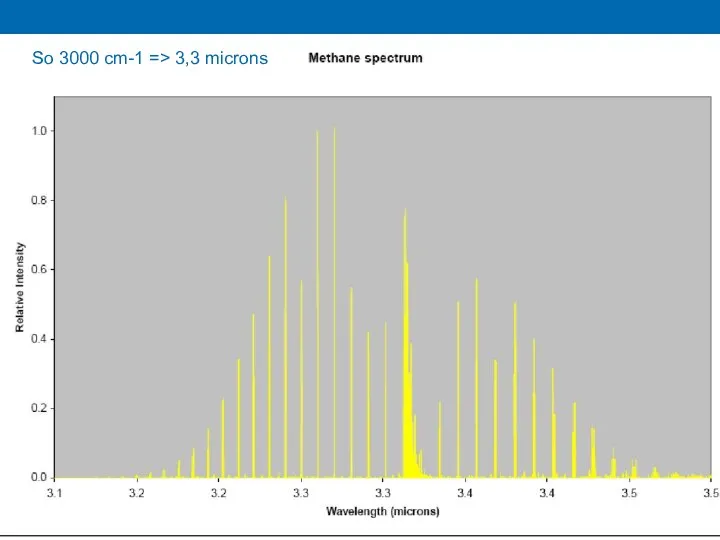
- 45. So 3000 cm-1 => 3,3 microns
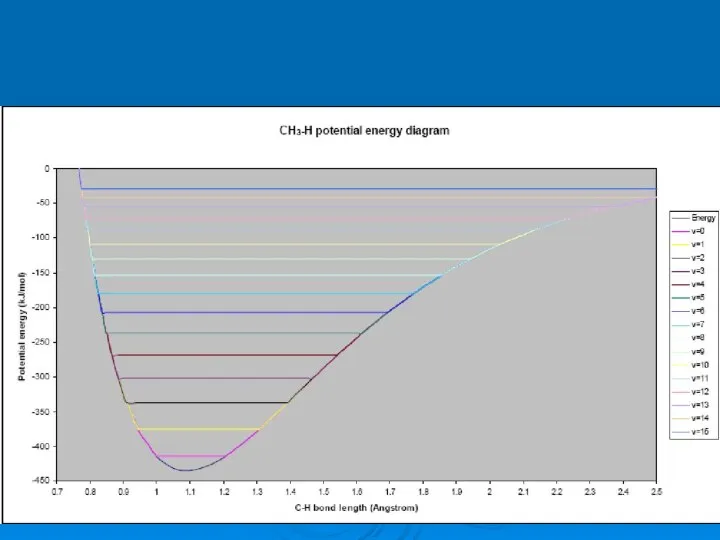
- 46. Основные колебания в метане Образование треугольной пирамиды
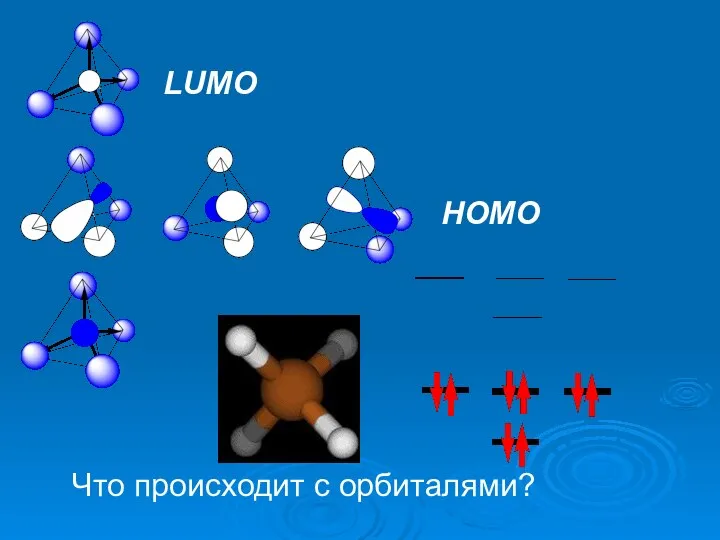
- 47. LUMO HOMO Что происходит с орбиталями?
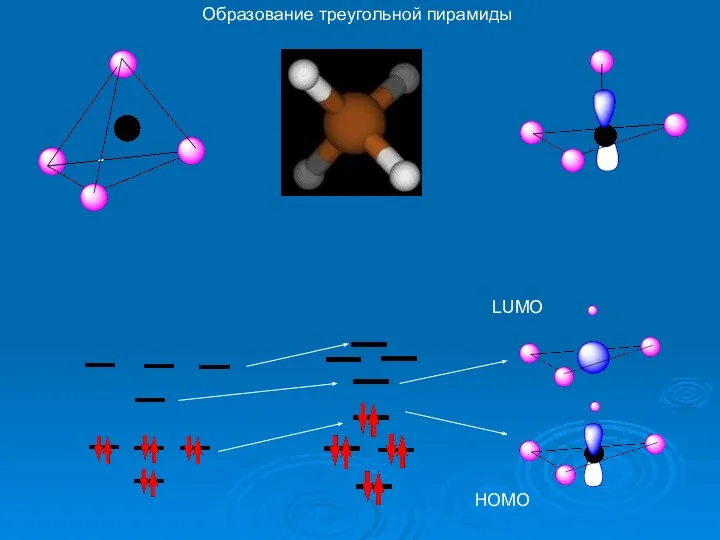
- 48. Образование треугольной пирамиды LUMO HOMO
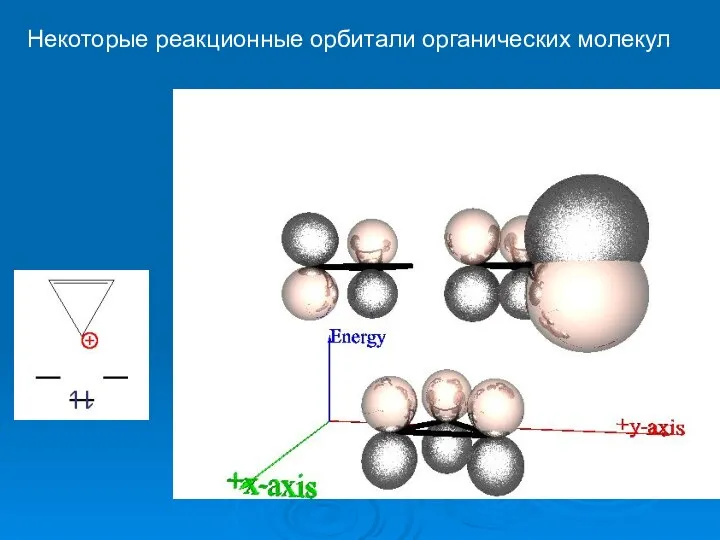
- 50. Некоторые реакционные орбитали органических молекул
- 55. Скачать презентацию









 Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны
Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны Химия и сельское хозяйство
Химия и сельское хозяйство Оксидтер мен негіздердің реакциялары
Оксидтер мен негіздердің реакциялары Алгоритмы при изучении химии
Алгоритмы при изучении химии Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Алкины и их свойства
Алкины и их свойства Химия и автомобиль
Химия и автомобиль Углеводороды: изомерия
Углеводороды: изомерия Амилаза. Строение амилазы
Амилаза. Строение амилазы Минеральные кислоты. Взаимодействие с простыми веществами
Минеральные кислоты. Взаимодействие с простыми веществами Энергетические уровни
Энергетические уровни Углеводороды (УВ)
Углеводороды (УВ) Олеиновая кислота
Олеиновая кислота Химия һәм сәламәт яшәү рәвеше
Химия һәм сәламәт яшәү рәвеше Презентация на тему Кальций
Презентация на тему Кальций  Арены. Бензол
Арены. Бензол Задания для подготовки к ЕГЭ по химии
Задания для подготовки к ЕГЭ по химии Окислительные свойства концентрированной серной кислоты
Окислительные свойства концентрированной серной кислоты Любовь и химия
Любовь и химия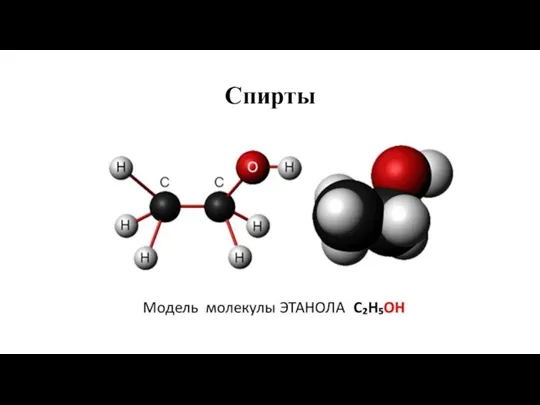 Спирты
Спирты Алкены. Этилен C2H4
Алкены. Этилен C2H4 Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Окисление этанола оксидом меди
Окисление этанола оксидом меди Смачивание и не смачивание жидкости. Капилляры
Смачивание и не смачивание жидкости. Капилляры Карбоновые кислоты
Карбоновые кислоты Предмет органической химии. Урок №1
Предмет органической химии. Урок №1 Характеристика кислорода и серы
Характеристика кислорода и серы Свойства ртути
Свойства ртути