Содержание
- 2. Классификация систем и их характеристики. В зависимости от однородности различают гомогенные и гетерогенные системы. Гомогенная система
- 3. Классификация систем и их характеристики. В зависимости от характера взаимодействия с окружающей средой различают системы изолированные,
- 4. Параметры Состояние системы характеризуется определенной совокупностью физических и химических величин, которые называются параметрами системы. Параметрами являются:
- 5. Параметры Экстенсивные параметры - параметры, значения которых пропорциональны числу частиц в системе (масса, объем, количество вещества).
- 6. Функции состояния Наряду с параметрами для характеристики состояния системы используют функции состояния. Их значения рассчитывают по
- 7. Процесс Переход системы из одного состояния в другое является процессом. Процесс - это переход системы из
- 8. Энергия Энергия (Е) - количественная мера интенсивности различных форм перемещения и взаимодействия частиц в системе, включая
- 9. Для описания энергетического состояния системы используется ее функция состояния - внутренняя энергия (U, кДж/моль). Внутренняя энергия
- 10. Абсолютное значение внутренней энергии определить невозможно, так как любая термодинамическая система материальна, а материя - с
- 11. Обмен энергией может осуществляться в виде работы и теплоты Работа - энергетическая мера направленных форм движения
- 12. Наряду с энергией для характеристики движения частиц в термодинамике используется еще одна функция состояния - энтропия.
- 13. Первый закон (первое начало) термодинамики - это всеобщий закон природы, закон сохранения и превращения энергии, соответствующий
- 14. Второй закон (второе начало) термодинамики определяет направленность и пределы протекания самопроизвольных процессов. В изолированных системах самопроизвольно
- 15. Для неизолированных систем нужно учитывать не только изменение энтропии, но и изменение энергии. Поэтому необходимо рассматривать
- 16. Лекция 8. 2017/2018 Второй закон термодинамики для любых систем формулируется следующим образом: В системе при постоянной
- 18. Скачать презентацию















 Практическая работа по теме Получение и свойства соединений металлов
Практическая работа по теме Получение и свойства соединений металлов Соли в природе. Реакции с участием солей. Модуль 2. Лекция 2.1
Соли в природе. Реакции с участием солей. Модуль 2. Лекция 2.1 Её величество – вода Интегрированный урок химии в 8 классе
Её величество – вода Интегрированный урок химии в 8 классе Zirconium Dioxide
Zirconium Dioxide Неорганическая химия 1 семестра. Растворы
Неорганическая химия 1 семестра. Растворы Ацилирование. Лекция 4
Ацилирование. Лекция 4 Химический диктант как метод формирующего оценивания
Химический диктант как метод формирующего оценивания Теория валентных связей
Теория валентных связей Презентация на тему Изотопы
Презентация на тему Изотопы  Министерство сельского хозяйства Российской Федерации. Поляграфия и фотоэлектронная спектроскопия
Министерство сельского хозяйства Российской Федерации. Поляграфия и фотоэлектронная спектроскопия Закономерности изменения свойств галогенов
Закономерности изменения свойств галогенов Презентация на тему Характеристика щелочных металлов 9 класс
Презентация на тему Характеристика щелочных металлов 9 класс  Поделочный камень родонит
Поделочный камень родонит Лабораторное оборудование. Тесты
Лабораторное оборудование. Тесты G12 - класс антифризов
G12 - класс антифризов Взвешивание. Аналитические весы
Взвешивание. Аналитические весы Презентация на тему Химические реакции 11 класс
Презентация на тему Химические реакции 11 класс 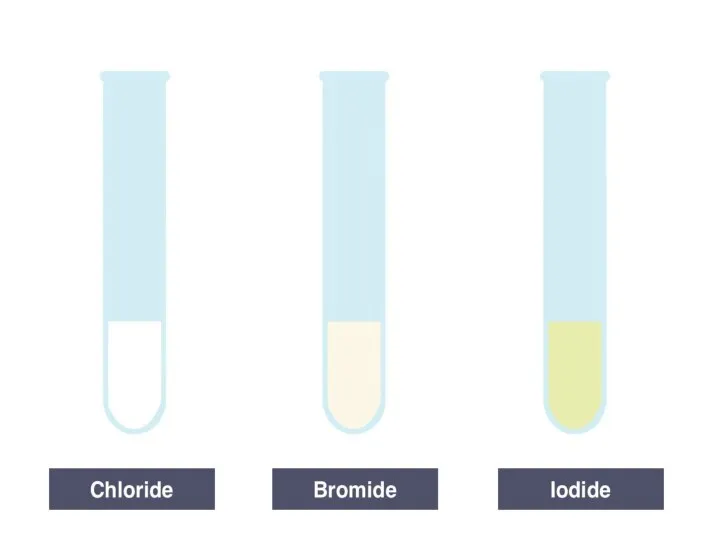 Определение галогенид-ионов в водном растворе. Лабораторный опыт
Определение галогенид-ионов в водном растворе. Лабораторный опыт Конкурс О, химия – ты муза вдохновения!
Конкурс О, химия – ты муза вдохновения! Количество теплоты, для получения углекислого газа. Химическое равновесие. Примеры. (Лекция 4)
Количество теплоты, для получения углекислого газа. Химическое равновесие. Примеры. (Лекция 4) Алкадиены. Строение. Изомерия. Свойства
Алкадиены. Строение. Изомерия. Свойства Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Степень окисления. Составление формул бинарных соединений. 8 класс
Степень окисления. Составление формул бинарных соединений. 8 класс Сложные эфиры и жиры
Сложные эфиры и жиры Алканы и алкены
Алканы и алкены Карбоновые кислоты
Карбоновые кислоты Металлы и их соединения. Решение экспериментальных задач
Металлы и их соединения. Решение экспериментальных задач Анилин как органическое основание
Анилин как органическое основание