Слайд 2ИСТОРИЯ
Квантовая химия зародилась
в середине 20-х годов XX столетия.

Слайд 3ПРИЧИНЫ ВОЗНИКНОВЕНИЯ
Экспериментальный материал нуждался
в интерпретации.
Слайд 4ИССЛЕДОВАНИЯ
ВЕРНЕРА ГЕЙЗЕНБЕРГА
1926 г.

Слайд 5УРАВНЕНИЕ
ШРЁДИНГЕРА
Уравнение
описывает изменение
в пространстве
и во времени
чистого состояния.

Слайд 6ГИПОТЕЗА
ДЕ БРОЙЛЯ
Дуализм не является особенностью только оптических явлений,
а имеет универсальный

характер. Частицы вещества также обладают волновыми свойствами
Слайд 7МЕТОД ХАРТРИ-ФОКА
Дуглас Рейнер Хартри
Владимир Александрович Фок

Слайд 9+
относительная простота
помогает легко представить молекулу
описывает неорганическую химию

Слайд 10-
даёт правильное описание в малой области химических соединений
малая предсказательная способность
не даёт магнитных

свойств веществ и их геометрию
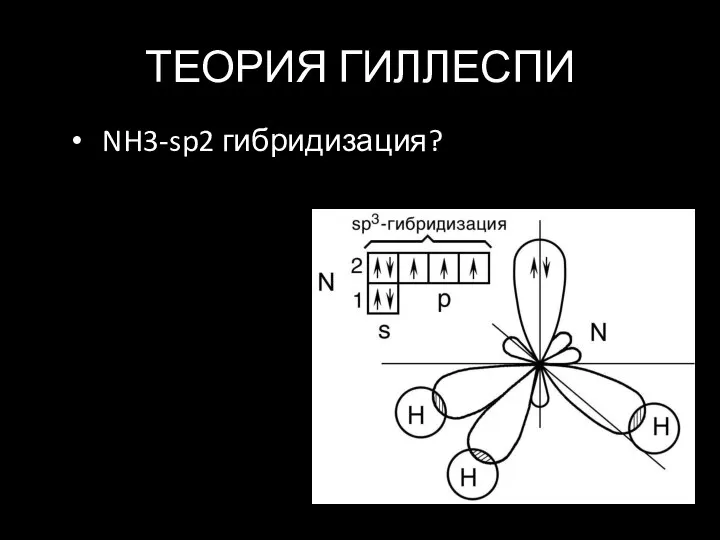
Слайд 12ТЕОРИЯ ГИЛЛЕСПИ
NH3-sp2 гибридизация?
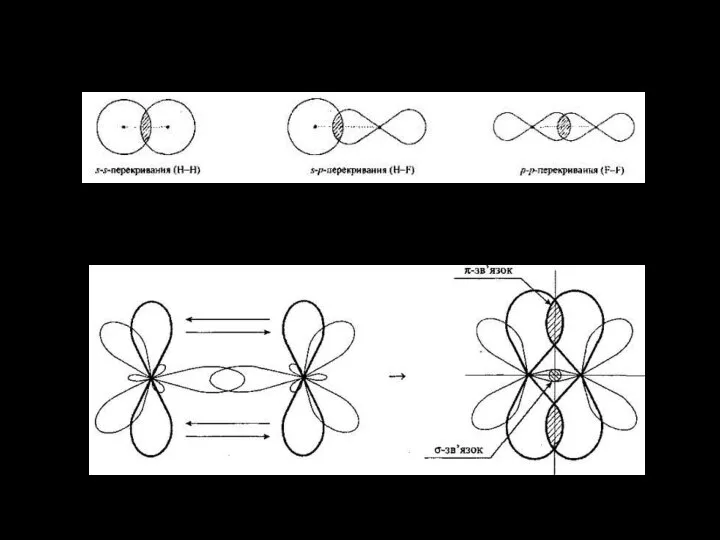
Слайд 13МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
Является наиболее универсальным широко используемым методом описания природы химической связи.

Этот метод базируется на последних достижениях в области квантовой механики.
Слайд 14МЕТОД ЛИНЕЙНОЙ КОМБИНАЦИИ АТОМНЫХ ОРБИТАЛЕЙ
-ПРОСТЕЙШИЙ МЕТОД ОПРЕДЕЛЕНИЯ ВОЛНОВЫХ ФУНКЦИЙ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ.

Слайд 15+
даёт геометрию молекулы
объективнее отражает реальность
имеет сильную предсказательную способность, даже без расчёта
предсказывает магнитные

свойства молекул
относительная простота математики
Слайд 16-
сложность подбора коэффициента для атомной обретали
рост сложности расчёта молекул с ростом количества

атомов
Слайд 18ЭЛЕКТРОННЫЕ ЭФФЕКТЫ
-смещение электронной плотности в молекуле, ионе или радикале под влиянием

заместителей.
Слайд 19ИНДУКТИВНЫЙ ЭФФЕКТ
-эффект переноса электронной плотности вдоль сигма связей.
















 Основания
Основания alkany
alkany Фосфаттардағы байланыс теориясы
Фосфаттардағы байланыс теориясы Методы повышения надежности. Резервирование сложных ХТС
Методы повышения надежности. Резервирование сложных ХТС металлы
металлы Аналитическая химия (ЛЕКЦИЯ 1)
Аналитическая химия (ЛЕКЦИЯ 1) История открытия и изучения каркасных фосфатов структурных типов коснарита и лангбейнита
История открытия и изучения каркасных фосфатов структурных типов коснарита и лангбейнита Презентация на тему Углеводороды (10 класс)
Презентация на тему Углеводороды (10 класс)  Характеристика химического элемента по его положению в периодической системе элементов Д.И. Менделеева
Характеристика химического элемента по его положению в периодической системе элементов Д.И. Менделеева Липиды. Омыляемые липиды. Рубежный контроль №2
Липиды. Омыляемые липиды. Рубежный контроль №2 Ионообменная хроматография в разделении белков
Ионообменная хроматография в разделении белков Ұнтақтар - дәрілік түр ретінде
Ұнтақтар - дәрілік түр ретінде Интересные свойства пластика
Интересные свойства пластика Вода-растворитель. Растворы
Вода-растворитель. Растворы Презентация на тему Коррозия металлов (11 класс)
Презентация на тему Коррозия металлов (11 класс)  Химическое вещество золото
Химическое вещество золото ОВР химияПрезентация
ОВР химияПрезентация Презентация на тему Золото
Презентация на тему Золото  Нитраты
Нитраты Оксиды азота
Оксиды азота Тест- тренажер по теме: Основные классы неорганических веществ Оксиды
Тест- тренажер по теме: Основные классы неорганических веществ Оксиды Органическая химия. Химические свойства и типы реакций. (9 класс)
Органическая химия. Химические свойства и типы реакций. (9 класс) Тестирование по химии
Тестирование по химии Лекции_ ОБМЕН ЛИПИДОВ
Лекции_ ОБМЕН ЛИПИДОВ Способы защиты химического оборудования от коррозии
Способы защиты химического оборудования от коррозии Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Задания по химии
Задания по химии Алюминий
Алюминий