Содержание
- 2. Химическая термодинамика. Термодинамические потенциалы. Термодинамические потенциалы или характеристические функции – термодинамические функции, посредством которых и их
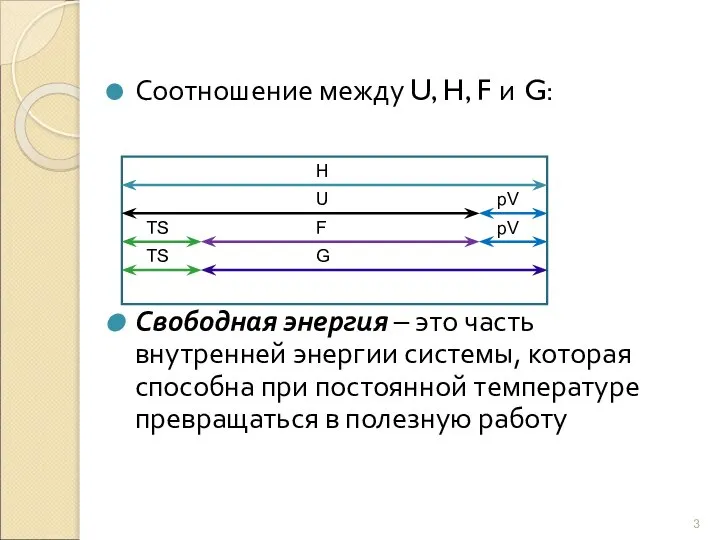
- 3. Соотношение между U, H, F и G: Свободная энергия – это часть внутренней энергии системы, которая
- 4. Теплосодержание системы ΔH = ΔG + TΔS ΔG – свободная энергия Гиббса, часть теплоты, которая может
- 5. Самопроизвольное протекание изохорно-изотермического процесса определяется энергией Гельмгольца (часть внутренней энергии, которую можно перевести в работу) ∆F
- 6. Основное уравнение термодинамики Описывает зависимость термодинамических потенциалов от их естественных переменных Объединяет первое и второе начала
- 7. Если в системе происходит химическая реакция или система открыта (т.е. обменивается с окружающей средой веществом и
- 8. Химический потенциал характеризует приращение соответствующего термодинамического потенциала при изменении количества данного вещества при фиксированных естественных переменных
- 9. Смысл термодинамических потенциалов: зная любой из четырех потенциалов как функцию естественных переменных, можно с помощью основного
- 10. Любой термодинамический потенциал в необратимых самопроизвольных процессах, протекающих при постоянстве естественных переменных, уменьшается и достигает минимума
- 11. В химических процессах одновременно изменяются энтальпия (энергетический запас системы) и энтропия (не совершающая работу энергия). Анализ
- 12. По определению энергия Гиббса G = H – TS Если продукты реакции и исходные вещества находятся
- 13. Изотермический равновесный процесс без затраты внешних сил может протекать самопроизвольно только в направлении убывания энергии Гиббса
- 14. Стандартная энергия Гиббса (при р=1 бар и Т=298К) Большинство процессов протекает при температурах более высоких, чем
- 16. Скачать презентацию












 Викторина. Химический элементарий. Д.И. Менделеев – гордость русской науки
Викторина. Химический элементарий. Д.И. Менделеев – гордость русской науки Охрана родников Ногликского района и анализ воды из этих родников
Охрана родников Ногликского района и анализ воды из этих родников каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами
каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами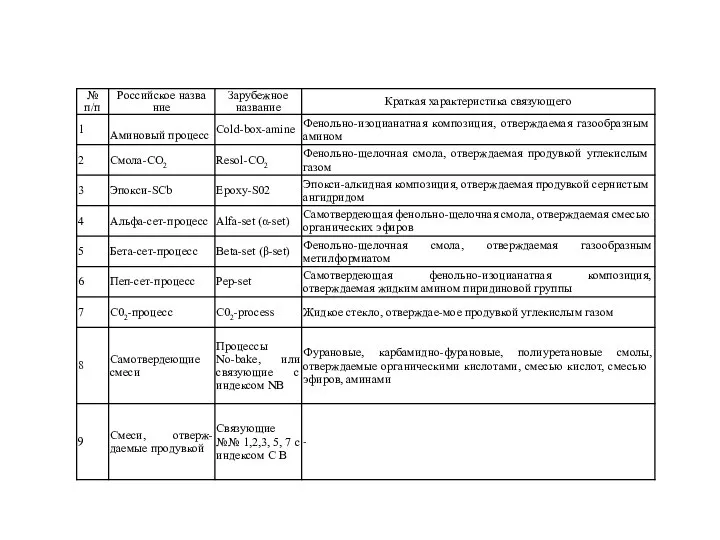 Фенольно-изоцианатная композиция
Фенольно-изоцианатная композиция Растворы. Определение
Растворы. Определение Как решить задания тестов ЕГЭ по химии, если знания на базовом уровне. Метод исключения
Как решить задания тестов ЕГЭ по химии, если знания на базовом уровне. Метод исключения Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия
Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания
Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Алкины. Строение, номенклатура, изометрия, физические свойства
Алкины. Строение, номенклатура, изометрия, физические свойства Практикум по химии и технологии нефти и газа
Практикум по химии и технологии нефти и газа Атомы химических элементов
Атомы химических элементов Общая характеристика элементов подгруппы углерода. Углерод как простое вещество
Общая характеристика элементов подгруппы углерода. Углерод как простое вещество Синтез-газ
Синтез-газ Галогеналканы и реакции отщепления
Галогеналканы и реакции отщепления Бинарные соединения – оксиды и летучие водородные соединения. 8 класс
Бинарные соединения – оксиды и летучие водородные соединения. 8 класс Структура металлов, сплавов, интерметаллидов и квазикристаллов
Структура металлов, сплавов, интерметаллидов и квазикристаллов Формула аспирина. Решение задач
Формула аспирина. Решение задач Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация на тему Комплексные соединения
Презентация на тему Комплексные соединения  Терпеноиды. Эфирные масла
Терпеноиды. Эфирные масла Практическая работа №1. Определение содержания нитратов в овощах и фруктах
Практическая работа №1. Определение содержания нитратов в овощах и фруктах Альдегиды и кетоны
Альдегиды и кетоны Квантовая химия
Квантовая химия Химия и сельское хозяйство
Химия и сельское хозяйство Алкины
Алкины Химия в нашей жизни
Химия в нашей жизни Альдегиды, свойства, получение, применение
Альдегиды, свойства, получение, применение