Слайд 2Общая характеристика Общая характеристика VI-Общая характеристика VI-а подгруппы
Сера
Сероводород и сульфиды
Оксиды серы
Оксид серы

(Оксид серы (IV)
Оксид серы (Оксид серы (VI)
Сернистая кислота
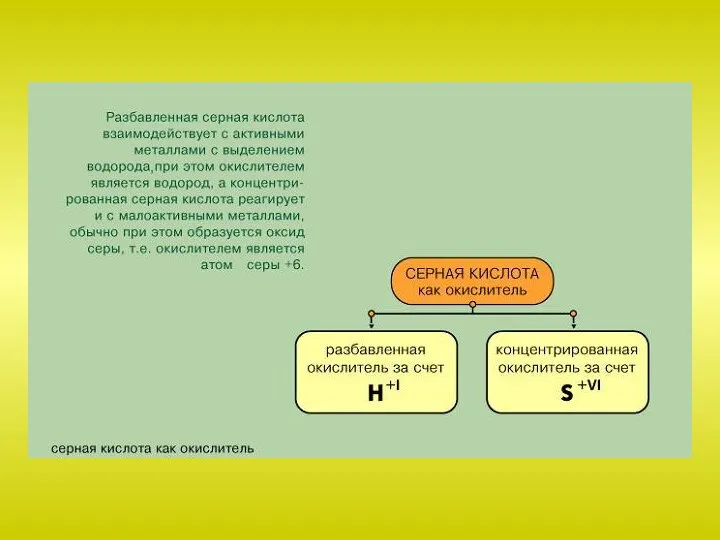
Серная кислота
Слайд 3Общая характеристика VI-а подгруппы

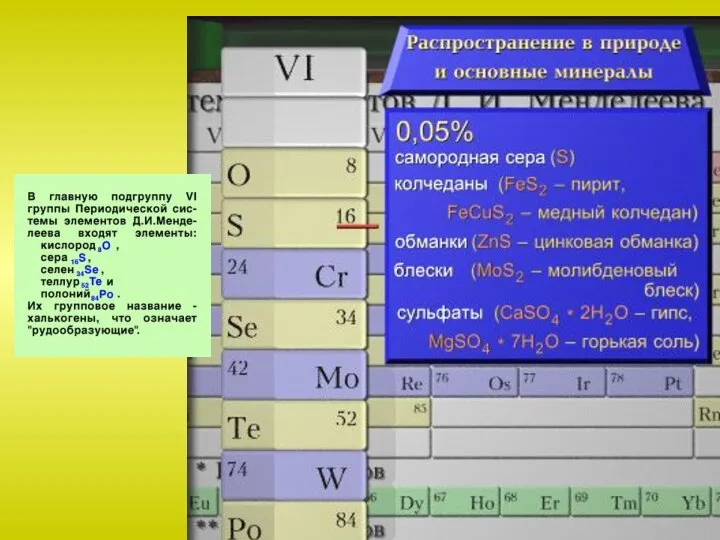
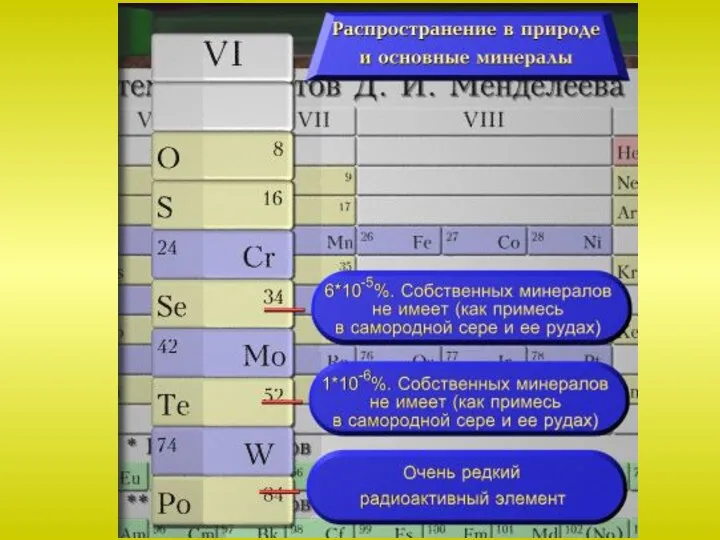
Слайд 13Сера известна с давних времен. В природе встречается в свободном и связанном

виде. Общее содержание серы по массе в земной коре составляет около 0,1% или 0,7% массы планеты. Главная масса серы в виде сульфидов металлов находится в мантии Земли на глубине 1100-1400 км.
Слайд 14Известно несколько аллотропных модификаций серы. До температуры 150°C молекула серы имеет циклическую

форму. Это кольцо из 8 атомов, соединенных в виде короны. В обычных условиях это кристаллы так называемой ромбической модификации. При повышении температуры до 100°С она превращается в моноклинную. Расплавленная сера при 187°C становится очень вязкой, кольца S8 разрываются и происходит полимеризация в виде спиральных молекул с длиной цепи до 10 000 атомов. При дальнейшем нагревании эти молекулы разрываются и вязкость уменьшается. Охлаждая такой расплав атомы серы образуют пластическую серу, которая через некоторое время переходит в кристаллическую ромбическую модификацию.
Слайд 16В воде сера не растворяется (всплывает), растворима в органических растворителях. Диэлектрик.

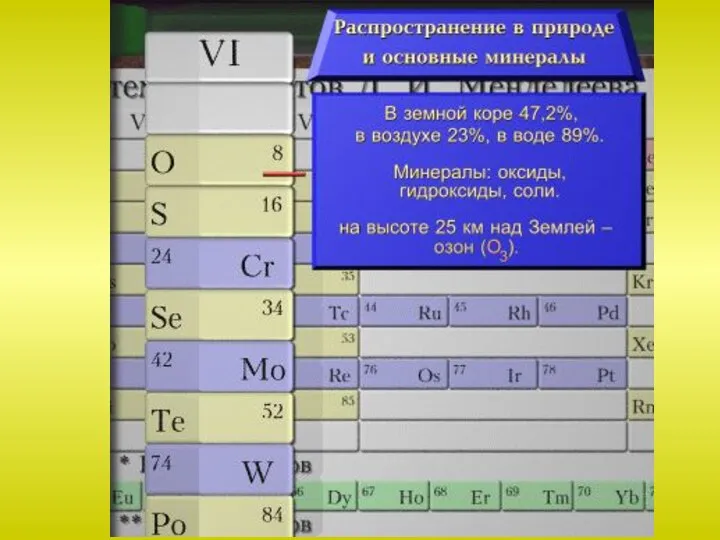
Слайд 17Элементы подгруппы кислорода в значительной мере отличаются от кислорода, прежде всего в

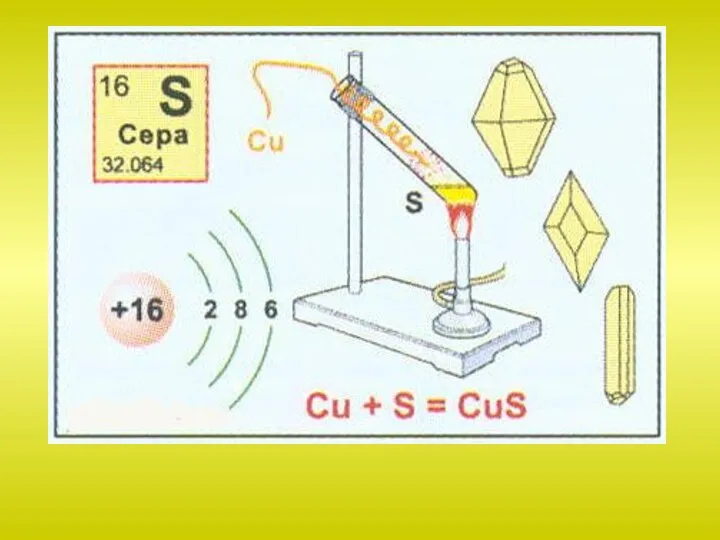
способности проявлять положительные степени окисления. На внешнем электронном слое у атома серы шесть электронов. Формула электронной конфигурации 3s23p4. Взаимодействуя с менее электроотрицательными элементами сера может принимать 2 электрона, проявляя степень окисления –2. Также сера способна отдавать электроны, проявляя степень окисления от +2 до +6, причем только в соединениях с кислородом и некоторыми галогенами.
Слайд 18Сера – активный неметалл. Среди металлов только золото, платина и рутений не
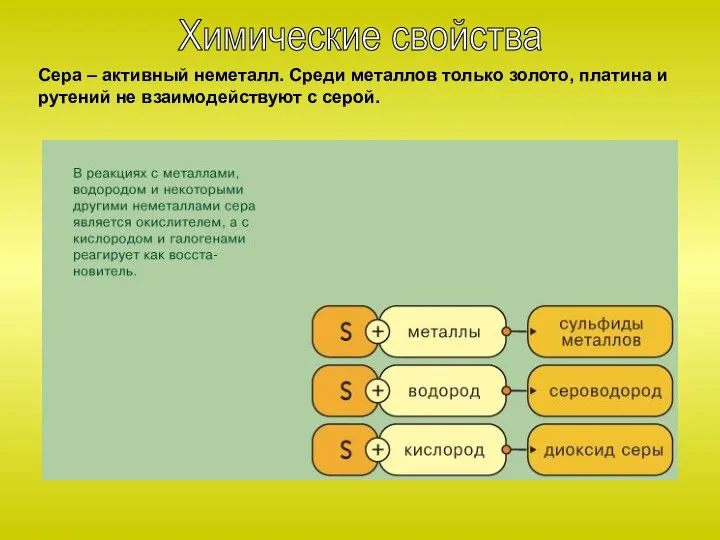
взаимодействуют с серой.
Химические свойства
Слайд 19При нагревании сера реагирует с водородом, образуя сероводород:
S + Н2 = H2S
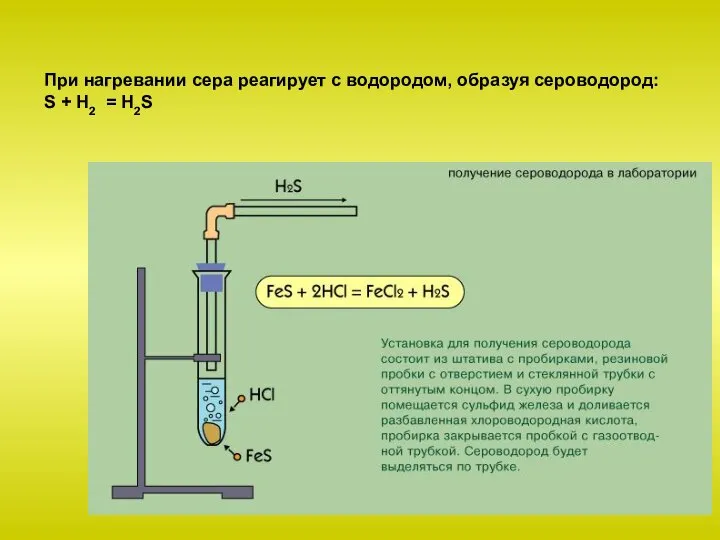
Слайд 20Сера взаимодействует со многими металлами, образуя сульфиды:
S + Fe = FeS
2Al +

3S = Al2S3
Слайд 21Из неметаллов только азот и йод не соединяются с серой. Сжигание серы

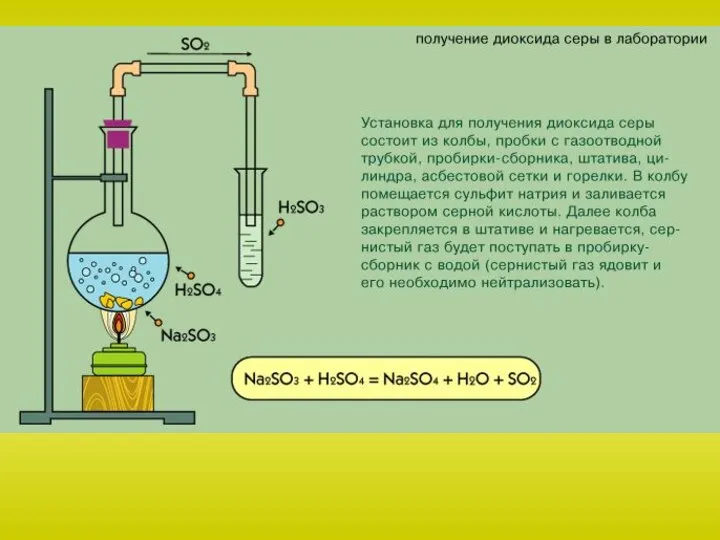
в струе кислорода приводит к образованию сернистого газа или сернистого ангидрида SO2:
S + O2 = SO2
Элементарная сера может также проявлять восстановительные свойства:
S + 2HNO3 = H2SO4 + 2NO
Слайд 23Сера используется при вулканизации каучука, приготовления черного пороха, спичек, ядохимикатов, для получения

серной кислоты.
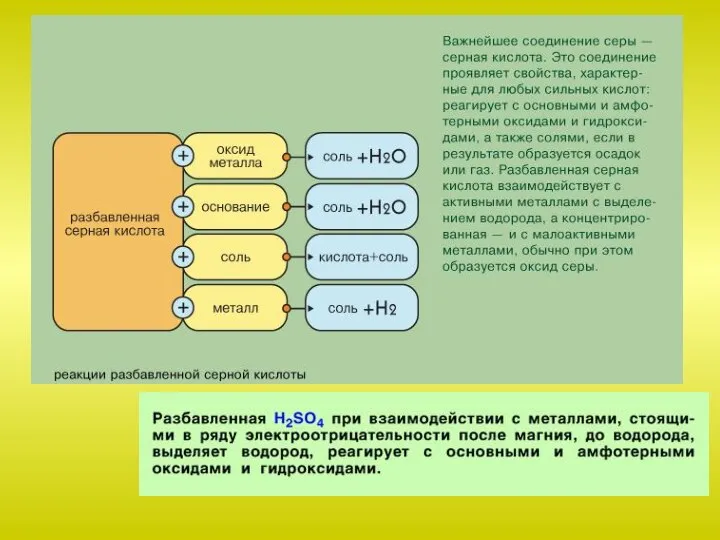
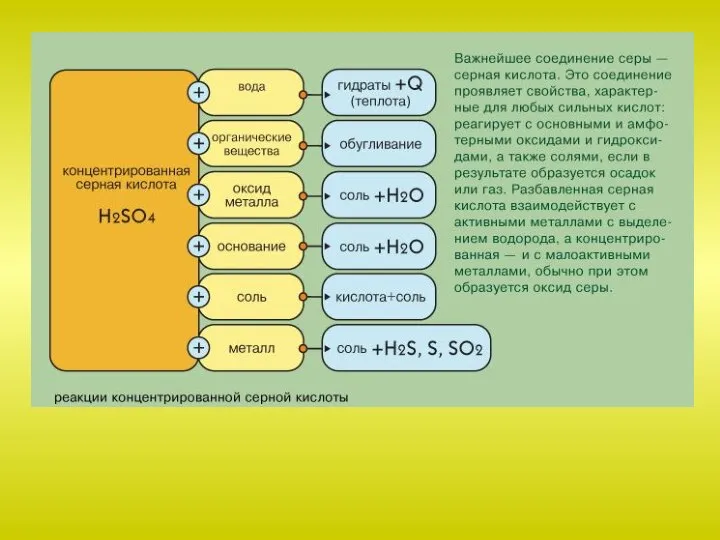
Слайд 37Как кислотный оксид взаимодействует с основными оксидами, основаниями, водой:



















































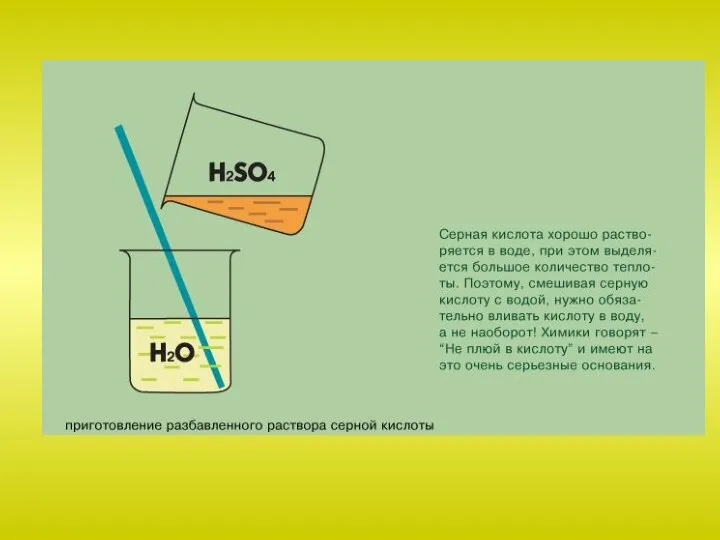

 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 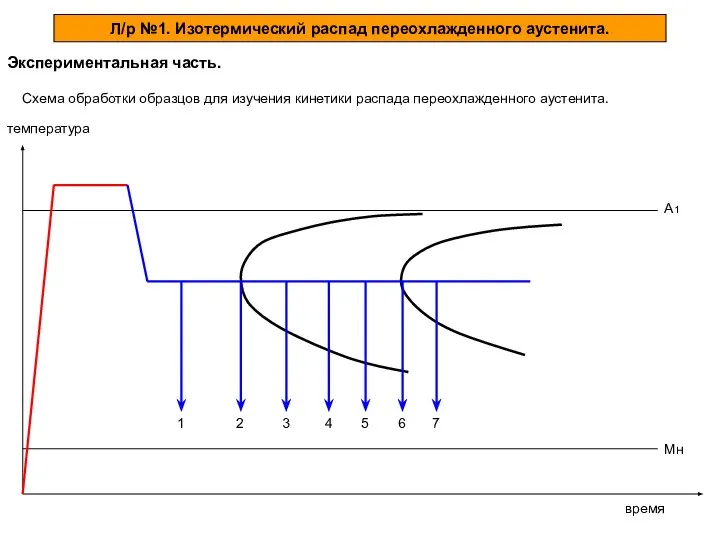 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций