Содержание
- 2. Химические явления – превращение одних веществ в другие Ржавление железа Скисание молока Гниение листьев Процесс фотосинтеза
- 3. Признаки химических реакций Выпадение осадка Выделение газа Появление запаха Выделение или поглощение теплоты Появление света Изменение
- 4. Реакция никеля с соляной кислотой Признак реакции – изменение цвета Сульфид натрия с соляной кислотой Признак
- 5. Йодид калия с нитратом свинца (II) Признак реакции – выпадение осадка Кусочек мела в соляной кислоте
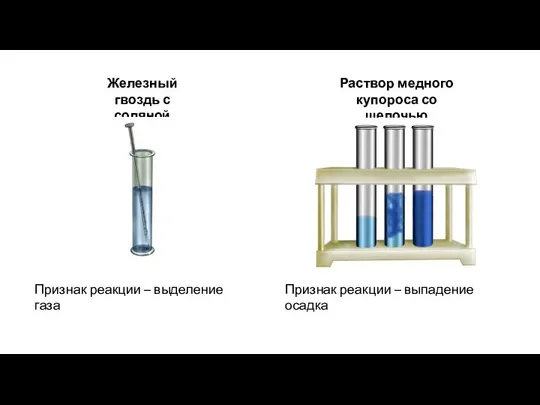
- 6. Железный гвоздь с соляной кислотой Признак реакции – выделение газа Раствор медного купороса со щелочью Признак
- 7. FeS Серого цвета Тонет в воде Не притягивается магнитом
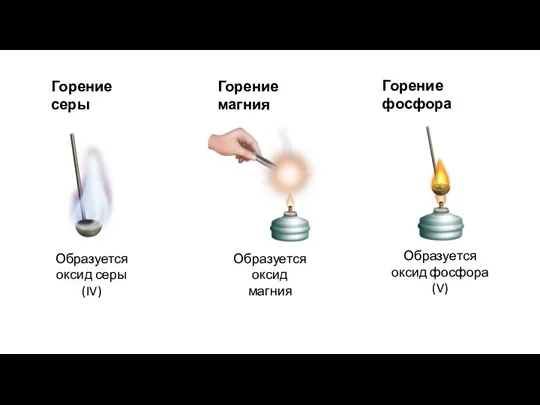
- 8. Горение серы Горение магния Горение фосфора Образуется оксид серы (IV) Образуется оксид магния Образуется оксид фосфора
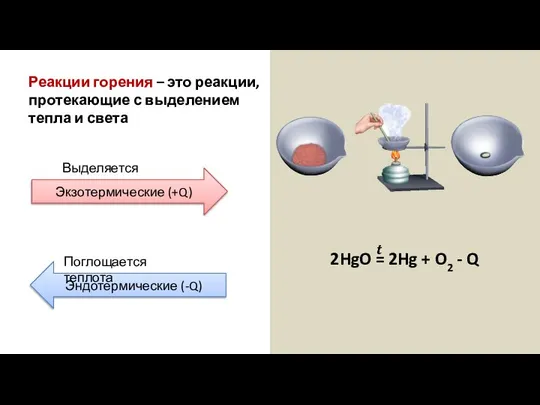
- 9. Реакции горения – это реакции, протекающие с выделением тепла и света Выделяется теплота Экзотермические (+Q) Эндотермические
- 10. Условия протекания химических реакций Соприкосновение реагирующих веществ Нагревание для определенных реакций Свет или электрический ток в
- 11. В 1748 году открыт ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ М.В. Ломоносов Атомы не разрушаются и не образуются,
- 12. Подтверждение закона сохранения массы веществ ЗНАЧЕНИЕ закона сохранения массы веществ Развитие химии как науки. На основании
- 13. Химическое уравнение – условная запись химической реакции с помощью химических формул и знаков А + Б
- 14. Молекулярное уравнение – это уравнение, в котором исходные вещества и продукты реакции записаны в виде молекул
- 15. ПРОВЕРКА Д/3 (из видео – прошлый урок!!!)
- 16. ПРОВЕРКА Д/3 (из видео – прошлый урок!!!)
- 18. Скачать презентацию












 Prezentatsia_Microsoft_PowerPoint
Prezentatsia_Microsoft_PowerPoint Карбоновые кислоты
Карбоновые кислоты Скорость химической реакции
Скорость химической реакции Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Стерилизация технологических потоков и оборудования
Стерилизация технологических потоков и оборудования Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Алканы
Алканы Основные классы неорганических соединений. Гидроксиды
Основные классы неорганических соединений. Гидроксиды Аспирин и его влияние на организм человека
Аспирин и его влияние на организм человека Алканы
Алканы Альдегиды. Строение молекул
Альдегиды. Строение молекул Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Алюминий
Алюминий Презентация на тему Экологические риски при добыче и переработке нефти
Презентация на тему Экологические риски при добыче и переработке нефти  Дополнительный_материал_09.14_19.10.2022_b0aaa559
Дополнительный_материал_09.14_19.10.2022_b0aaa559 98675992
98675992 Классификация спиртов. Изомерия спиртов
Классификация спиртов. Изомерия спиртов Ионные уравнения реакций
Ионные уравнения реакций Презентация на тему Вопросы от …
Презентация на тему Вопросы от …  Классификация и номенклатура аминов. 11 класс
Классификация и номенклатура аминов. 11 класс Презентация на тему Оксиды
Презентация на тему Оксиды  06_Типы_химических_реакций_в_органической_химии
06_Типы_химических_реакций_в_органической_химии Гибридизация АО. Пространственное строение молекул (геометрия молекул)
Гибридизация АО. Пространственное строение молекул (геометрия молекул) Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия
Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия Строение электронной оболочки атома часть 2
Строение электронной оболочки атома часть 2 Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Окислительновосстановительные процессы
Окислительновосстановительные процессы