Содержание
- 2. План Эпидемиология Пути проникновения. Нейроинвазия Нейровирулентность Рассеянный склероз. Определение Вирусная теория РС Механизмы действия Изменение иммунитета
- 3. Эпидемиология До 25% больных COVID-19 могут иметь симптомы поражения ЦНС Наиболее часто неврологическая симптоматика наблюдается при
- 4. Нейроинвазивность вируса SARS-CoV-2
- 5. Эндотелиальные клетки ГЭБ Они способны экспрессировать два типа рецепторов- ACE2 и CD209L, взаимодействуя с которыми SARS-CoV2
- 6. Обонятельные нервы Интраназальная инокуляция мышей MERS-CoV вызывает поражение головного мозга с вовлечением таламуса и ствола мозга.
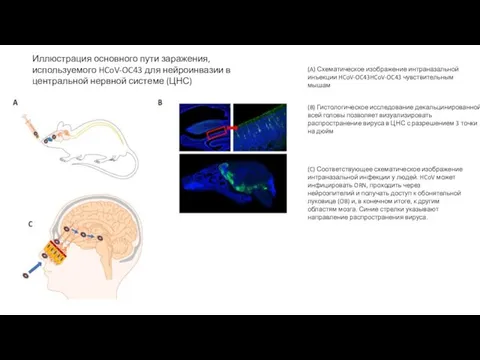
- 7. (A) Схематическое изображение интраназальной инъекции HCoV-OC43HCoV-OC43 чувствительным мышам (B) Гистологическое исследование декальцинированной всей головы позволяет визуализировать
- 8. Нейровирулентность вируса SARS-CoV-2
- 9. Цитокиновый шторм при различных вариантах COVID-19 ”Цитокиновый шторм”- воспалительная реакция в организме ,при которой уровень цитокинов
- 10. Механизм молекулярной мимикрии, при котором инфицированные вирусы имеют общие эпитопы, подобные некоторым компонентам периферических нервов, тем
- 11. Двойная экспрессия Т-клеточного рецептора Т-клетки способны экспрессировать более одного Т-клеточного рецептора, на некоторых клетках возможна экспрессия
- 12. При классическом варианте антигенного распознавания Т-хелпер активируется под влиянием взаимодействия Т-клеточного антигенраспознающего рецептора и пептида, который
- 13. . Активация аутореактивных Т-лимфоцитов. Доказано, что суперантигены могут непосредственно активировать аутореактивные Т-лимфоциты, которые затем мигрируют в
- 14. EBV сохраняется в В-клетках памяти при периферическом кровообращении: у здоровых серопозитивных людей они жестко регулируются иммунной
- 15. Особенности иммунного ответа при COVID-19 1 Отмечается снижение общего количества Т-лимфоцитов (CD4+, CD8+, NK-клеток). Наиболее низкие
- 16. COVID-19 и рассеянный склероз В моделях РС на животных были идентифицированы аутореактивные Т-лимфоциты, которые перекрестно реагируют
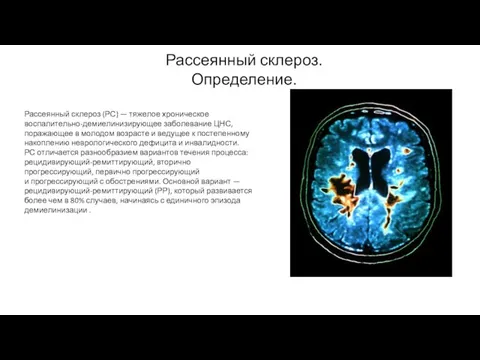
- 17. Рассеянный склероз. Определение. Рассеянный склероз (РС) — тяжелое хроническое воспалительно-демиелинизирующее заболевание ЦНС, поражающее в молодом возрасте
- 18. 04 Этиология рассеянного склероза до сих пор окончательно не установлена. На сегодняшний день наиболее распространённой теорией
- 19. Роль Th17 клеток в иммунном ответе Наше понимание роли Т-клеток в заболевании человека подвергается пересмотру в
- 20. Лечение Наибольшее беспокойство в связи с новой коронавирусной инфекцией при всех нейроиммунологических заболеваниях вызывают последствия иммунотерапии.
- 21. Интерфероны-b были первыми, кто получил одобрение для лечения РС и доступен в виде подкожных и внутримышечных
- 22. Клинический случай 1 случай пациента с COVID-19 с недавно диагностированными демиелинизирующими поражениями. История болезни Женщина 54
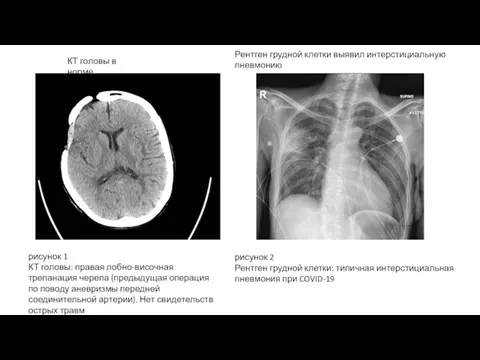
- 23. рисунок 1 КТ головы: правая лобно-височная трепанация черепа (предыдущая операция по поводу аневризмы передней соединительной артерии).
- 24. Пациентка была госпитализирована в нейрохирургическое отделение. общие анализы крови показали умеренную лимфоцитопению с незначительным повышением воспалительных
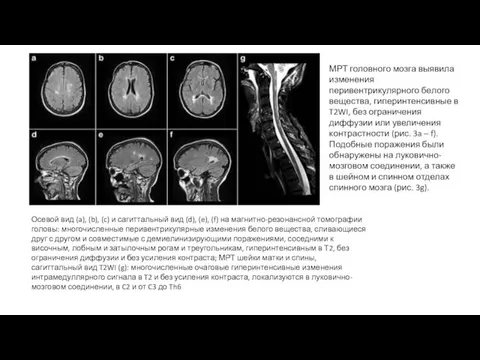
- 25. Осевой вид (a), (b), (c) и сагиттальный вид (d), (e), (f) на магнитно-резонансной томографии головы: многочисленные
- 26. Было проведено Лечение высокими дозами стероидов (дексаметазон 20 мг в день в течение 10 дней и
- 27. У пациентки были симптомы, соответствующие неврологическому поражению вследствие инфекции SARS-CoV-2. Аносмия и дисгевзия появились рано, а
- 29. Скачать презентацию





















 Антисептики, дезинфицирующие средства, антибиотики. Лекция 22
Антисептики, дезинфицирующие средства, антибиотики. Лекция 22 ГУЗ Липецкая ГБ № 4 Липецк-Мед
ГУЗ Липецкая ГБ № 4 Липецк-Мед Общие понятия о здоровье как основной ценности человека
Общие понятия о здоровье как основной ценности человека Классификация переломов
Классификация переломов Организация акушерско-гинекологической помощи в Республике Беларусь
Организация акушерско-гинекологической помощи в Республике Беларусь Ми – жұлын сұйықтығының құрамы мен диагностикалық маңызы
Ми – жұлын сұйықтығының құрамы мен диагностикалық маңызы Психопатологическая семиотика
Психопатологическая семиотика Гигиена зрения ребенка
Гигиена зрения ребенка Первичная артериальная гипертензия
Первичная артериальная гипертензия Гигиена ухода за животными. Санитарно-гигиеническое значение ухода за кожей
Гигиена ухода за животными. Санитарно-гигиеническое значение ухода за кожей Особенности лечебной тактики при экстрагенитальном эндометриозе
Особенности лечебной тактики при экстрагенитальном эндометриозе Острые респираторные заболевания и грипп
Острые респираторные заболевания и грипп Основы инфектологии
Основы инфектологии Противомикробные средства
Противомикробные средства Бронхиальды астма терапиясының фармакоэкономикасы
Бронхиальды астма терапиясының фармакоэкономикасы Нарушения речи, связанные с затруднениями в реализации моторной программы
Нарушения речи, связанные с затруднениями в реализации моторной программы Қарттар үйі
Қарттар үйі Сохранение здоровья ребенка до 1 года
Сохранение здоровья ребенка до 1 года Ресинхронизирующая терапия (устройства)
Ресинхронизирующая терапия (устройства) Тератомалар
Тератомалар Причины отклонений в развитии
Причины отклонений в развитии Гемопоэз и группы крови
Гемопоэз и группы крови Физиологические барьеры организма и их роль во врожденном иммунитете
Физиологические барьеры организма и их роль во врожденном иммунитете Aortic diseases
Aortic diseases Хронический насморк
Хронический насморк Здоровое питание
Здоровое питание Деменция - приобретённое слабоумие
Деменция - приобретённое слабоумие Нарушения сознания
Нарушения сознания