Содержание
- 2. ЦЕЛЬ: сформировать представление учащихся о кислороде, как химическом элементе и простом веществе. Задачи урока: - продолжить
- 3. Кислород. Оксиды. Горение. Общая характеристика. Химический знак – О Атомная масса Аr =16 Химическая формула О2
- 4. Нахождение в природе: Кислород – самый распространенный элемент в природе. В воздухе содержится – 20,9% В
- 5. История открытия Английский ученый Д. Пристли в 1774 году, изучая газы, проделал опыты с разложением оксида
- 6. Получение В лаборатории получают при реакции разложения сложных веществ: 2Н2 О ---- 2 Н2 + О2
- 7. Физические свойства Бесцветный газ, без вкуса, запаха, малорастворим в воде. При температуре -183 С –сжижается, а
- 8. Участвует в реакциях горения: С + О2 ----- С О 2 S + O2 ----- S
- 9. Оксиды Взаимодействие веществ с кислородом относится к реакциям окисления, образует оксиды. Оксиды – сложные вещества, которые
- 10. Применение кислорода В разных отраслях химической промышленности: Металлургии Сварка и резка металлов Ракетных двигателях Используется в
- 11. Обобщение урока
- 13. Скачать презентацию










 Вышивка. Образ птицы
Вышивка. Образ птицы Орфографическая диктовка
Орфографическая диктовка Для сх
Для сх Натюрморт
Натюрморт Права несовершеннолетних
Права несовершеннолетних СТОП вырубке ёлок!
СТОП вырубке ёлок! Русский мир
Русский мир Исследование развития речи детей старшего дошкольного возраста в игровой деятельности
Исследование развития речи детей старшего дошкольного возраста в игровой деятельности Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников
Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников Физиология мотивации
Физиология мотивации Маркетинговая стратегия
Маркетинговая стратегия СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ
СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ  Иконы православных праздников
Иконы православных праздников Олимпийские игры в Древней Греции
Олимпийские игры в Древней Греции Бумажная филигрань Бумагокручение Квиллинг
Бумажная филигрань Бумагокручение Квиллинг Бенчмаркинг, как инструмент управления организацией
Бенчмаркинг, как инструмент управления организацией Стандартизация. Общие положения стандартизации
Стандартизация. Общие положения стандартизации «Поспорили однажды корень, стебель, лист – кто из них важнее?»
«Поспорили однажды корень, стебель, лист – кто из них важнее?» В море коварном товаров и цен. Бизнес-корабль ведёт…
В море коварном товаров и цен. Бизнес-корабль ведёт… ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ.
ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ. Служу Отечеству
Служу Отечеству Продукты для «1С:Предприятия»
Продукты для «1С:Предприятия» Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu
Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu Урок -путешествие
Урок -путешествие Прогнозирование и анализ временных рядов
Прогнозирование и анализ временных рядов هدف از معامله کردن در بازار فارکس
هدف از معامله کردن در بازار فارکس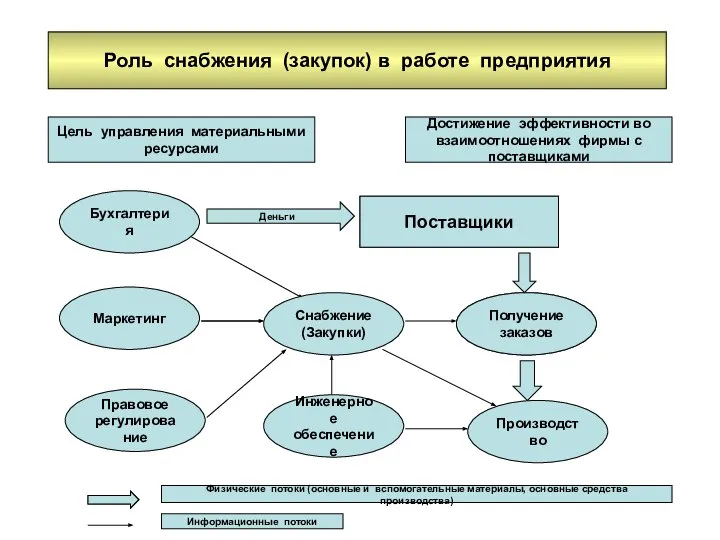 Роль снабжения, закупок в работе предприятия
Роль снабжения, закупок в работе предприятия Правописание о – е после шипящих и ц в окончаниях существительных 5 класс
Правописание о – е после шипящих и ц в окончаниях существительных 5 класс