Содержание
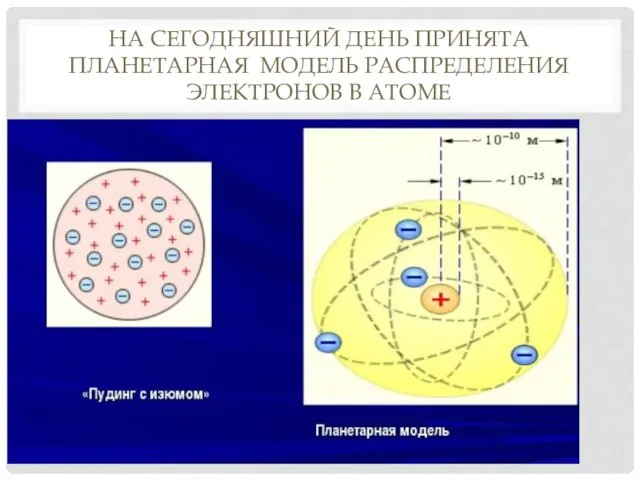
- 2. НА СЕГОДНЯШНИЙ ДЕНЬ ПРИНЯТА ПЛАНЕТАРНАЯ МОДЕЛЬ РАСПРЕДЕЛЕНИЯ ЭЛЕКТРОНОВ В АТОМЕ
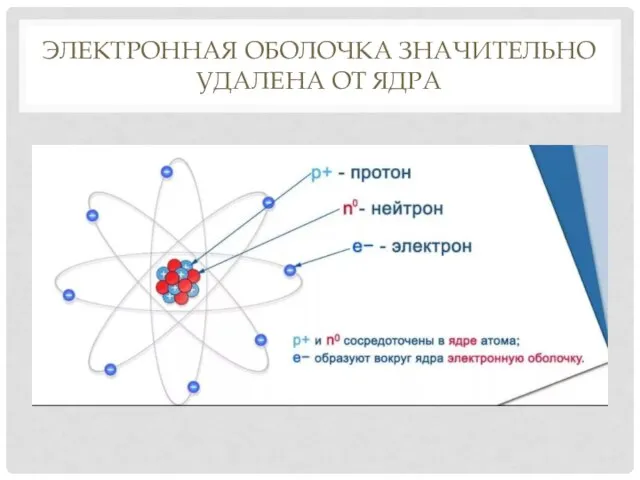
- 4. ЭЛЕКТРОННАЯ ОБОЛОЧКА ЗНАЧИТЕЛЬНО УДАЛЕНА ОТ ЯДРА
- 5. ЭЛЕКТРОНЫ В АТОМЕ ДВИЖУТСЯ НЕ ХАОТИЧНО, А РАСПРЕДЕЛЯЮТСЯ В ЭЛЕКТРОННОЙ ОБОЛОЧКЕ ПО УРОВНЯМ, СООТВЕТСТВЕННО СОБСТВЕННОЙ ЭНЕРГИИ
- 6. СУЩЕСТВУЕТ ТАКОЕ ПРАВИЛО: В АТОМЕ НЕ МОЖЕТ БЫТЬ ДВУХ ОДИНАКОВЫХ ЭЛЕКТРОНОВ, ПОЭТОМУ… На 1 электронном уровне
- 7. ПОЧЕМУ ТОЛЬКО 2 ЭЛЕКТРОНА? Они отличаются спинами ! Спин (не спина!) – это вращение вокруг своей
- 8. 1 ПЕРИОД ПОКАЗЫВАЕТ, ЧТО АТОМЫ ИМЕЮТ 1 ЭЛЕКТРОННЫЙ УРОВЕНЬ, И ЗДЕСЬ РАЗМЕЩАЮТСЯ ТОЛЬКО ДВА ЭЛЕМЕНТА: ВОДОРОД
- 9. ПОТОМУ ЧТО У НИХ РАЗНЫЕ СПИНЫ, Т.Е. РАЗНЫЕ ВЕКТОРА ДВИЖЕНИЯ Второй период начинается с лития, у
- 10. ВТОРОЙ ПЕРИОД СЛЕДУЮЩИЙ ЭЛЕМЕНТ БЕРИЛЛИЙ, У НЕГО 4 ЭЛЕКТРОНА: 2 НА 1 УРОВНЕ, 2 - НА
- 11. СКОЛЬКО ЭЛЕКТРОНОВ МОЖЕТ ПОМЕСТИТЬСЯ НА ВТОРОМ УРОВНЕ? Чтобы рассчитать количество электронов, которое помещается на любом уровне,
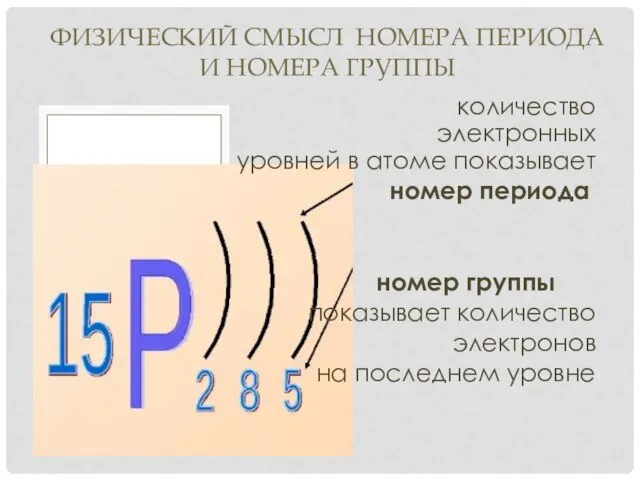
- 12. количество электронных уровней в атоме показывает номер периода номер группы показывает количество электронов на последнем уровне
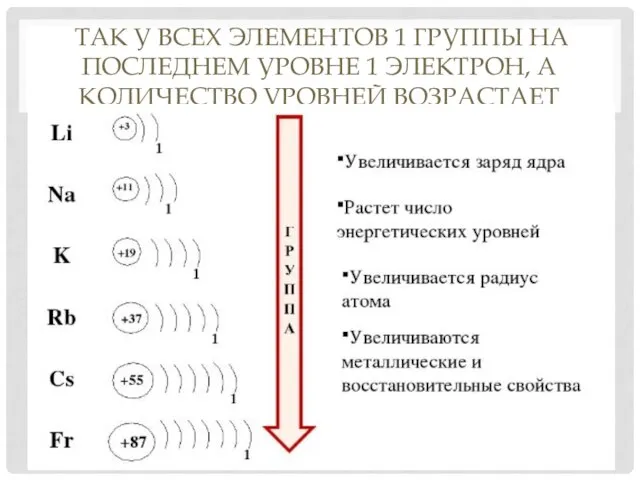
- 13. ТАК У ВСЕХ ЭЛЕМЕНТОВ 1 ГРУППЫ НА ПОСЛЕДНЕМ УРОВНЕ 1 ЭЛЕКТРОН, А КОЛИЧЕСТВО УРОВНЕЙ ВОЗРАСТАЕТ
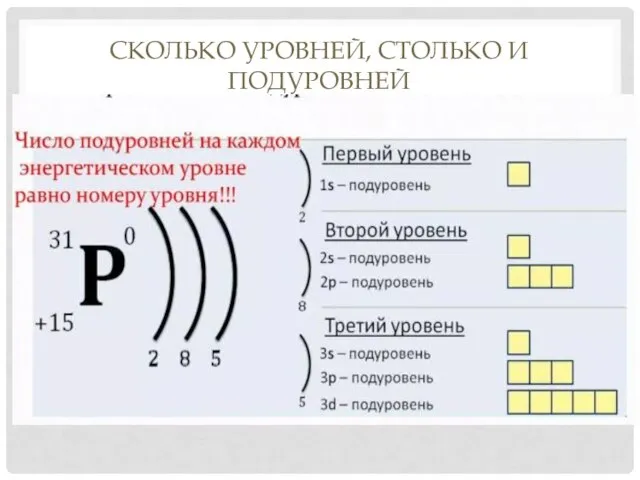
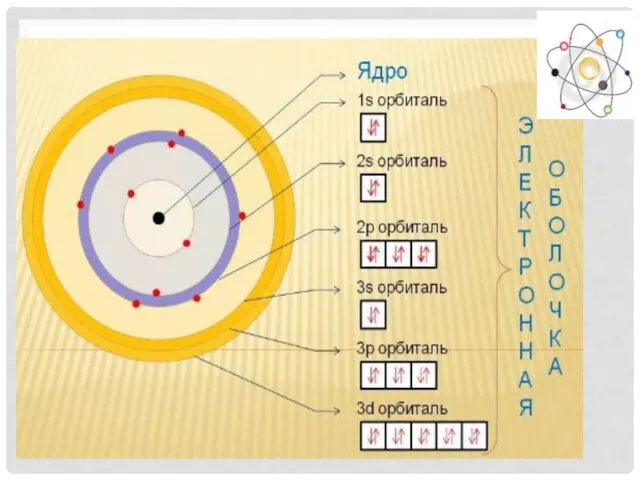
- 14. УРОВНИ И ПОДУРОВНИ Поскольку на одной орбитали могут разместиться только 2 электрона, то каждый уровень может
- 15. СКОЛЬКО УРОВНЕЙ, СТОЛЬКО И ПОДУРОВНЕЙ
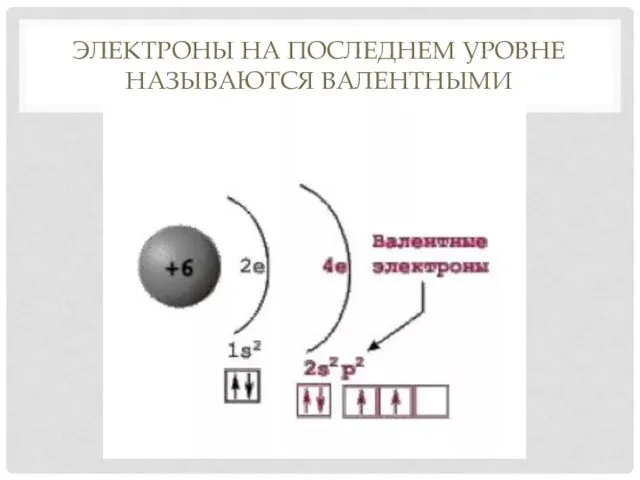
- 17. ЭЛЕКТРОНЫ НА ПОСЛЕДНЕМ УРОВНЕ НАЗЫВАЮТСЯ ВАЛЕНТНЫМИ
- 18. ЗАПОМНИ!
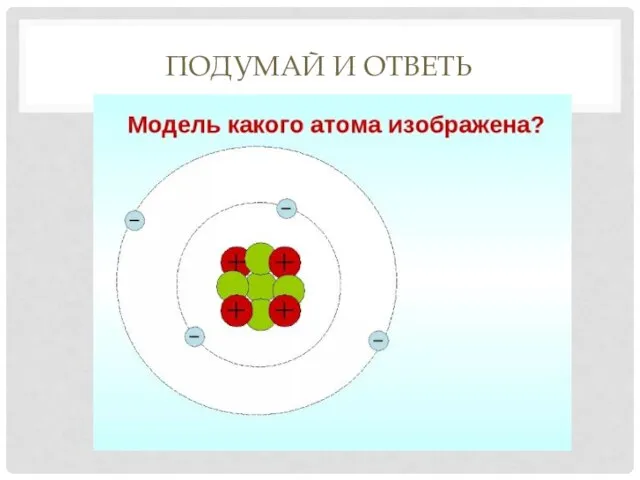
- 19. ПОДУМАЙ И ОТВЕТЬ
- 21. Скачать презентацию










 Центр образования,исследований и разработок «ИНО Томск’2020»
Центр образования,исследований и разработок «ИНО Томск’2020» London's architectural ensembles of the XI-XX centuries as the fixed music
London's architectural ensembles of the XI-XX centuries as the fixed music На зарядку становись!
На зарядку становись! Планы на счастье. Ведущая тренинга
Планы на счастье. Ведущая тренинга Культура и быт народов Северного Кавказа
Культура и быт народов Северного Кавказа Как слово наше отзовется
Как слово наше отзовется ПРИРОДНЫЕ ГЕПАТОПРОТЕКТОРЫ
ПРИРОДНЫЕ ГЕПАТОПРОТЕКТОРЫ g?c суперфрукт Содержит липокаротины tm
g?c суперфрукт Содержит липокаротины tm Стекло
Стекло Историческое культурное наследие Белгородской области в 19 веке
Историческое культурное наследие Белгородской области в 19 веке Презентация на тему Строение электронных оболочек атомов
Презентация на тему Строение электронных оболочек атомов Этнокультурные особенности Германии
Этнокультурные особенности Германии Викторина. Году театра посвящается. Г. Сыктывкар
Викторина. Году театра посвящается. Г. Сыктывкар ВЕГЕТАТИВНЫЕ ОРГАНЫ РАСТЕНИЙ
ВЕГЕТАТИВНЫЕ ОРГАНЫ РАСТЕНИЙ Проверка домашнего задания
Проверка домашнего задания Межрегиональный фестиваль чувашской эстрадной песни Виръял Шевлисем, 25 летие
Межрегиональный фестиваль чувашской эстрадной песни Виръял Шевлисем, 25 летие A day in London
A day in London Приоритетный национальный проект «Образование» в нашей школе
Приоритетный национальный проект «Образование» в нашей школе ИНФОРМАЦИОННО-ТЕХНИЧЕСКОЕ УСТРОЙСТВО – СИСТЕМА МОВС-1-АФИ ГНУ АФИ РОССЕЛЬХОЗАКАДЕМИИ Система МОВС-1-АФИ – малогабаритная оптимиз
ИНФОРМАЦИОННО-ТЕХНИЧЕСКОЕ УСТРОЙСТВО – СИСТЕМА МОВС-1-АФИ ГНУ АФИ РОССЕЛЬХОЗАКАДЕМИИ Система МОВС-1-АФИ – малогабаритная оптимиз Використання МОБІЛЬНИХ ЗАСТОСУНКІВ ДЛЯ РЕЄСТРАЦІЇ ПОКАЗНИКІВ ФІЗИЧНОГО СТАНУ Кардаш
Використання МОБІЛЬНИХ ЗАСТОСУНКІВ ДЛЯ РЕЄСТРАЦІЇ ПОКАЗНИКІВ ФІЗИЧНОГО СТАНУ Кардаш Умножение и деление чисел (2 класс)
Умножение и деление чисел (2 класс) Курс семинаров. Интернет-маркетинг. Старт
Курс семинаров. Интернет-маркетинг. Старт Всемирный фестиваль молодёжи и студентов 2017
Всемирный фестиваль молодёжи и студентов 2017 пороки разв уха детей
пороки разв уха детей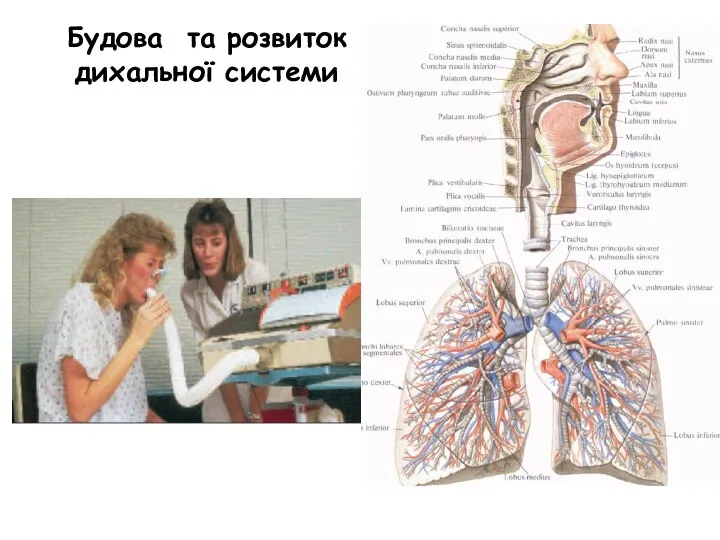 № 1-2-2 Будова та розвиток дихальної системи
№ 1-2-2 Будова та розвиток дихальної системи Общаться с ребенком. Как?
Общаться с ребенком. Как? Трансформация природной формы в дизайн-форму
Трансформация природной формы в дизайн-форму Моё хобби - ГЕОГРАФИЯ
Моё хобби - ГЕОГРАФИЯ