Содержание
- 2. Атомдағы электрондар қозғалысы
- 3. Сабақтың мақсаты атомдық орбиталь, электрондық бұлт, энергетикалық деңгей, энергетикалық деңгейше ұғымдарын білу; алғашқы 36 элементтің электрондық
- 4. Бағалау критерийлері: Атомдық орбитальды және энергетикалық деңгейлерді, деңгейшелерді біледі; алғашқы 36 элементтің электрондық және графикалық формуласын
- 5. Атом құрылысы Атом дегеніміз - химиялық жолмен бөлінбейтін затттың ең ұсақ бөлшек. Атом бүтіндей алғанда зарядсыз,
- 6. Электрондар ядроның төңірегінде белгілі бір заңдылықтармен орналасады. Атомның ядро заряды қанша болса, ондағы электрондар саны да
- 7. Энергетикалық деңгейшелер - энергия мәндері бірдей электрондардан түзілген орбитальдар, деңгейшелері Атомдық орбитал (АО) ұғымы электрондарың атомда
- 8. Slides.kz 11Na 1s22s22р63s1; 12Mg 1s22s22р63s2; 13Al 1s22s22р63s23p1;
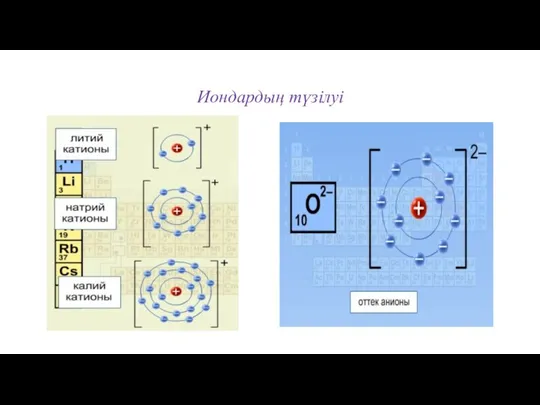
- 10. Катион (+) – оң зарядталған ион (электронды береді) Анион (-) – теріс зарядталған ион (электронды қабылдайды)
- 11. «Октет» ережесі 11Na ( натрий металы: 1s2 2s2 2p6 3s1) - e- = 11Na+ ( натрий
- 12. Иондардың түзілуі
- 13. Қалыптастырушы бағалау тапсырмалары Тапсырма №1 Кестеде көрсетілген элементтер тұрақты күйге жету үшін қанша электрон қосып алуы
- 14. Дескриптор: Элементтер тұрақты күйге жету үшін қанша электрон қосып алуы керек немесе беріп жіберуі керек екенін
- 15. Тапсырма №2 Төменде берілген иондар мен атомдарының электрондық конфигурациясын жаз Дескриптор: Берілген иондар мен атомдарының электрондық
- 16. Тапсырма №3
- 18. Үй тапсырмасы Алғашқы 36 химиялық элементтің атомдарының электрондық және графикалық формуласын құру
- 20. Скачать презентацию
















 Взаимосвязь метапредметных и предметных результатов обучения в начальной школе
Взаимосвязь метапредметных и предметных результатов обучения в начальной школе Эталонная модель RM OSI: данные, функции
Эталонная модель RM OSI: данные, функции Ecological and economic problems of management of lan resourses
Ecological and economic problems of management of lan resourses  Николай Рубцов
Николай Рубцов Презентация на тему Адресация в сети интернет
Презентация на тему Адресация в сети интернет ДЕТСТВО, ОПАЛЕННОЕ ВОЙНОЙ
ДЕТСТВО, ОПАЛЕННОЕ ВОЙНОЙ Презентация на тему Состав, структура и соотношения цен
Презентация на тему Состав, структура и соотношения цен  урок 31 Степенные функции их свойства и графики
урок 31 Степенные функции их свойства и графики Маньяки… кто есть кто
Маньяки… кто есть кто Бенчмаркинг. Производство фанеры за январь-май 2018 года
Бенчмаркинг. Производство фанеры за январь-май 2018 года Внеклассное мероприятие День птиц «Птичьи трели»
Внеклассное мероприятие День птиц «Птичьи трели» Петербургский метрополитен. История, факты, схема
Петербургский метрополитен. История, факты, схема Накануне 50-летия нашего города я решил найти фотографии его строительства. Зачастую местность так меняется, что, сопоставив две фо
Накануне 50-летия нашего города я решил найти фотографии его строительства. Зачастую местность так меняется, что, сопоставив две фо Жизнь животных зимой
Жизнь животных зимой Система бухгалтерской отчетности
Система бухгалтерской отчетности Метод скользящего контроля для оценки качества рекомендательных интернет-сервисов
Метод скользящего контроля для оценки качества рекомендательных интернет-сервисов Выбор компании разработчика
Выбор компании разработчика N_F_Andreychenko_Osvoenie_intellektualnykh_funktsiy
N_F_Andreychenko_Osvoenie_intellektualnykh_funktsiy Должностная инструкция учителя
Должностная инструкция учителя ЭКОНОМИКА ЗДРАВООХРАНЕНИЯ
ЭКОНОМИКА ЗДРАВООХРАНЕНИЯ  Что такое налоги зачем их платить? Кружок Основы финансовой грамотности 8, 9 класс
Что такое налоги зачем их платить? Кружок Основы финансовой грамотности 8, 9 класс Презентация на тему строение клетки
Презентация на тему строение клетки Компьютеры фирмы Apple
Компьютеры фирмы Apple Особенности социально-экономического развития ведущих стран глобальной экономики в 1870-1913
Особенности социально-экономического развития ведущих стран глобальной экономики в 1870-1913 Слово в общенациональном и юридическом языке. Соломоново решение. Над презентацией
Слово в общенациональном и юридическом языке. Соломоново решение. Над презентацией  Бизнес-план ОООCerberus
Бизнес-план ОООCerberus Презентация на тему Прошедшее время глагола в русском языке
Презентация на тему Прошедшее время глагола в русском языке  Дифференциальная диагностика и лечение поражений ЦНС у больных ВИЧ-инфекцией
Дифференциальная диагностика и лечение поражений ЦНС у больных ВИЧ-инфекцией