Содержание
- 2. Алканы - углеводороды, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода.
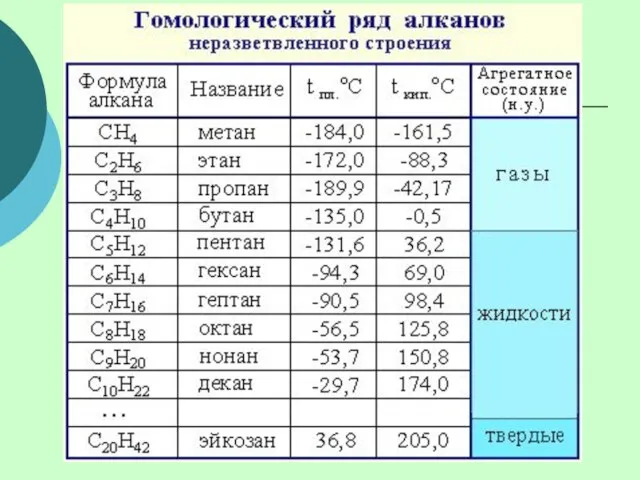
- 3. Гомологический ряд алканов CH4 или Н-СН2-Н – первый член гомологического ряда – метан (содержит 1 атом
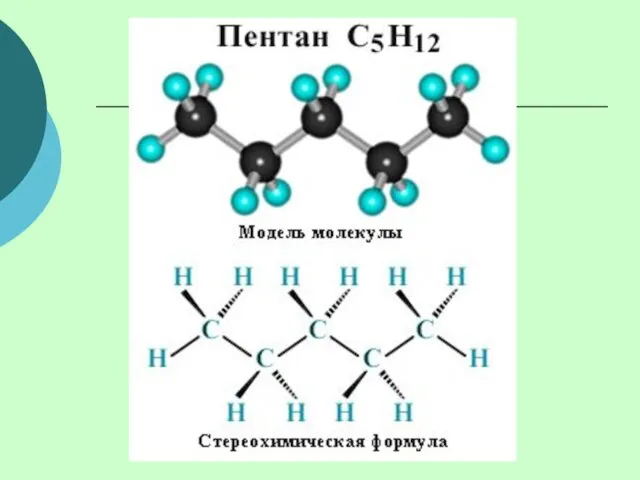
- 5. Простейшие представители алканов
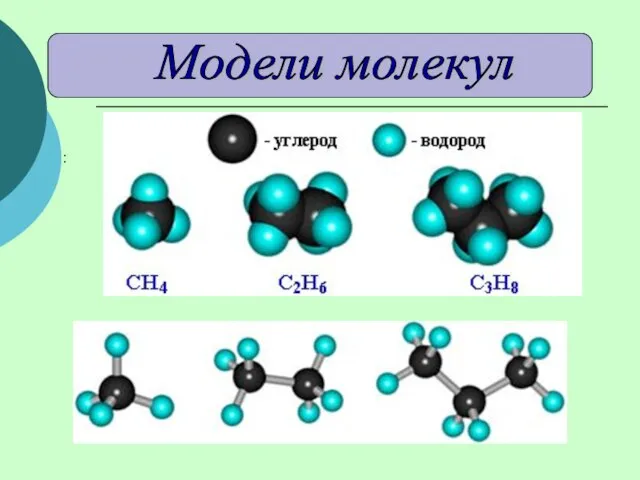
- 6. : Модели молекул
- 7. Строение алканов Химическое строение Электронное строение Пространственное строение
- 8. Химическое строение (порядок соединения атомов в молекулах) простейших алканов – метана, этана и пропана – показывают
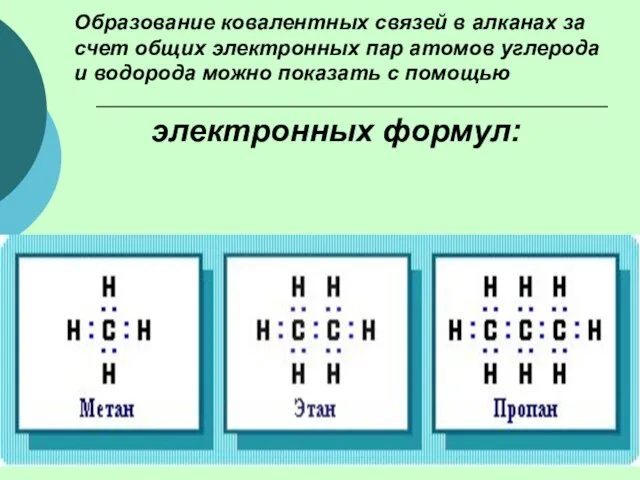
- 9. Образование ковалентных связей в алканах за счет общих электронных пар атомов углерода и водорода можно показать
- 10. Пространственное строение, т.е. взаимное расположение атомов молекулы в пространстве, зависит от направленности атомных орбиталей (АО) этих
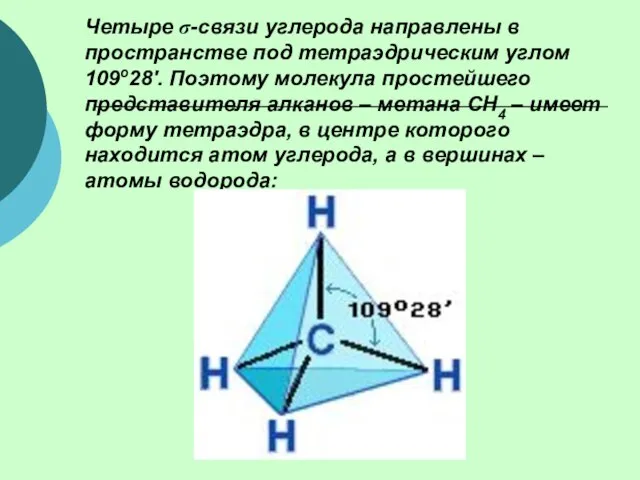
- 11. Четыре σ-связи углерода направлены в пространстве под тетраэдрическим углом 109о28'. Поэтому молекула простейшего представителя алканов –
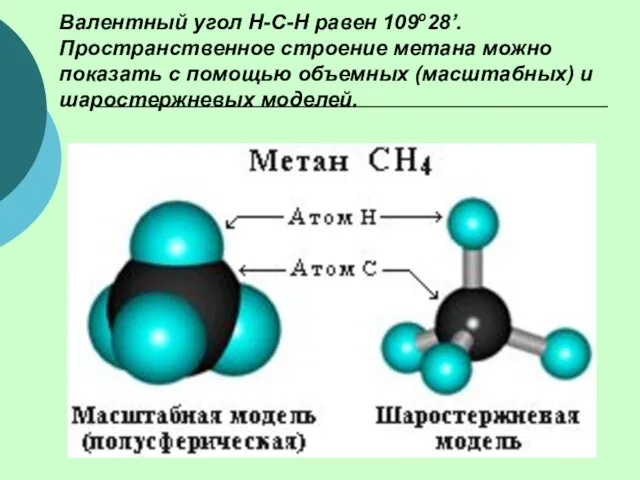
- 12. Валентный угол Н-С-Н равен 109о28’. Пространственное строение метана можно показать с помощью объемных (масштабных) и шаростержневых
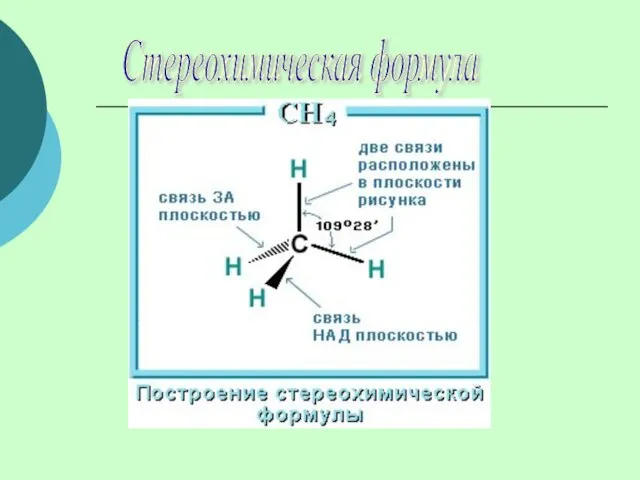
- 13. Стереохимическая формула
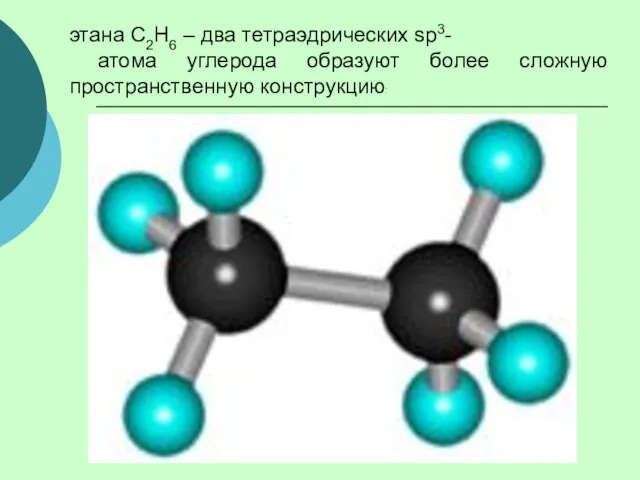
- 14. этана С2Н6 – два тетраэдрических sp3- атома углерода образуют более сложную пространственную конструкцию:
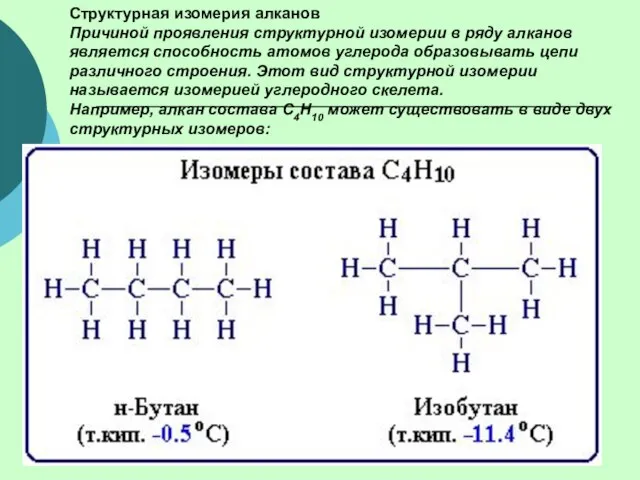
- 16. Структурная изомерия алканов Причиной проявления структурной изомерии в ряду алканов является способность атомов углерода образовывать цепи
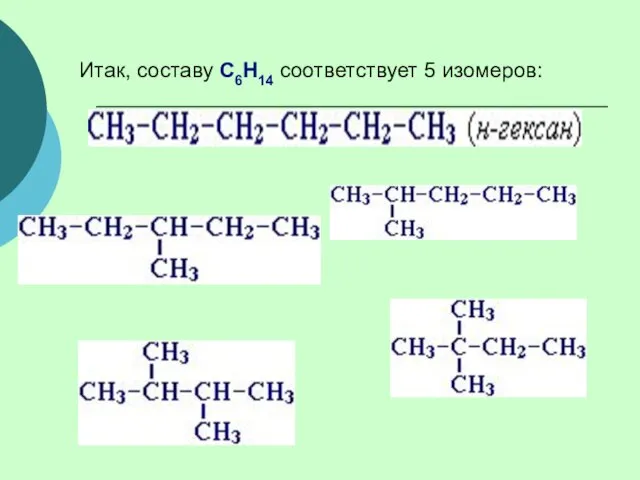
- 17. Итак, составу С6Н14 соответствует 5 изомеров:
- 19. Скачать презентацию





 Псевдо-конфликт. Факт-конфликт. Эго-конфликт
Псевдо-конфликт. Факт-конфликт. Эго-конфликт Превращение веществ. История химии
Превращение веществ. История химии Святой Николай
Святой Николай Как стать режиссером своей жизни и создать сюжет счастливого будущего за 12 дней?
Как стать режиссером своей жизни и создать сюжет счастливого будущего за 12 дней? Дифференциация К-Г
Дифференциация К-Г Теории детского развития
Теории детского развития Оптимизированное решение для малого бизнеса
Оптимизированное решение для малого бизнеса Северская АЭС
Северская АЭС Викторина
Викторина Правила поведения на экскурсии
Правила поведения на экскурсии Нам не дано предугадать как слово наше отзовется. Для для 9-11 классов
Нам не дано предугадать как слово наше отзовется. Для для 9-11 классов Применение международных протоколов обследования и лечения при ведении пациентов с синдромом Веста.
Применение международных протоколов обследования и лечения при ведении пациентов с синдромом Веста. Uroven_6_Zanyatie_3_1
Uroven_6_Zanyatie_3_1 Политическая система и ее роль в жизни общества
Политическая система и ее роль в жизни общества Abbigliamento
Abbigliamento Овощной калейдоскоп
Овощной калейдоскоп Великий князь Александр Невский
Великий князь Александр Невский Образ красоты русского человека (женский образ). Красота – тоже оберег
Образ красоты русского человека (женский образ). Красота – тоже оберег Валентинов День
Валентинов День Презентация для защиты
Презентация для защиты Символизм в европейском искусстве
Символизм в европейском искусстве Заключительный этап проекта
Заключительный этап проекта Конструирование в дизайне среды. Малоэтажные здания
Конструирование в дизайне среды. Малоэтажные здания Объяснение электрических явлений
Объяснение электрических явлений КонференцииСеминары Встречи
КонференцииСеминары Встречи Презентация на тему Современные воспитательные технологии
Презентация на тему Современные воспитательные технологии Тригонометрия
Тригонометрия Компетенции по предмету Информатика Информационно – коммуникативно – технологическая компетентность (ИКТ). ИКТ состоит из: инфо
Компетенции по предмету Информатика Информационно – коммуникативно – технологическая компетентность (ИКТ). ИКТ состоит из: инфо