Содержание
- 2. Содержание Алкены Номенклатура Изомерия Физические свойства Строение алкенов Химические свойства (Химические свойства (реакции присоединения: галогенирование, Химические
- 3. Алкены Алкенами или олефинами, или этиленовыми углеводородами называются углеводороды, содержащие в молекуле одну двойную связь и
- 4. Номенклатура Название алкенов по систематической номенклатуре образуют из названий аналогично построенных алканов, заменяя суффиксы –ан на
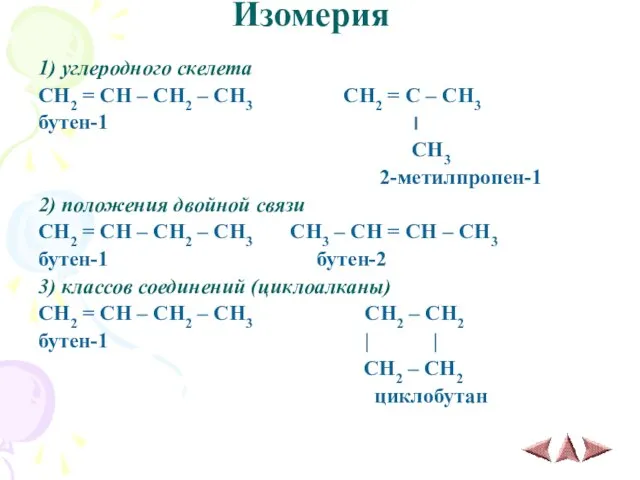
- 5. Изомерия 1) углеродного скелета CH2 = CH – CH2 – CH3 CH2 = C – CH3
- 6. 4) пространственная CH3 H H H \ / \ / C = C C = C
- 7. Физические свойства По физическим свойствам этиленовые углеводороды близки к алканам. При нормальных условиях углеводороды C2–C4 –
- 8. Строение алкенов Углеродные атомы в молекуле этилена находятся в состоянии sp2-гибридизации, т.е. в гибридизации участвуют одна
- 9. Каждая оставшаяся гибридная орбиталь атомов углерода перекрывается с s- орбиталью атомов водорода, приводя к образованию в
- 10. Длина связи λ – расстояние между центрами ядер связанных друг с другом атомов (нм). Энергия связи
- 11. σ-связь – плотность электронного облака максимальна вдоль оси, соединяющей ядра атомов. π–связь – плотность электронного облака
- 12. π- Связь менее прочна, чем σ- связь, так как p- орбитали с параллельными осями перекрываются значительно
- 13. Химические свойства Для алкенов наиболее типичными являются реакции присоединения. 1) Галогенирование. Алкены при обычных условиях присоединяют
- 14. 2) Гидрирование. Легко присоединяют водород в присутствии катализаторов (Pt, Pd, Ni) образуя предельные углеводороды. CH3–CH=CH2 +
- 15. Присоединение галогеноводородов к пропилену и другим несимметричным алкенам происходит в соответствии с правилом В.В.Марковникова (водород присоединяется
- 16. 4) Гидратация. В присутствии минеральных кислот олефины присоединяют воду, образуя спирты. H+ CH3−C=CH2 + H2O →
- 17. Окисление Алкены легко окисляются. В зависимости от условий проведения реакции образуются различные продукты. 1) При сжигании
- 18. 3) При окислении алкенов разбавленным раствором перманганата калия образуются двухатомные спирты – гликоли (реакция Е.Е.Вагнера). Реакция
- 19. Реакция полимеризации. Реакцией полимеризации называется процесс образования высокомолекулярного соединения (полимера) путем соединения друг с другом молекул
- 20. Получение 1) Дегидрогенизация алканов при повышенной температуре с катализатором. CH3–CH2–CH2–CH3 ––300°C,Cr2O3 → CH2=CH–CH2–CH3(бутен-1) + H2 CH3–CH2–CH2–CH3
- 21. Порядок дегидратации вторичных и третичных спиртов определяется правилом А.М.Зайцева: при образовании воды атом водорода отщепляется от
- 22. 4) Реакция дегалогенирования (отщепление двух атомов галогена от соседних атомов углерода) при нагревании дигалогенидов с активными
- 23. Применение Алкены широко используются в промышленности в качестве исходных веществ для получения растворителей (спирты, дихлорэтан, эфиры
- 24. Литература 1. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. Учебник для вузов./ Под ред. Петрова
- 26. Скачать презентацию






















 Поисковое движение России в Московской области
Поисковое движение России в Московской области ВЕЛИКАЯ ФРАНЦУЗСКАЯ РЕВОЛЮЦИЯ (1789-1794)
ВЕЛИКАЯ ФРАНЦУЗСКАЯ РЕВОЛЮЦИЯ (1789-1794) Силикатная промышленность как отрасль производства
Силикатная промышленность как отрасль производства квн НА ТЕМУ " Вредные привычки "
квн НА ТЕМУ " Вредные привычки " Презентация на тему Математика. Единицы площади
Презентация на тему Математика. Единицы площади Дополнительное описание к Дилерской Политике
Дополнительное описание к Дилерской Политике Богомол
Богомол Радіо
Радіо  Трофическая структура биогеоценоза
Трофическая структура биогеоценоза Презентация на тему 12 подвигов Геракла
Презентация на тему 12 подвигов Геракла  Охрана животных 3 класс
Охрана животных 3 класс Уральский экономический район
Уральский экономический район Пантограф (Лифт для одежды)
Пантограф (Лифт для одежды) ПЕРСПЕКТИВЫ ПРИМЕНЕНИЯ В ЗДРАВООХРАНЕНИИСТРАТЕГИИ CALSВ. Н. Теплинский
ПЕРСПЕКТИВЫ ПРИМЕНЕНИЯ В ЗДРАВООХРАНЕНИИСТРАТЕГИИ CALSВ. Н. Теплинский Публикации международного уровня: практические рекомендации
Публикации международного уровня: практические рекомендации Жанр фэнтези
Жанр фэнтези Упрочнение оснований фундаментов
Упрочнение оснований фундаментов Государственная образовательная политика РФ
Государственная образовательная политика РФ CNews Analytics«Рынок ЦОВ: новости и тенденции»
CNews Analytics«Рынок ЦОВ: новости и тенденции» 1911_Ðенинги_ÐонÑпекÑ
1911_Ðенинги_ÐонÑпекÑ Вырасти дерево
Вырасти дерево Требования к оформлению проектной комнаты Обеи
Требования к оформлению проектной комнаты Обеи Культура движения
Культура движения Стратегия деятельности школы
Стратегия деятельности школы Презентация на тему История и методология юридической науки
Презентация на тему История и методология юридической науки Инфракрасные пейзажи
Инфракрасные пейзажи ИХН
ИХН Стратегия развития сети Академкнига
Стратегия развития сети Академкнига