Содержание
- 2. Алкены (этиленовые углеводороды, олефины) – непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда
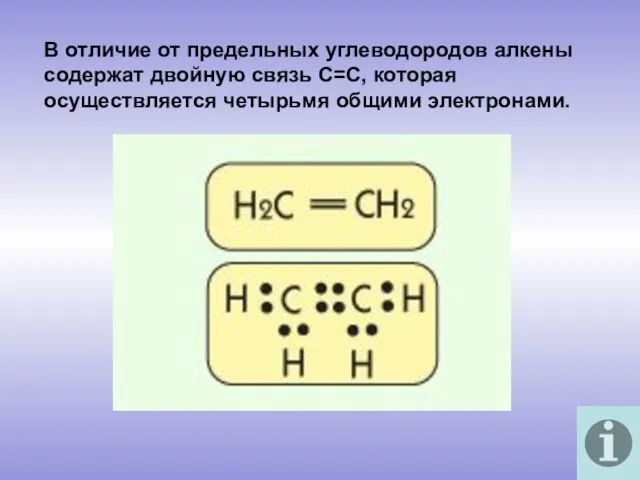
- 3. В отличие от предельных углеводородов алкены содержат двойную связь С=С, которая осуществляется четырьмя общими электронами.
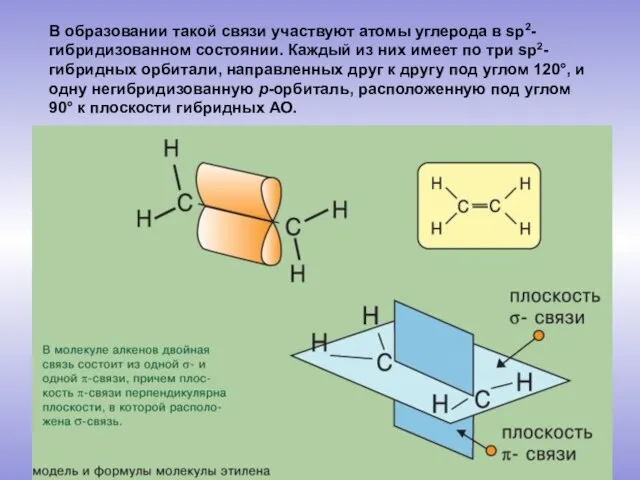
- 4. В образовании такой связи участвуют атомы углерода в sp2-гибридизованном состоянии. Каждый из них имеет по три
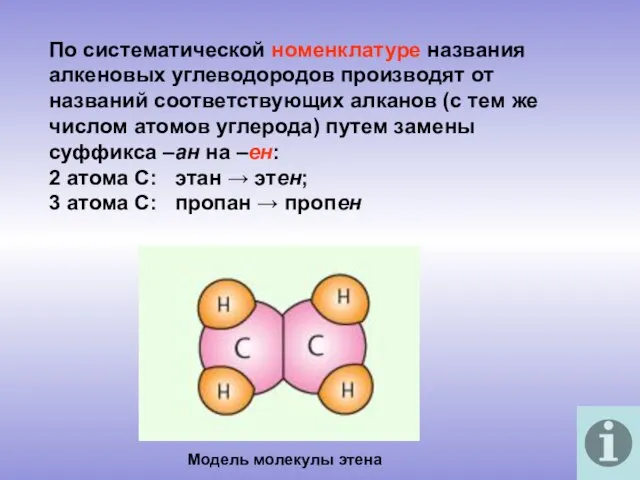
- 5. По систематической номенклатуре названия алкеновых углеводородов производят от названий соответствующих алканов (с тем же числом атомов
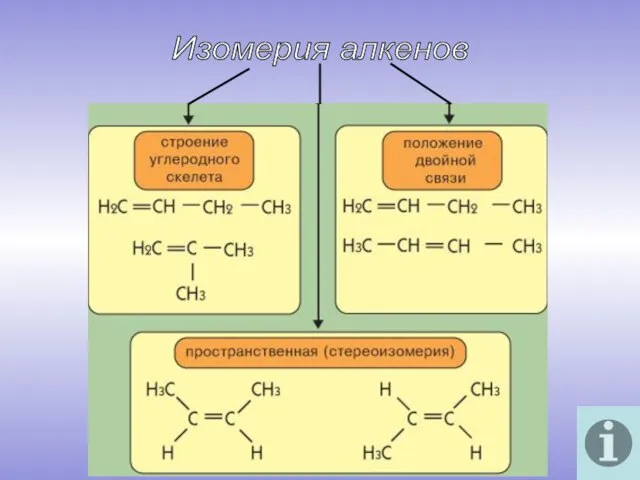
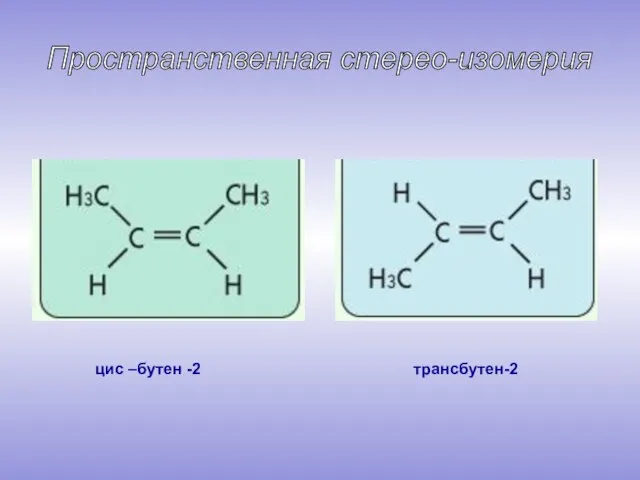
- 6. Изомерия алкенов
- 7. цис –бутен -2 трансбутен-2 Пространственная стерео-изомерия
- 8. Физические свойства алкенов закономерно изменяются в гомологическом ряду: от С2Н4 до С4Н8 – газы, начиная с
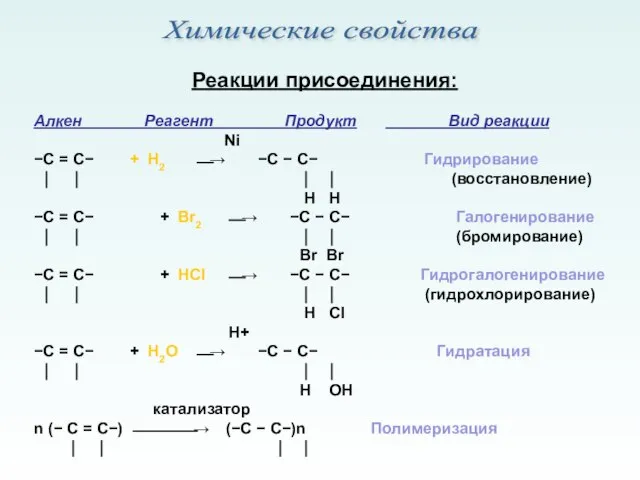
- 9. Реакции присоединения: Алкен Реагент Продукт Вид реакции Ni −С = С− + Н2 ⎯→ −С −
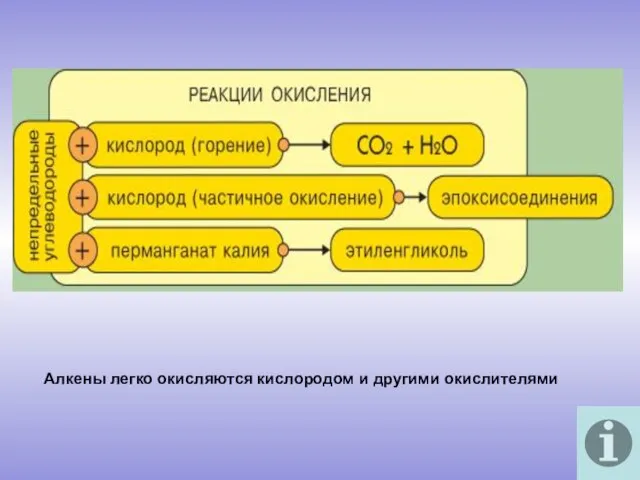
- 10. Алкены легко окисляются кислородом и другими окислителями
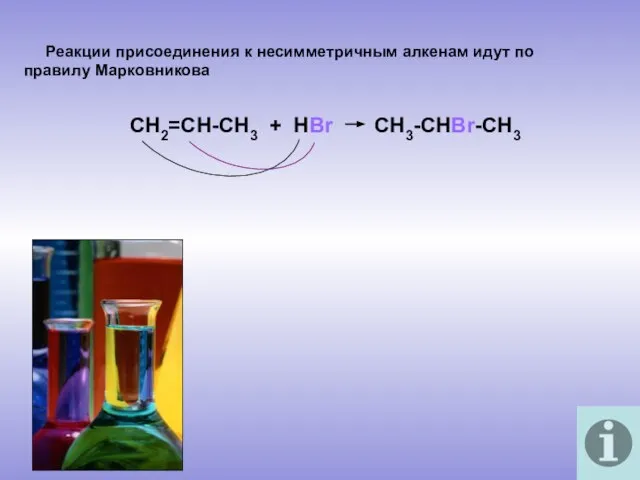
- 11. Реакции присоединения к несимметричным алкенам идут по правилу Марковникова СН2=СН-СН3 + НВr CH3-CHBr-CH3
- 12. Важнейшей реакцией непредельных углеводородов является реакция полимеризации –соединение молекул углеводородов друг с другом с образованием длинных
- 13. Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al2O3). Изомеризация алкенов приводит или к
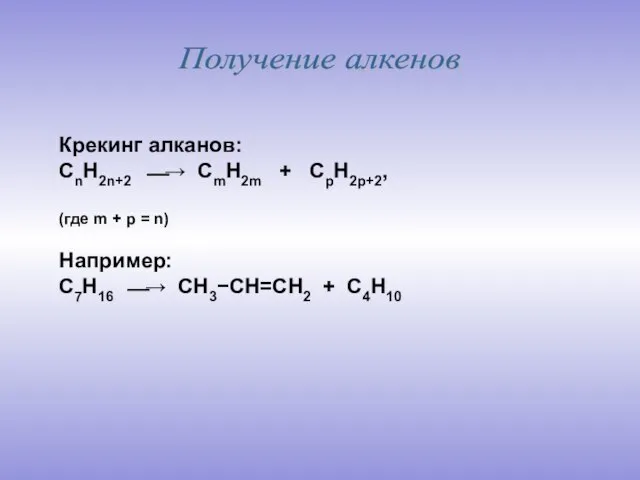
- 14. Получение алкенов Крекинг алканов: CnH2n+2 ⎯→ CmH2m + CpH2p+2, (где m + p = n) Например:
- 15. Получение алкенов Дегидратация спиртов (лабораторный способ) при t > 150 °C в присутствии водоотнимающих реагентов H2SO4
- 16. Получение алкенов Дегидрогалогенирование моногалогеналканов при действии спиртового_раствора щелочи : СН3−СНBr−CH3 + KOH (спирт) → CH3−CH=CH2 +
- 17. Применение алкенов Получение спиртов, альдегидов, кислот Получение полимеров и пластмасс Этилен –для ускорения созревания плодов Получение
- 19. Скачать презентацию






 Как жили земледельцы и ремесленники в египте
Как жили земледельцы и ремесленники в египте Кордиеритовая керамика
Кордиеритовая керамика Презентация на тему Магнетизм
Презентация на тему Магнетизм  GOOGLE СЛУЖИТ НАРОДУ
GOOGLE СЛУЖИТ НАРОДУ День Победы
День Победы beetles
beetles  Диагностика коллектива и личности ребенка как основа планирования воспитательной работы. Воспитательные и социально – воспитате
Диагностика коллектива и личности ребенка как основа планирования воспитательной работы. Воспитательные и социально – воспитате Компания ООО РедКаско приглашает на работу
Компания ООО РедКаско приглашает на работу Лекция №1. Введение в КСЕ.Природа, культура, наука.
Лекция №1. Введение в КСЕ.Природа, культура, наука. Операционные системы
Операционные системы V Версия 2.00
V Версия 2.00 Ya_kontseptsia_Ya_ustal
Ya_kontseptsia_Ya_ustal ФЭМП Измерение объема
ФЭМП Измерение объема -50% на ваш товар
-50% на ваш товар МОУ Волжская СОШ Красноярского района6 Б класс
МОУ Волжская СОШ Красноярского района6 Б класс Великая Отечественная Война 1941-1945
Великая Отечественная Война 1941-1945 The depletion of ozone layer
The depletion of ozone layer  Обсуждение, развитие идеи и разработка эскиза. Планирование работы
Обсуждение, развитие идеи и разработка эскиза. Планирование работы К.Д.Ушинский - классик педагогики и мой учитель.
К.Д.Ушинский - классик педагогики и мой учитель. Алгоритм определения объемов электроэнергии, реализуемых по регулируемым и нерегулируемым ценам
Алгоритм определения объемов электроэнергии, реализуемых по регулируемым и нерегулируемым ценам Экология жилища
Экология жилища основная_презентация_школа21_031022
основная_презентация_школа21_031022 Особенности польского произношения
Особенности польского произношения Приказ от 30.12.2021г. № 456 Об утверждении положения об оплате труда работников ФГБУ Госсорткомиссия
Приказ от 30.12.2021г. № 456 Об утверждении положения об оплате труда работников ФГБУ Госсорткомиссия История возникновения книги
История возникновения книги Анализ деятельности МОУ Стремуткинской средней общеобразовательной школы по формированию положительного имиджа.
Анализ деятельности МОУ Стремуткинской средней общеобразовательной школы по формированию положительного имиджа. Генетика
Генетика Команда: Акционерное Общество Научно-исследовательский институт полимерных материалов
Команда: Акционерное Общество Научно-исследовательский институт полимерных материалов