Содержание
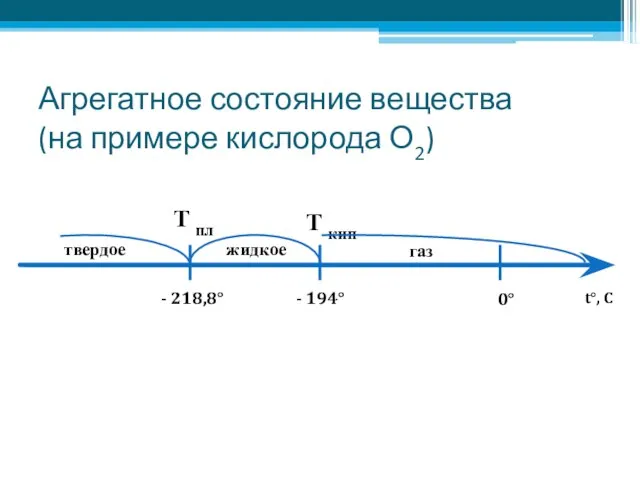
- 2. Агрегатное состояние вещества (на примере кислорода О2) - 218,8° - 194° 0° t°, C Т пл
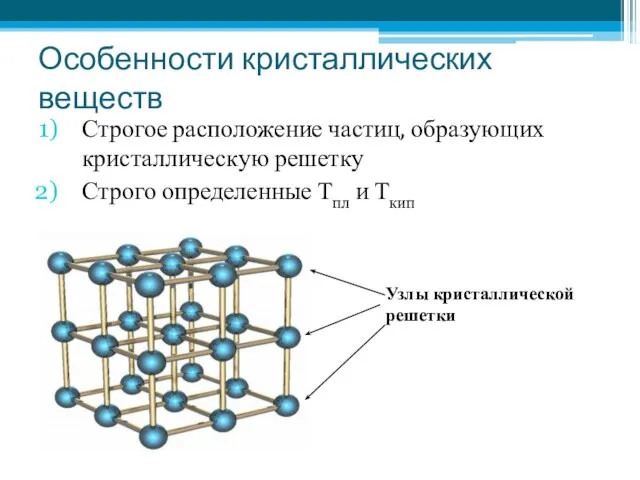
- 3. Особенности кристаллических веществ Строгое расположение частиц, образующих кристаллическую решетку Строго определенные Тпл и Ткип Узлы кристаллической
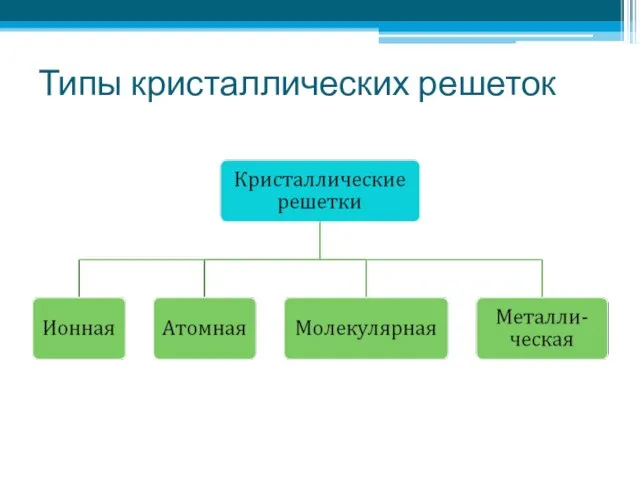
- 4. Типы кристаллических решеток
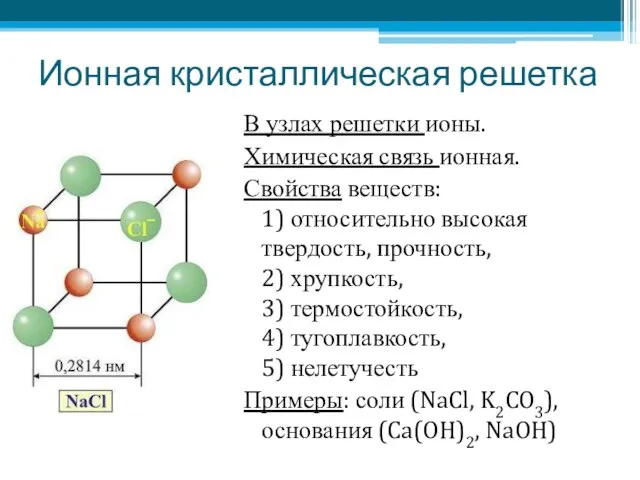
- 5. Ионная кристаллическая решетка В узлах решетки ионы. Химическая связь ионная. Свойства веществ: 1) относительно высокая твердость,
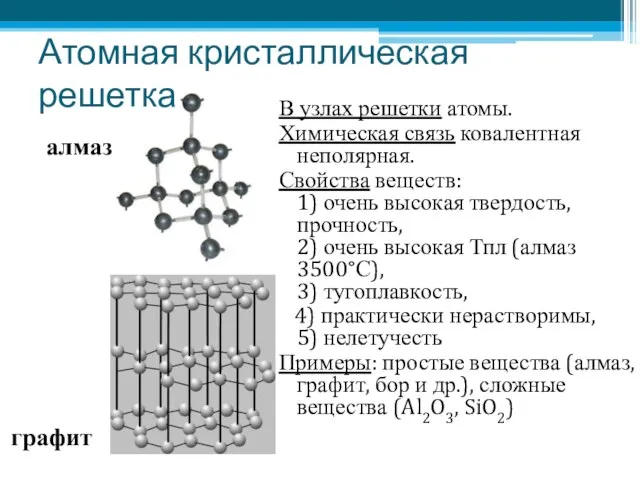
- 6. Атомная кристаллическая решетка В узлах решетки атомы. Химическая связь ковалентная неполярная. Свойства веществ: 1) очень высокая
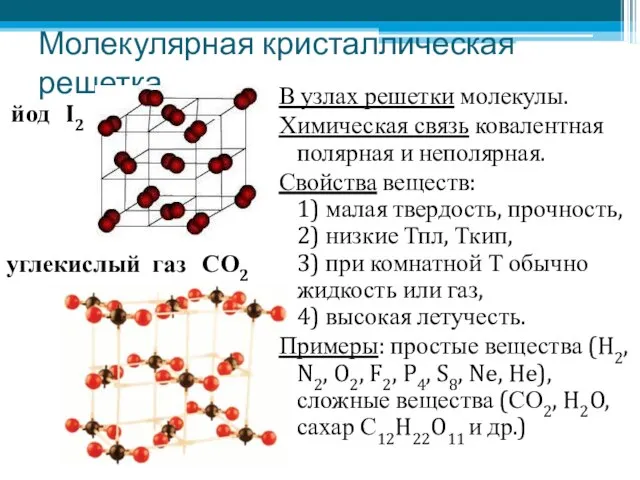
- 7. Молекулярная кристаллическая решетка В узлах решетки молекулы. Химическая связь ковалентная полярная и неполярная. Свойства веществ: 1)
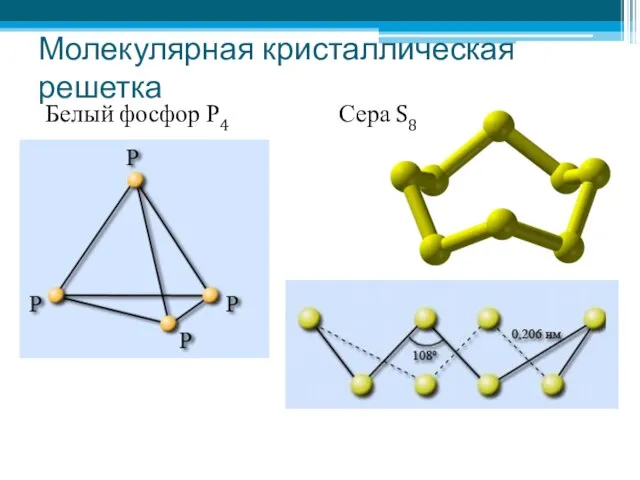
- 8. Молекулярная кристаллическая решетка Белый фосфор Р4 Сера S8
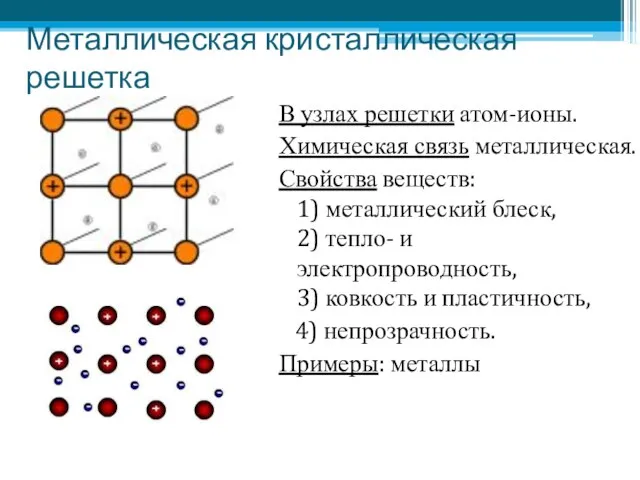
- 9. Металлическая кристаллическая решетка В узлах решетки атом-ионы. Химическая связь металлическая. Свойства веществ: 1) металлический блеск, 2)
- 10. Закон постоянства состава (Пруст, 1799-1803) Молекулярные химические соединения независимо от способа их получения имеют постоянный состав
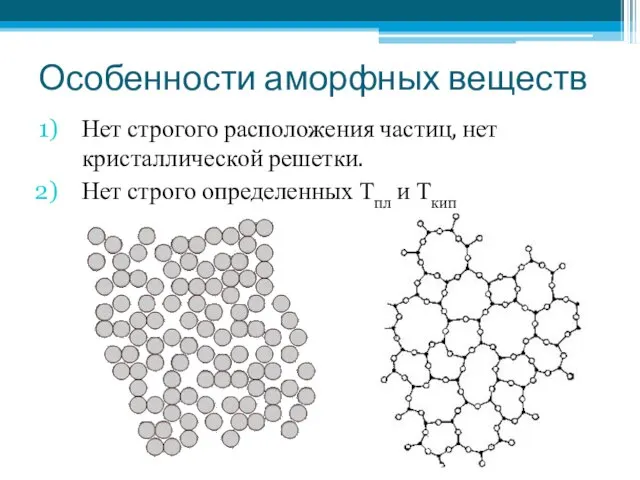
- 11. Особенности аморфных веществ Нет строгого расположения частиц, нет кристаллической решетки. Нет строго определенных Тпл и Ткип
- 12. Аморфные вещества
- 13. Аморфные вещества
- 14. Аморфные вещества
- 15. Аморфные вещества
- 16. Аморфные вещества
- 17. Аморфные вещества
- 18. Аморфные вещества
- 19. Задание. Определите тип кристаллической решетки в веществах KNO3 NO2 CH4 Si Fe NaF As
- 21. Скачать презентацию








 Труд и творчество 6 класс
Труд и творчество 6 класс Зимующие птицы
Зимующие птицы Рresident of Egypt
Рresident of Egypt Развитие регионального сегмента ЕИАС в Санкт-Петербурге
Развитие регионального сегмента ЕИАС в Санкт-Петербурге Планирование учебного процесса на основе перехода к системе зачетных единиц
Планирование учебного процесса на основе перехода к системе зачетных единиц Команда НИУ ВШЭ. Конкурс им. Филипа Джессопа
Команда НИУ ВШЭ. Конкурс им. Филипа Джессопа Презентация на тему ПСОРИАЗ
Презентация на тему ПСОРИАЗ  Диагностическая линия NTS 5xx
Диагностическая линия NTS 5xx Фотоальбом. Комсомольск- на- Амуре
Фотоальбом. Комсомольск- на- Амуре Structure. Quick review
Structure. Quick review Сертификаты и лицензии
Сертификаты и лицензии Моя студенческая жизнь!
Моя студенческая жизнь! Поздравления с днём Студента
Поздравления с днём Студента Тренажер: Части речи
Тренажер: Части речи Числовые характеристики изображений
Числовые характеристики изображений Презентация на тему Изобразительное искусство реализма
Презентация на тему Изобразительное искусство реализма Результати першого випуску за програмою підготовки Школа професійного розвитку інженерів-конструкторів
Результати першого випуску за програмою підготовки Школа професійного розвитку інженерів-конструкторів 22 июня – День памяти и скорби
22 июня – День памяти и скорби Правописание безударных окончаний имён существительных
Правописание безударных окончаний имён существительных Псалмопевец Давид
Псалмопевец Давид Игра Зоопарк
Игра Зоопарк Михаил Михайлович Зощенко 1894 -1958
Михаил Михайлович Зощенко 1894 -1958  ПРЕЗЕНТАЦИЯ
ПРЕЗЕНТАЦИЯ A day
A day Перспективы книжной розницы:Облачность или конец света
Перспективы книжной розницы:Облачность или конец света ИЭК Сервис. Отчет за 2020 год. Перечень услуг и работ по управлению, содержанию и текущему ремонту общего имущества
ИЭК Сервис. Отчет за 2020 год. Перечень услуг и работ по управлению, содержанию и текущему ремонту общего имущества Профессиональные и образовательные стандарты в области ИТ как инструмент подготовки кадров для перспективных потребностей росси
Профессиональные и образовательные стандарты в области ИТ как инструмент подготовки кадров для перспективных потребностей росси РЕСУРС-МАСТЕР®
РЕСУРС-МАСТЕР®