Слайд 2Химический состав
Основные химические элементы, входящие в состав белков
С(углерод) – 50%
O(кислород) – 17-24%
H(водород)

– 6,5-7,3%
N(азот) – 15-18%
S(сера) – 0,2-2,4%
Белки – это полимеры, мономерами которых являются аминокислоты.
Слайд 3Строение аминокислот
Общая формула:
- основная группа
- кислотная группа
- радикал

Слайд 4Строение аминокислоты
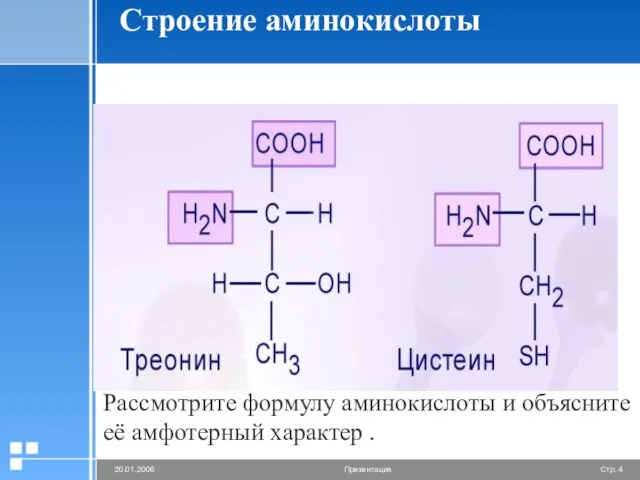
Рассмотрите формулу аминокислоты и объясните
её амфотерный характер .
Слайд 5Пептидная связь
Соединение молекул аминокислот:
Рассмотрите схему образования дипептида.
Какие атомы образовали молекулу воды в

результате соединения двух аминокислот?
Слайд 6Полимер, состоящий из аминокислот

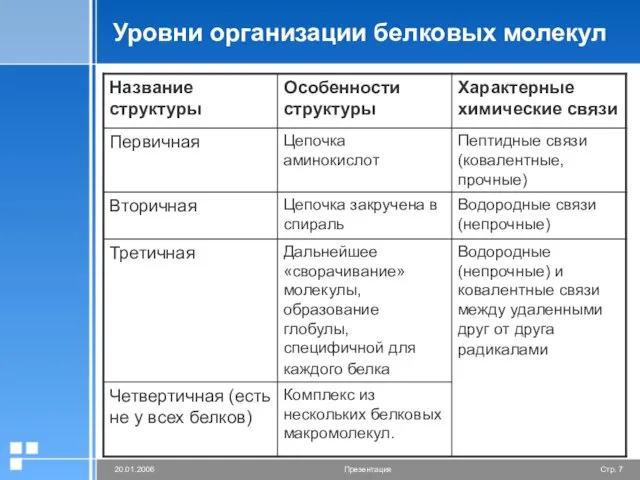
Слайд 7Уровни организации белковых молекул
Слайд 8Первичная структура белка
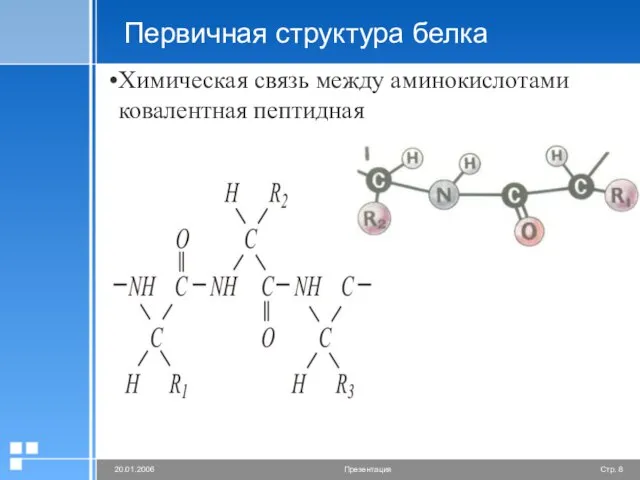
Химическая связь между аминокислотами
ковалентная пептидная
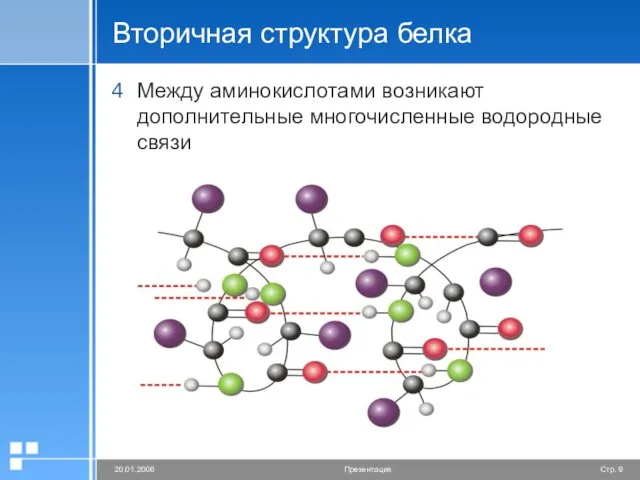
Слайд 9Вторичная структура белка
Между аминокислотами возникают дополнительные многочисленные водородные связи
Слайд 10Третичная структура белка
Образована дисульфидными (S-S-), гидрофобными и ионными связями

Слайд 11Четвертичная структура белка
Её образуют ионные, водородные, гидрофобные связи.

Слайд 12Свойства белков
Белки – водорастворимые молекулы
Несут большой поверхностный заряд
Термолабильны
Им присуща денатурация
Ренатурация
Слайд 13Денатурация белка
Денатурация белка - нарушение природной вторичной и третичной структуры белка под

действием природных факторов (температуры, радиации, химических веществ, и т.д.)
Виды денатурации:
Обратимая
Необратимая














 Содержание Концепции компетентностно- ориентированного образования и меры по ее реализации
Содержание Концепции компетентностно- ориентированного образования и меры по ее реализации Архангельск, тренинг промоутеров
Архангельск, тренинг промоутеров Проект – презентация«Город Николаевск – на – Амуре»
Проект – презентация«Город Николаевск – на – Амуре» wellies a rubber
wellies a rubber Зотова Ирина, родилась на Юге России. Аспирантка Российской Академии Государственной Службы. Кафедра Акмеологии и психологии проф
Зотова Ирина, родилась на Юге России. Аспирантка Российской Академии Государственной Службы. Кафедра Акмеологии и психологии проф Эмоциональный интеллект. Развитие ребенка - развитие семьи
Эмоциональный интеллект. Развитие ребенка - развитие семьи Новый программный продукт для предприятий электроэнергетики!
Новый программный продукт для предприятий электроэнергетики! Номинация проекта: «Математическое моделирование реальных процессов в природе и обществе»
Номинация проекта: «Математическое моделирование реальных процессов в природе и обществе» Формирование метапредметных компетенций школьников в урочной и внеурочной деятельности
Формирование метапредметных компетенций школьников в урочной и внеурочной деятельности 1-2 Software
1-2 Software Стажировка в Высшей медицинской школе Ганновера (Германия)
Стажировка в Высшей медицинской школе Ганновера (Германия) Oriflame. Вырасти от старшего менеджера до директора
Oriflame. Вырасти от старшего менеджера до директора 39 лет итальянской красоты от природы 1972В Пиенце (Тоскания, Италия) открывается лавка, торгующая лечебными травами под названием Botte
39 лет итальянской красоты от природы 1972В Пиенце (Тоскания, Италия) открывается лавка, торгующая лечебными травами под названием Botte Опыт внедрения системы Офис-кайдзен в ТЭЦ ОАО Иркутскэнерго
Опыт внедрения системы Офис-кайдзен в ТЭЦ ОАО Иркутскэнерго Extra sport club
Extra sport club Культура и быт России в XVII веке
Культура и быт России в XVII веке Осуществление системного подхода к формированию мыслительных умений и навыков в процессе преподавания физики
Осуществление системного подхода к формированию мыслительных умений и навыков в процессе преподавания физики Композиция и сюжет в изобразительном искусстве
Композиция и сюжет в изобразительном искусстве Плоскость. Прямая. Луч.
Плоскость. Прямая. Луч. ВНЕУРОЧНАЯ ДЕЯТЕЛЬНОСТЬКАК СОСТАВЛЯЮЩАЯФедерального государственногообразовательного стандарта НОВОГО ПОКОЛЕНИЯ
ВНЕУРОЧНАЯ ДЕЯТЕЛЬНОСТЬКАК СОСТАВЛЯЮЩАЯФедерального государственногообразовательного стандарта НОВОГО ПОКОЛЕНИЯ Презентация на тему COLOURS
Презентация на тему COLOURS  МАСС-СПЕКТРОМЕТРИЯ В ПРОТЕОМНЫХ ИССЛЕДОВАНИЯХ
МАСС-СПЕКТРОМЕТРИЯ В ПРОТЕОМНЫХ ИССЛЕДОВАНИЯХ Магнитогорский государственный технический университет им. Г.И. Носова. Институт строительства архитектуры и искусства. Дизайн
Магнитогорский государственный технический университет им. Г.И. Носова. Институт строительства архитектуры и искусства. Дизайн Презентация на тему Диагностика эффективности внеурочной деятельности
Презентация на тему Диагностика эффективности внеурочной деятельности  Инструментальный ансамбль Путешествуем с гитарой. Итоги учебного года 2019-2020
Инструментальный ансамбль Путешествуем с гитарой. Итоги учебного года 2019-2020 Учтивость в словах и обращениях современного школьника.
Учтивость в словах и обращениях современного школьника. Приёмы работы с картиной
Приёмы работы с картиной Сотовый телефон : за и против
Сотовый телефон : за и против