Содержание
- 2. Теория электролитической диссоциации. Изучив тему, следует знать: Основные положения теории электролитической диссоциации. Кислоты, основания и соли
- 3. Писать уравнения диссоциации кислот, оснований и солей. Определять реакции ионного обмена, идущие до конца, составлять уравнения
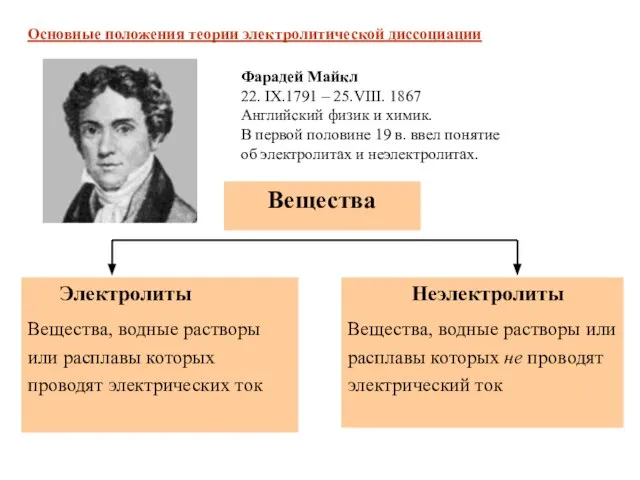
- 4. Основные положения теории электролитической диссоциации Фарадей Майкл 22. IX.1791 – 25.VIII. 1867 Английский физик и химик.
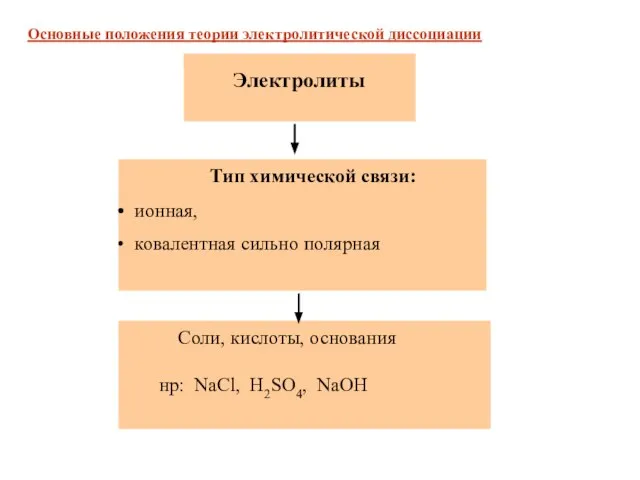
- 5. Тип химической связи: ионная, ковалентная сильно полярная Электролиты Соли, кислоты, основания нр: NaCl, H2SO4, NaOH Основные
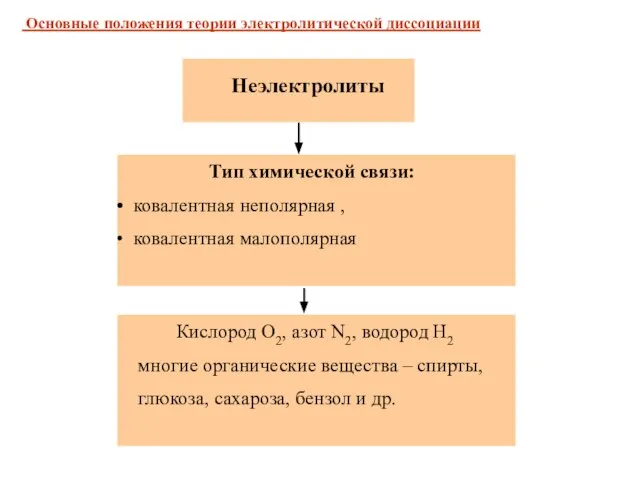
- 6. Неэлектролиты Тип химической связи: ковалентная неполярная , ковалентная малополярная Кислород O2, азот N2, водород H2 многие
- 7. Сванте Август Аррениус- 1859 – 1927 г.г. Шведский физико-химик. Автор теории электролитической диссоциации (1887 г.) В
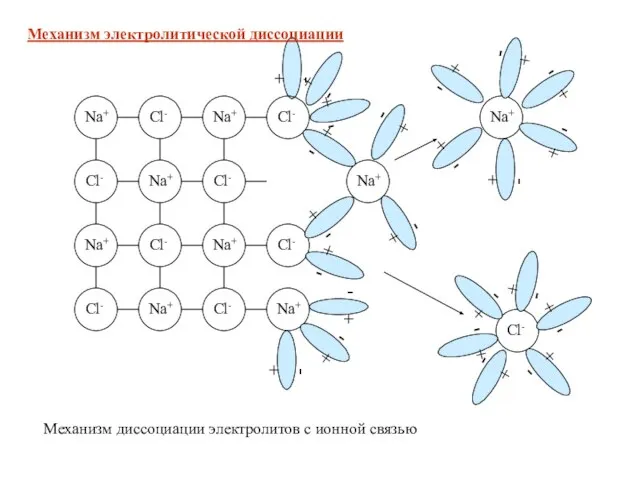
- 8. + - Механизм диссоциации электролитов с ионной связью Механизм электролитической диссоциации
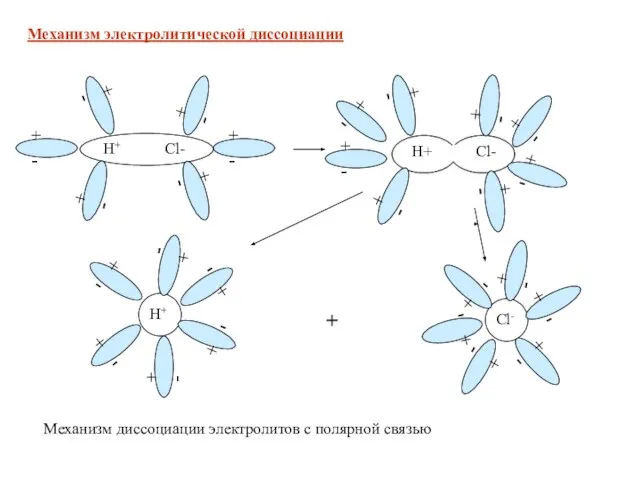
- 9. + - Механизм диссоциации электролитов с полярной связью Механизм электролитической диссоциации
- 10. Степень электролитической диссоциации. Сильные и слабые электролиты Степень электролитической диссоциации – число, показывающее, какая часть молекул
- 11. Степень диссоциации (α) зависит от природы растворяемого вещества и растворителя. концентрации раствора. При разбавлении раствора, α
- 12. Сильные электролиты (α → 1 или 100%) соли 2) сильные кислоты (H2SO4, HCl, HNO3, HClO4, HClO3,
- 13. Слабые электролиты (α → 0) 1) вода 2) cлабые кислоты (H2S, H2CO3, H2SiO3, HNO2, H3PO4, H2SO3,
- 14. Кд (NH4OH) = 1,8 · 10-5 Кд (H2O) = 1,8 · 10-16 Степень электролитической диссоциации. Сильные
- 15. Кислоты, основания и соли с точки зрения ТЭД Уравнение электролитической диссоциации сильных кислот: HCl ↔ H+
- 16. Уравнение диссоциации сильных оснований (щелочей) NaOH ↔ Na+ + OH- Ba(OH)2 ↔ Ba2+ + 2OH- Слабые
- 17. Уравнение электролитической диссоциации Zn(OH)2 (без учета ступенчатого характера) 2H+ + ZnO22- ↔ H2ZnO2 = Zn(OH)2 ↔
- 18. K2CO3 ↔ 2K+ + CO32- Al2(SO4)3 ↔ 2Al3+ + 3SO42- Средние (нормальные) соли – сильные электролиты,
- 19. NaHCO3 ↔ Na+ + HCO3- (α = 1) НСО3- ↔ Н+ + СО32- (α Кислые соли
- 20. Основные соли – электролиты, которые при диссоциации образуют анионы кислотного остатка и сложные катионы, состоящие из
- 21. Условия течения реакций ионного обмена до конца Реакции, протекающие между ионами, называются ионными реакциями.
- 22. образование малорастворимых веществ (осадки ↓) 2) образование газообразных или летучих веществ (↑) 3) образование малодиссоциирующих веществ
- 23. Реакции с образованием малорастворимых веществ, выпадающих в осадок молекулярное уравнение: AgNO3 + HCl → AgCl↓ +
- 24. 2. Реакции, протекающие с образованием газообразных или летучих веществ молекулярное уравнение: Na2CO3 + 2HCl → 2NaCl
- 25. 3. Реакции, идущие с образованием малодиссоциирующих веществ – слабых электролитов молекулярное уравнение: NaOH + HCl →
- 26. Если исходными веществами реакций обмена являются сильные электролиты, которые при взаимодействии не образуют малорастворимых или малодиссоциирующих
- 27. Диссоциация воды. Водородный показатель H2O ↔ H+ + OH- При 250С [Н+] = [ОН-] = 10-7
- 28. Диссоциация воды. Водородный показатель Водородный показатель рН - это отрицательный десятичный логарифм концентрации ионов водорода Н+
- 29. Если [Н+] = 10-7 моль/л , то рН = - lg 10-7 = 7 среда раствора
- 31. Скачать презентацию




















![Диссоциация воды. Водородный показатель H2O ↔ H+ + OH- При 250С [Н+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/373229/slide-26.jpg)

![Если [Н+] = 10-7 моль/л , то рН = - lg 10-7](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/373229/slide-28.jpg)
 Презентация на тему My family (2 класс)
Презентация на тему My family (2 класс) Задачи на построение являются одними из основных задач школьного курса геометрии, которые формируют необходимые практические нав
Задачи на построение являются одними из основных задач школьного курса геометрии, которые формируют необходимые практические нав Аннотация проекта
Аннотация проекта С. Ю. Витте – личность и реформы
С. Ю. Витте – личность и реформы Каждый ребенок имеет право, ответственность и обязанность
Каждый ребенок имеет право, ответственность и обязанность Загадка
Загадка Lektsiya dlya vechernikov_ Upravlenie kontentom v organizatsii
Lektsiya dlya vechernikov_ Upravlenie kontentom v organizatsii Работа с дробями
Работа с дробями Мал шаруашылығы өнімдерінің ауыр металл тұздарымен ластануын анықтау және оларға қарсы ветсаншараларды ұйымдастыру
Мал шаруашылығы өнімдерінің ауыр металл тұздарымен ластануын анықтау және оларға қарсы ветсаншараларды ұйымдастыру Образ художника. Сюрреализм
Образ художника. Сюрреализм Программа «Paint»
Программа «Paint» Healthy Food
Healthy Food Лекция 1
Лекция 1 Расширенное Участие Trust Fund Кодексав деятельности Кодекса
Расширенное Участие Trust Fund Кодексав деятельности Кодекса Техническое задание. Фотографии
Техническое задание. Фотографии Инициативное бюджетирование для школьников: опыт Санкт-Петербурга
Инициативное бюджетирование для школьников: опыт Санкт-Петербурга Организационная встреча для участников ПМАМ 2021-22 уч.г
Организационная встреча для участников ПМАМ 2021-22 уч.г Геометрия египетских пирамид
Геометрия египетских пирамид VII Всероссийский конкурс учебно-исследовательских экологических проектов «Человек на Земле» Номинация №3 «Этнографические исс
VII Всероссийский конкурс учебно-исследовательских экологических проектов «Человек на Земле» Номинация №3 «Этнографические исс Основы метапредметного обучения русскому языку и формирование лингвистической компетентности всех участников образовательного
Основы метапредметного обучения русскому языку и формирование лингвистической компетентности всех участников образовательного  Цилиндр (задача В-9)
Цилиндр (задача В-9) Урок правовых знаний
Урок правовых знаний Мыши: внешний вид, образ жизни. Профилактика, средства избавления
Мыши: внешний вид, образ жизни. Профилактика, средства избавления Интуиция
Интуиция ООО «Инновационно-трастовая энергетическая компания»
ООО «Инновационно-трастовая энергетическая компания» История фотографии (9 класс)
История фотографии (9 класс) Мастер-класс: Техника Друдлы
Мастер-класс: Техника Друдлы СЛУЖБА СКОРОЙ МЕДИЦИНСКОЙ ПОМОЩИ В СИСТЕМЕ ОМС
СЛУЖБА СКОРОЙ МЕДИЦИНСКОЙ ПОМОЩИ В СИСТЕМЕ ОМС