Слайд 2Цель:
Изучить электрические и химические процессы в электролитах.

Слайд 3Задачи:
Доказать что концентрация раствора электролита влияет на силу тока.
Установить, как влияет

расстояния между электродами на силу тока.
Выяснить, как влияет природа электролита на силу тока в нём.
Слайд 4План
I.Введение.
II.Основная часть.
К истории законов электролиза.
Библиографическая справка о М. Фарадеи.
Электрический ток в

электролитах.
III.Практическая часть.
IV. Выводы.
Слайд 6ФАРАДЕЙ (Faraday) Майкл
(1791-1867)
Английский физик, основоположник учения об электромагнитном поле, иностранный

почетный член Петербургской АН (1830). Обнаружил химическое действие электрического тока, взаимосвязь между электричеством и магнетизмом, магнетизмом и светом. Открыл (1831) электромагнитную индукцию — явление, которое легло в основу электротехники. Установил (1833-34) законы электролиза, названные его именем, открыл пара- и диамагнетизм, вращение плоскости поляризации света в магнитном поле (эффект Фарадея). Доказал тождественность различных видов электричества. Ввел понятия электрического и магнитного поля, высказал идею существования электромагнитных волн.
Слайд 7Термин
«электролит»
(от греческого
«разлагаемый электричеством»)
впервые предложил английский
химик и физик
М.Фарадей

Слайд 8Электролитами принято называть
проводящие среды, в которых
протекание электрического тока
сопровождается переносом

вещества.
Слайд 9Прохождение электрического тока через электролит сопровождается выделением веществ на электродах.
Это явление
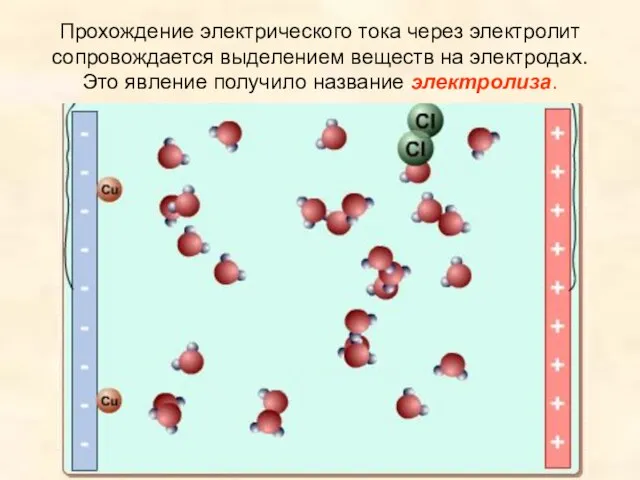
получило название электролиза.
Слайд 10Ток в растворах электролитов – это упорядоченное движение положительных и отрицательных ионов.
Электролиз
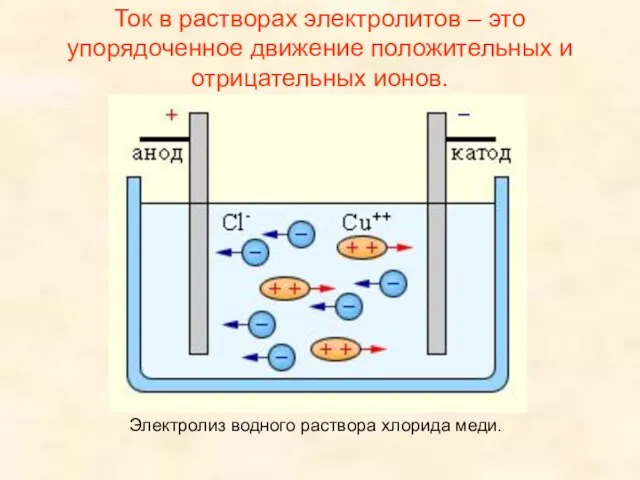
водного раствора хлорида меди.
Слайд 11Первый закон электролиза.
Закон электролиза был экспериментально установлен английским физиком М. Фарадеем в

1833 году. Закон Фарадея определяет количества первичных продуктов, выделяющихся на электродах при электролизе.
Слайд 12Первый закон электролиза.
Масса m вещества, выделившегося на электроде, прямо пропорциональна заряду q,

прошедшему через электролит:
m=kq=kIt.
Слайд 13Второй закон Фарадея
Данный закон отвечает на вопрос от чего зависит электрохимический

эквивалент.
Электрохимические эквиваленты различных веществ пропорциональны их атомным весам и обратно пропорциональны числам, выражающим их химическую валентность.
Слайд 16Практическая часть №1
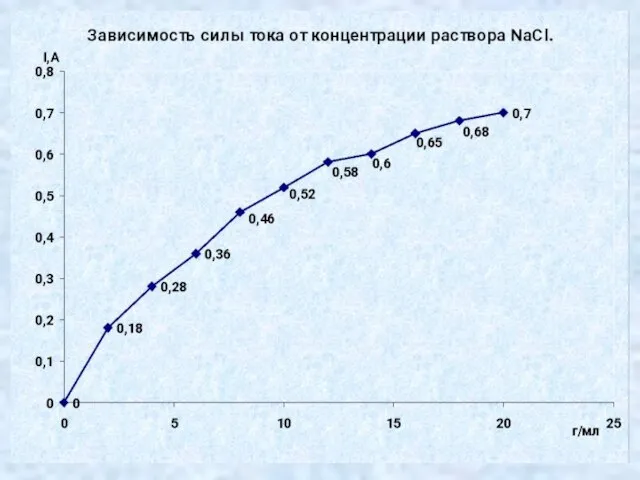
Доказать что концентрация раствора электролита влияет на силу тока.

Слайд 18Вывод № 1.
Сила тока зависит от концентрации раствора, чем насыщение раствор, тем

больше сила тока.
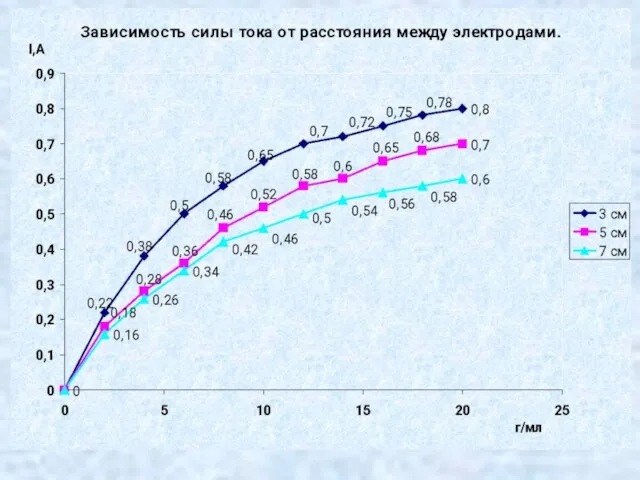
Слайд 19Практическая часть № 2.
Установить, как влияет расстояния между электродами на силу тока.

Слайд 21Вывод № 2.
Сила тока зависит от расстояния между электродами, чем меньше расстояние

тем больше сила тока и наоборот.
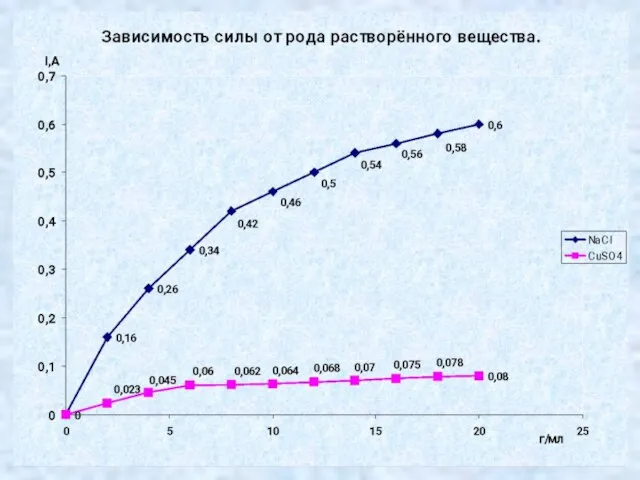
Слайд 22Практическая часть № 3.
Выяснить, как влияет природа электролита на силу тока в

нём.
Слайд 24Вывод № 3.
Различные электролиты по-разному проводят электрический ток.

Слайд 25Применение электролиза
Электрический метод получения чистых металлов.
Гальваностегия.
Гальванопластика.
Электрическая полировка.
Электрометаллургия.

Слайд 26Вывод:
Сам факт разложение электролитов при прохождении через них тока показывает, что в

них движения зарядов сопровождается движение атомов или групп атомов, связанных друг с другом; эти атомы или атомные группы представляют собой части молекулы растворенного вещества. Естественно предположить, что заряжены именно эти части молекул в растворе и что они являются носителями электрического заряда. Их перемещение под действием сил электрического поля и представляют собой электрический ток, идущий через электролит. Тщательно поставленные опыты позволили установить, что для электролитов справедлив закон Ома.





















 Коммерческая лига по мини-футболу г. Череповец
Коммерческая лига по мини-футболу г. Череповец Текстовый редактор Microsoft WORD
Текстовый редактор Microsoft WORD Фестиваль семейного творчества. Творчество семьи Рамата
Фестиваль семейного творчества. Творчество семьи Рамата Математические игры как средство развития логического мышления дошкольника
Математические игры как средство развития логического мышления дошкольника ЧЕЛОЕК. ПРАВО. ГОСУДАРСТВО
ЧЕЛОЕК. ПРАВО. ГОСУДАРСТВО Practical Phonetics
Practical Phonetics Физика и оружие победы
Физика и оружие победы Сергей Есенин
Сергей Есенин Easy Chinese online course lesson 成功之路. Вопросительные местоимения
Easy Chinese online course lesson 成功之路. Вопросительные местоимения КУРСЫ ПОВЫШЕНИЯ КВАЛИФИКАЦИИ в рамках совместного европейского проекта TEMPUS-WeNeT «Создание сети дистанционного повышения квалифик
КУРСЫ ПОВЫШЕНИЯ КВАЛИФИКАЦИИ в рамках совместного европейского проекта TEMPUS-WeNeT «Создание сети дистанционного повышения квалифик Язык Рефлекс – диалект Си для программирования ПЛК
Язык Рефлекс – диалект Си для программирования ПЛК Escentric Molecules. Качество упаковки
Escentric Molecules. Качество упаковки Защита окружающей среды (Global Problems of Ecology)
Защита окружающей среды (Global Problems of Ecology) Долговременная терапия эндометриоидной болезни прогестинами нового поколения
Долговременная терапия эндометриоидной болезни прогестинами нового поколения На рассвете у Воскресенского моста. Конец XVII века
На рассвете у Воскресенского моста. Конец XVII века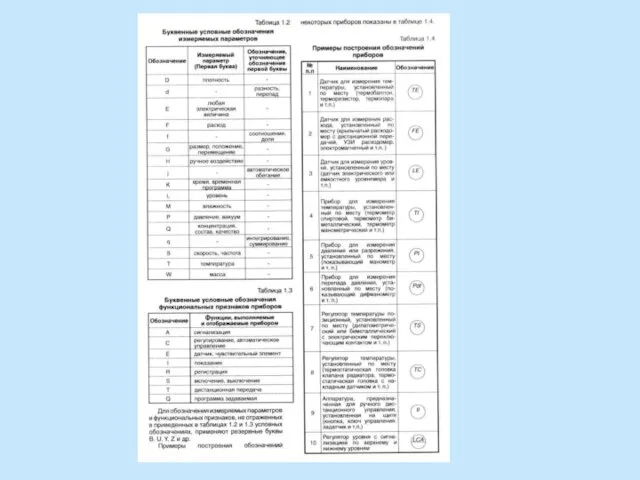 Часть автоматической систем ТГВ
Часть автоматической систем ТГВ Арт-бизнес консалтинг. Рецепты управленческой кухни. Нематериальная мотивация
Арт-бизнес консалтинг. Рецепты управленческой кухни. Нематериальная мотивация Профессии искусства. Художник
Профессии искусства. Художник Наталья Николаевна Пушкина
Наталья Николаевна Пушкина Труд людей весной. 1 класс
Труд людей весной. 1 класс Шаблон проекта
Шаблон проекта Самоклеящаяся термоэтикетка
Самоклеящаяся термоэтикетка New trends of architectures
New trends of architectures  Китайский язык
Китайский язык Аналитический обзор “Юридическое образование в России”
Аналитический обзор “Юридическое образование в России” Pedagogika_vysshey_shkoly
Pedagogika_vysshey_shkoly С днём Святого Валентина! Желаем счастья в этот день, Тепла от всех кто будет рядом, Улыбок светлых на лице.
С днём Святого Валентина! Желаем счастья в этот день, Тепла от всех кто будет рядом, Улыбок светлых на лице. Политика разрядки: надежды и результаты
Политика разрядки: надежды и результаты