Содержание
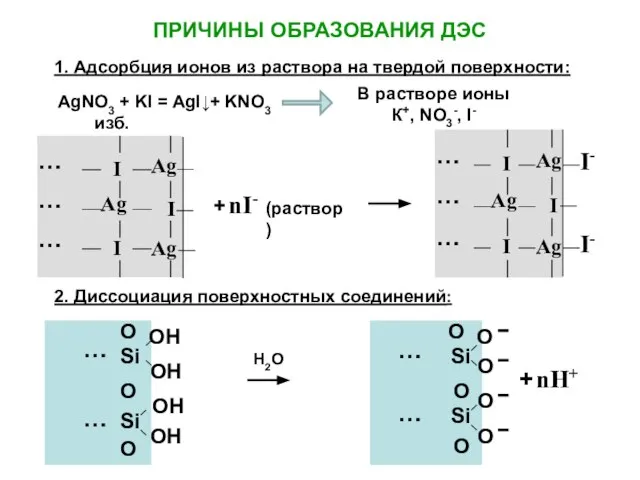
- 2. ПРИЧИНЫ ОБРАЗОВАНИЯ ДЭС 1. Адсорбция ионов из раствора на твердой поверхности: 2. Диссоциация поверхностных соединений: AgNO3
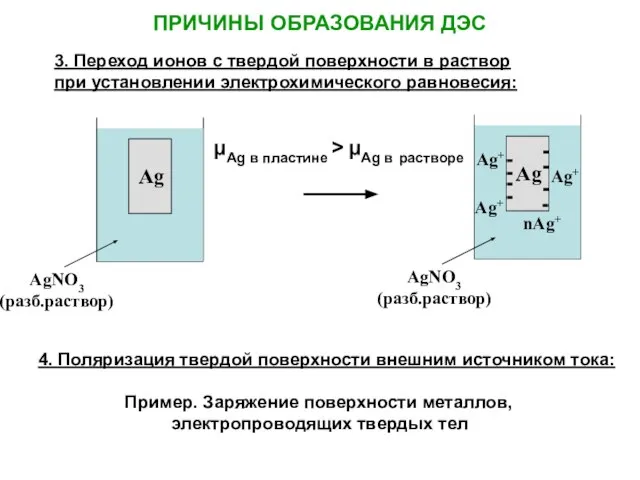
- 3. 3. Переход ионов с твердой поверхности в раствор при установлении электрохимического равновесия: 4. Поляризация твердой поверхности
- 4. Терминология ДЭС Приготовление золя AgI с отрицательным зарядом коллоидной частицы: AgNO3 + KI = AgI↓+ KNO3
- 5. ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ, ОПИСЫВАЮЩИЙ СОСТОЯНИЕ ИОНОВ В РАСТВОРЕ
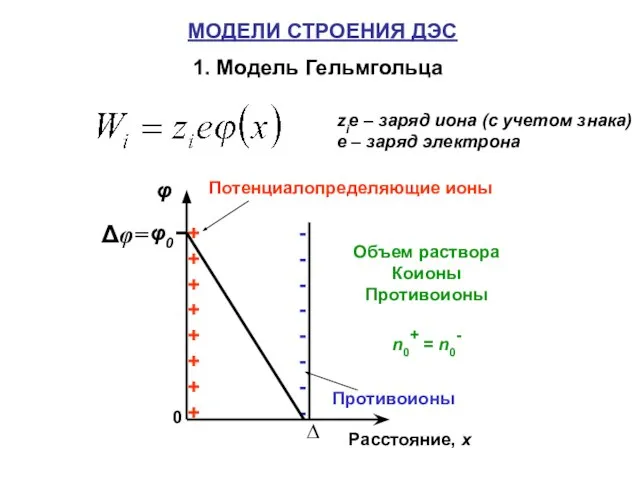
- 6. МОДЕЛИ СТРОЕНИЯ ДЭС 1. Модель Гельмгольца zie – заряд иона (с учетом знака) е – заряд
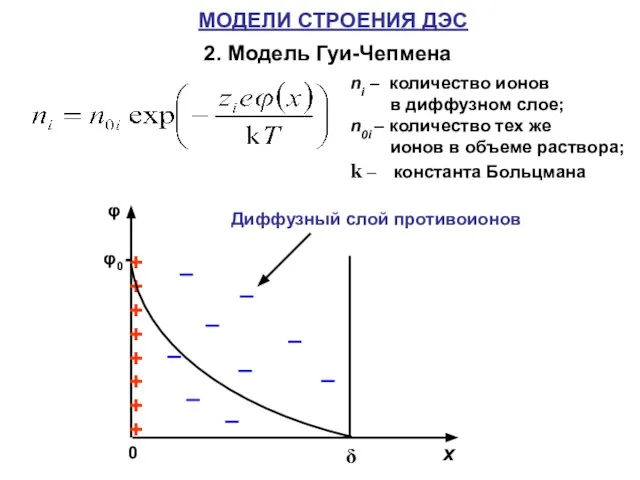
- 7. МОДЕЛИ СТРОЕНИЯ ДЭС 2. Модель Гуи-Чепмена ni – количество ионов в диффузном слое; n0i – количество
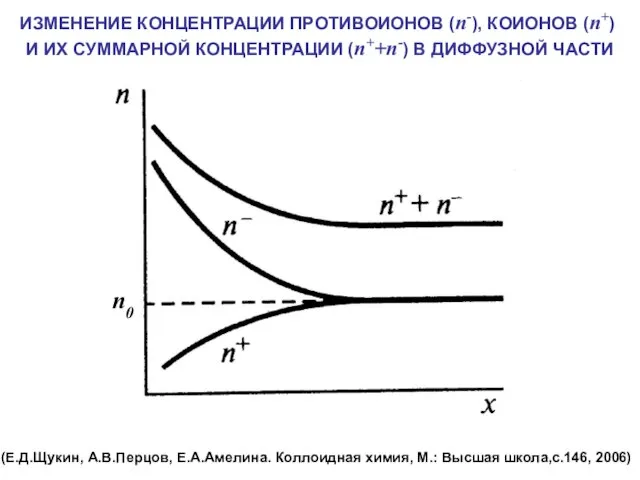
- 8. ИЗМЕНЕНИЕ КОНЦЕНТРАЦИИ ПРОТИВОИОНОВ (n-), КОИОНОВ (n+) И ИХ СУММАРНОЙ КОНЦЕНТРАЦИИ (n++n-) В ДИФФУЗНОЙ ЧАСТИ (Е.Д.Щукин, А.В.Перцов,
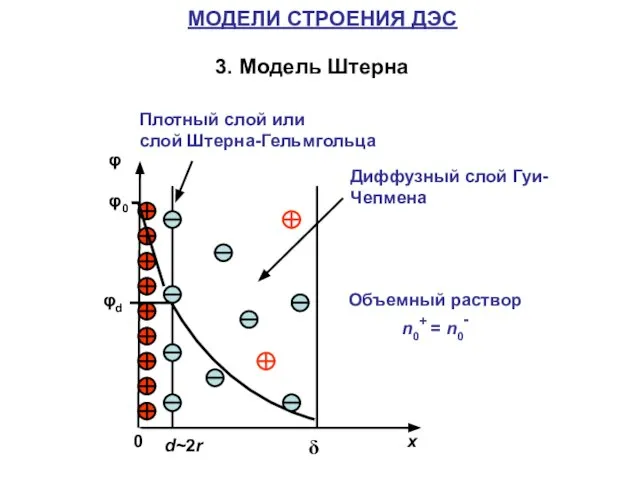
- 9. МОДЕЛИ СТРОЕНИЯ ДЭС 3. Модель Штерна
- 10. Для плоской поверхности раздела и для симметричного электролита Краевые условия: 1. 2. Уравнение Пуассона ЗАВИСИМОСТЬ ПОТЕНЦИАЛА
- 11. ЗАВИСИМОСТЬ ПОТЕНЦИАЛА ДИФФУЗНОГО СЛОЯ ОТ РАССТОЯНИЯ ОТ ТВЕРДОЙ ПОВЕРХНОСТИ где при ;
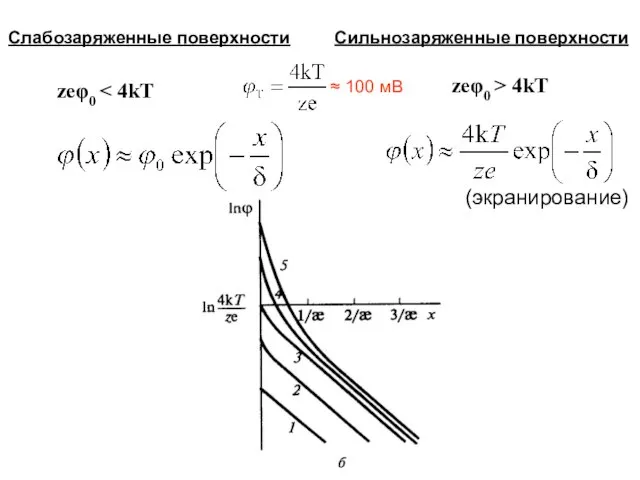
- 12. Слабозаряженные поверхности Сильнозаряженные поверхности (экранирование) zeφ0 zeφ0 > 4kT
- 13. ФОРМУЛА МИЦЕЛЛЫ ГИДРОФОБНОГО ЗОЛЯ AgI { (mAgI) nI- (n-x)K + } x- xK +
- 14. - Электрокинетический потенциал ζ ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ДЭС: - Толщина плотного слоя d - Эффективная толщина диффузного
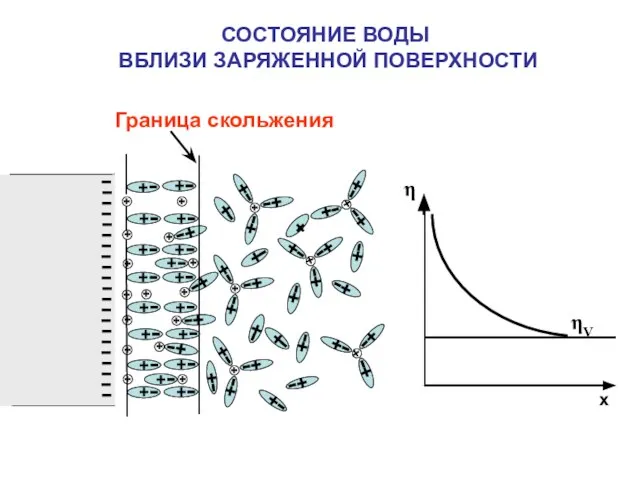
- 15. СОСТОЯНИЕ ВОДЫ ВБЛИЗИ ЗАРЯЖЕННОЙ ПОВЕРХНОСТИ
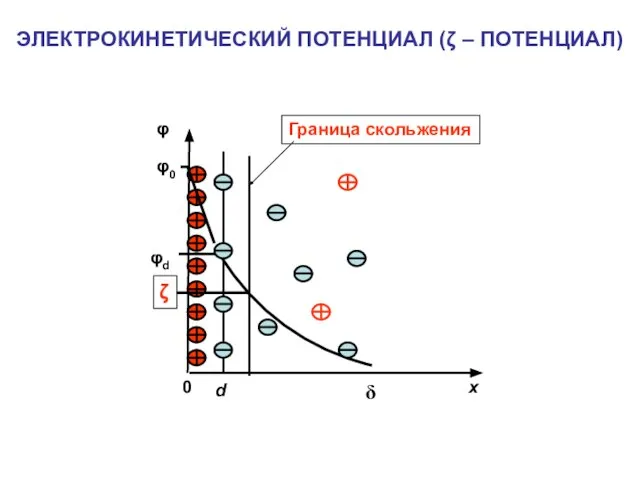
- 16. ЭЛЕКТРОКИНЕТИЧЕСКИЙ ПОТЕНЦИАЛ (ζ – ПОТЕНЦИАЛ)
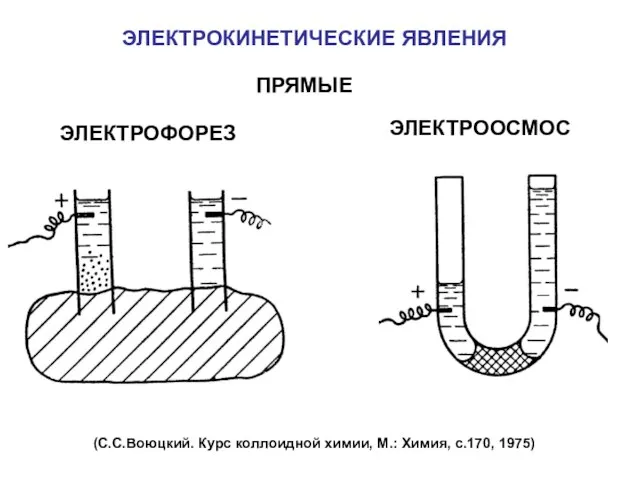
- 17. ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ ЭЛEКТРОФОРЕЗ ЭЛЕКТРООСМОС ПРЯМЫЕ (С.С.Воюцкий. Курс коллоидной химии, М.: Химия, с.170, 1975)
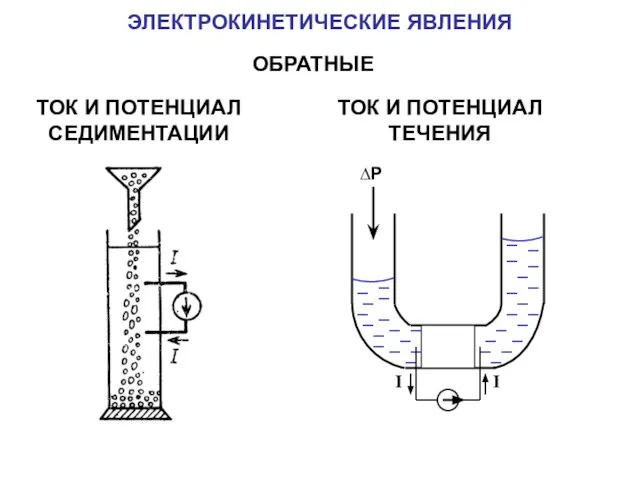
- 18. ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ ОБРАТНЫЕ ТОК И ПОТЕНЦИАЛ СЕДИМЕНТАЦИИ ТОК И ПОТЕНЦИАЛ ТЕЧЕНИЯ
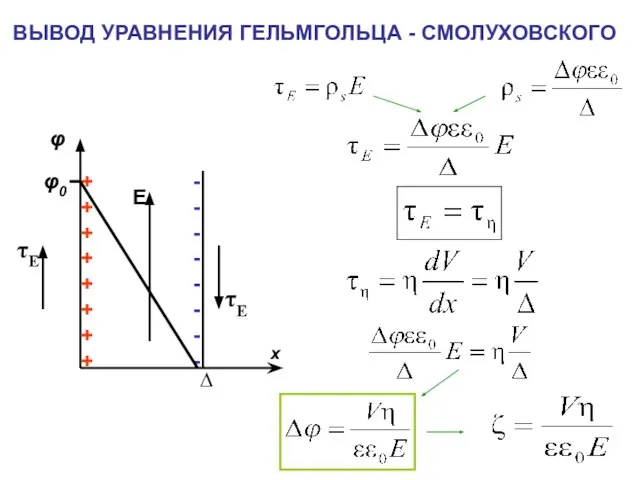
- 19. ВЫВОД УРАВНЕНИЯ ГЕЛЬМГОЛЬЦА - СМОЛУХОВСКОГО
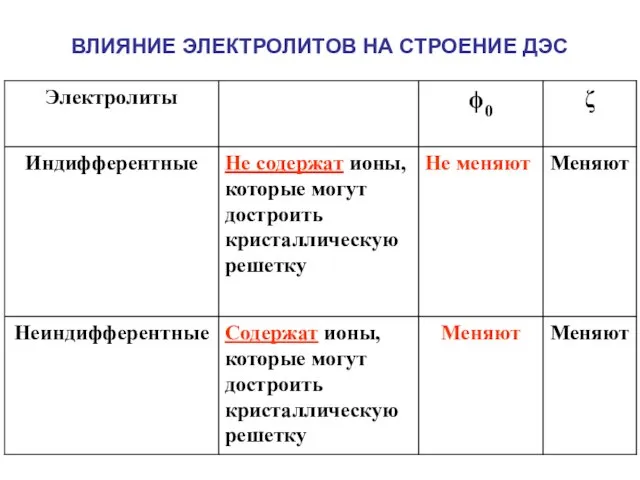
- 20. ВЛИЯНИЕ ЭЛЕКТРОЛИТОВ НА СТРОЕНИЕ ДЭС
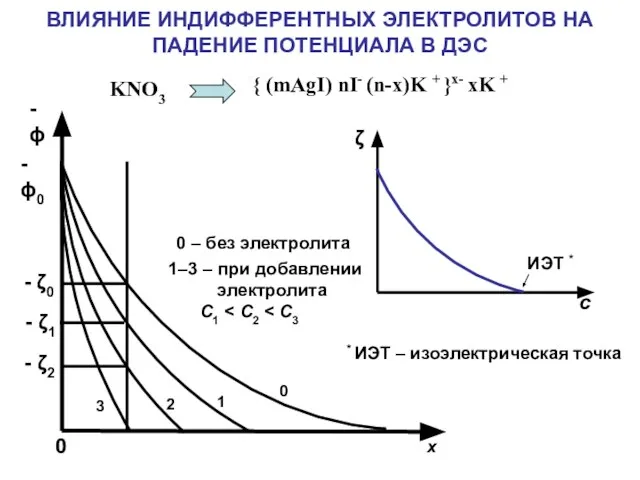
- 21. х - ϕ - ϕ0 0 - ζ0 - ζ1 - ζ2 0 1 2 3
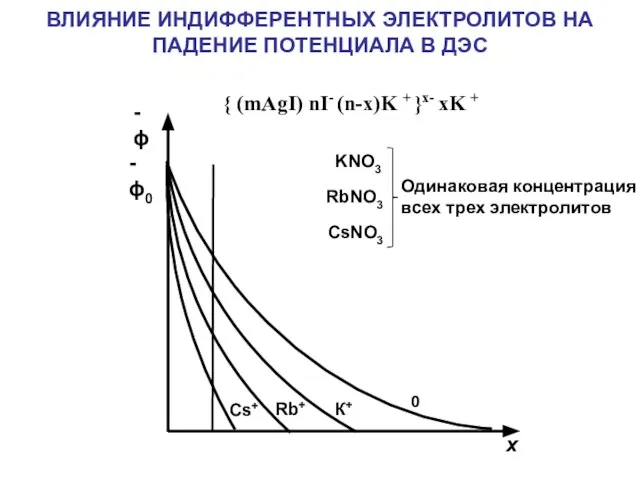
- 22. { (mAgI) nI- (n-x)K + }x- xK + 0 К+ Rb+ Cs+ - ϕ - ϕ0
- 23. ЛИОТРОПНЫЕ РЯДЫ Ряды ионов с убывающей адсорбционной способностью называются лиотропными рядами. Примеры: Одновалентные катионы Cs+ >
- 24. ИОННЫЙ ОБМЕН Уравнение Никольского ci – концентрация в двойном слое аi – активность в растворе Φi
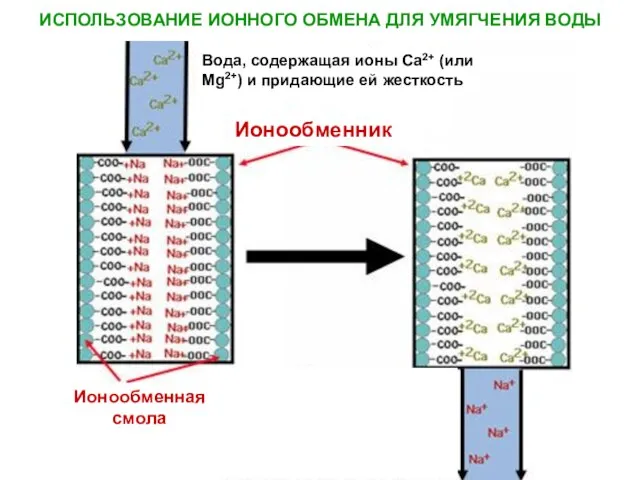
- 25. ИСПОЛЬЗОВАНИЕ ИОННОГО ОБМЕНА ДЛЯ УМЯГЧЕНИЯ ВОДЫ
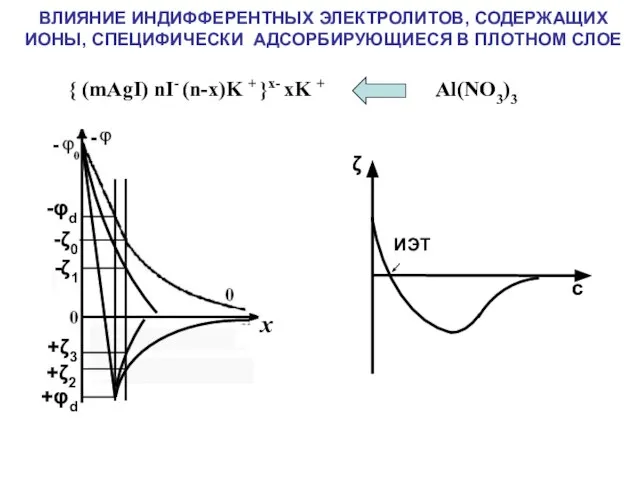
- 26. ВЛИЯНИЕ ИНДИФФЕРЕНТНЫХ ЭЛЕКТРОЛИТОВ, СОДЕРЖАЩИХ ИОНЫ, СПЕЦИФИЧЕСКИ АДСОРБИРУЮЩИЕСЯ В ПЛОТНОМ СЛОЕ -φd +φd -ζ0 +ζ2 { (mAgI)
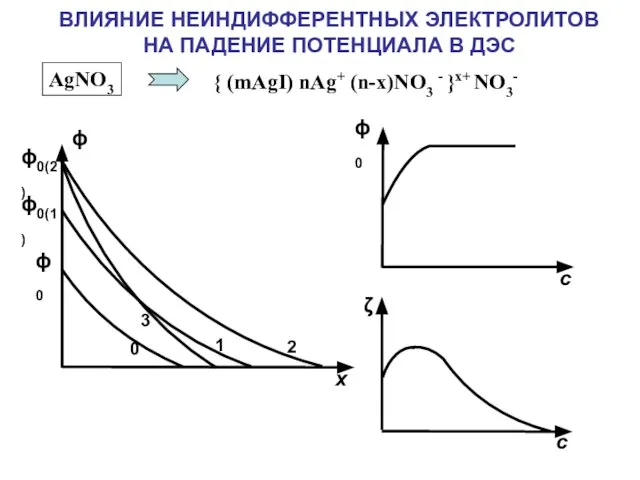
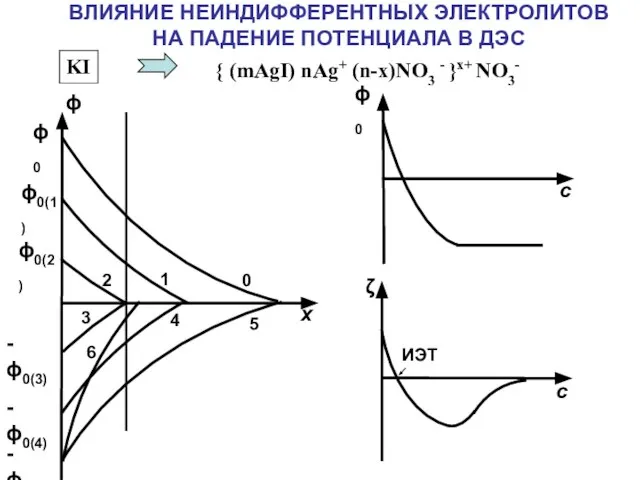
- 27. ВЛИЯНИЕ НЕИНДИФФЕРЕНТНЫХ ЭЛЕКТРОЛИТОВ НА ПАДЕНИЕ ПОТЕНЦИАЛА В ДЭС { (mAgI) nAg+ (n-x)NO3 - }x+ NO3- AgNO3
- 28. 0 1 2 3 4 5 6 ϕ ϕ0 ϕ0(1) ϕ0(2) - ϕ0(3) - ϕ0(4) -
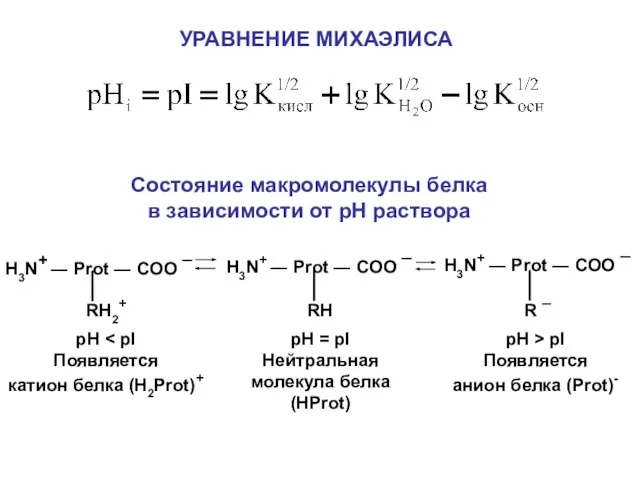
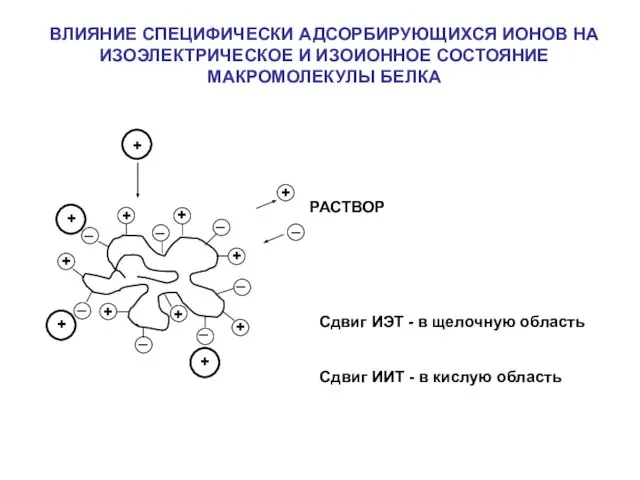
- 29. УРАВНЕНИЕ МИХАЭЛИСА Состояние макромолекулы белка в зависимости от рН раствора
- 30. + + + + + + + _ _ _ _ _ _ _ Сдвиг ИЭТ
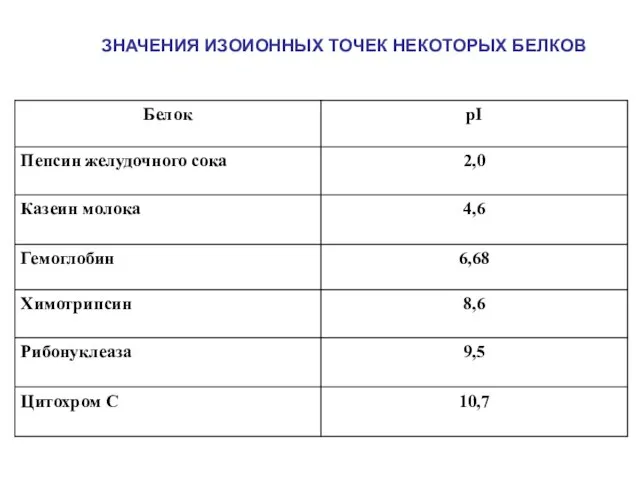
- 31. ЗНАЧЕНИЯ ИЗОИОННЫХ ТОЧЕК НЕКОТОРЫХ БЕЛКОВ
- 32. Электрофорез клеток Клетки позвоночных имеют отрицательный заряд. В гематологии: Аналитический и препаративный клеточный электрофорез: количественная оценка
- 33. Исследование электрофоретической подвижности эритроцитов периферической крови детей. 1. Установлено понижение электрофоретической подвижности эритроцитов периферической крови детей
- 34. ПРИМЕНЕНИЕ ЭЛЕКТРОКИНЕТИЧЕСКИХ ЯВЛЕНИЙ (Д.А.Фридрихсберг. Курс коллоидной химии, Санкт-Петербург: Химия, с.219, 1995) Электрофореграммы плазмы крови человека: здорового
- 36. Скачать презентацию











 Многообразие функций пейзажных описаний в структуре художественного текста
Многообразие функций пейзажных описаний в структуре художественного текста Научно-техническое творчество студентов ЯрГУ в 2015 году: итоги, проблемы, перспективы
Научно-техническое творчество студентов ЯрГУ в 2015 году: итоги, проблемы, перспективы Административная ответственность несовершеннолетних
Административная ответственность несовершеннолетних Лидерство в действии. Миссия, видение, ценности
Лидерство в действии. Миссия, видение, ценности Классификация сварных швов и соединений
Классификация сварных швов и соединений Презентация 27
Презентация 27 Kim Jong-un
Kim Jong-un Оценка текущей ситуации и возможные сценарии развития мировой экономики в 2010-2013 годах
Оценка текущей ситуации и возможные сценарии развития мировой экономики в 2010-2013 годах Тема урока: Екатерина II10 класс
Тема урока: Екатерина II10 класс Метрология, стандартизация и сертификация. Обеспечение качества Обеспечение качества продукции (Тема 1)
Метрология, стандартизация и сертификация. Обеспечение качества Обеспечение качества продукции (Тема 1) Игра Поле чудес
Игра Поле чудес OLAP-анализ данных: решаемые задачи, технологии, актуальные проблемы
OLAP-анализ данных: решаемые задачи, технологии, актуальные проблемы Let’s study english (фотографии)
Let’s study english (фотографии) Особенности развития мотивационной сферы в младшем школьном возрасте
Особенности развития мотивационной сферы в младшем школьном возрасте «Влияние электромагнитных волн на живые организмы»
«Влияние электромагнитных волн на живые организмы» Тепловые машины. Внутренняя энергия – как её использовать?
Тепловые машины. Внутренняя энергия – как её использовать? Тот, кто не знает своего прошлого, не может понять настоящее и предвидеть будущее. Н.М Карамзин
Тот, кто не знает своего прошлого, не может понять настоящее и предвидеть будущее. Н.М Карамзин Организация работы кофейни на 25 посадочных мест
Организация работы кофейни на 25 посадочных мест Театральная декорация
Театральная декорация 1 сентября - День знаний
1 сентября - День знаний Презентация .Уроки безопасности.Как вести при артобстреле
Презентация .Уроки безопасности.Как вести при артобстреле Компания ЮНИТЕКС Департамент офисных перегородок.
Компания ЮНИТЕКС Департамент офисных перегородок. Вернувшийся с войны Кислицин Николай Артемьевич
Вернувшийся с войны Кислицин Николай Артемьевич Воронец Анна АлександровнаСоциальная политика консервативных правительств Великобритании (1979 – 1997 гг.)
Воронец Анна АлександровнаСоциальная политика консервативных правительств Великобритании (1979 – 1997 гг.) 5_urok_svr (1)
5_urok_svr (1) ЧЕРНОВЦЫ
ЧЕРНОВЦЫ Великая Отечественная Война на Кольском Севере
Великая Отечественная Война на Кольском Севере Методы искусственного интеллекта
Методы искусственного интеллекта