Содержание
- 2. Общие свойства ферментов и неорганических катализаторов: Катализируют только термодинамически возможные реакции. Не расходуются в процессе реакции.
- 3. Отличия ферментов от неорганических катализаторов
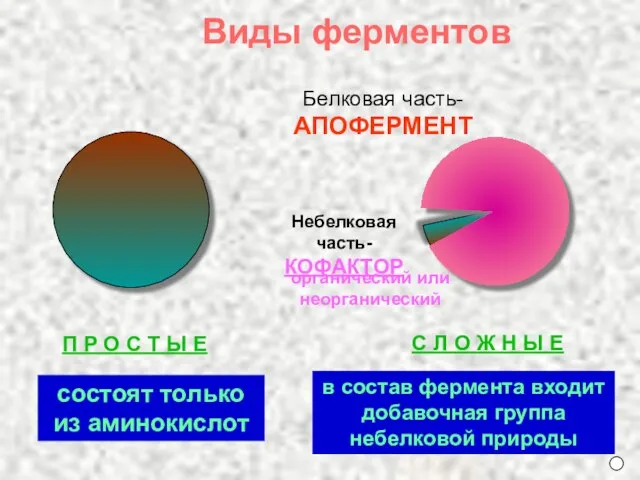
- 4. П Р О С Т Ы Е Белковая часть- АПОФЕРМЕНТ С Л О Ж Н Ы
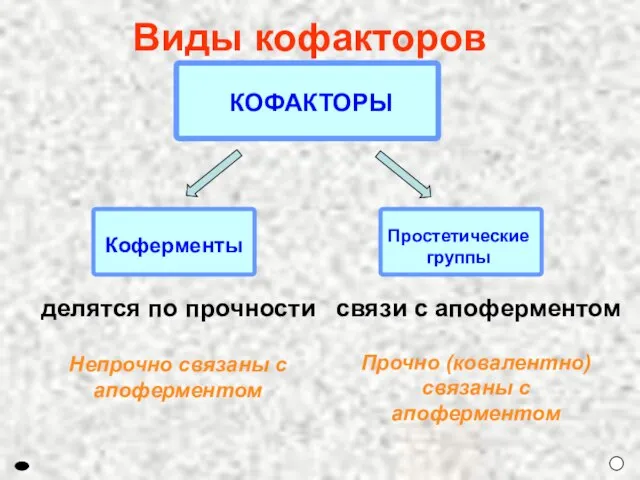
- 5. Непрочно связаны с апоферментом Прочно (ковалентно) связаны с апоферментом Виды кофакторов делятся по прочности связи с
- 6. Активный центр фермента Активный центр – это участок фермента, в котором происходит специфическое связывание субстрата и
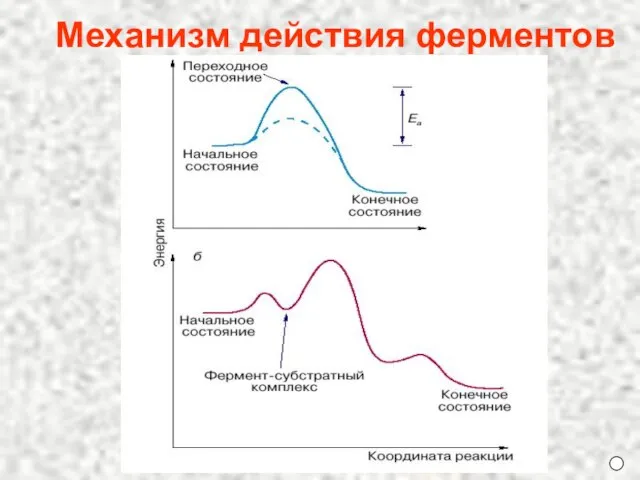
- 7. Механизм действия ферментов
- 8. Факторы, влияющие на каталитическую эффективность ферментов Сближение и ориентация реакционного центра субстрата под каталитическую группу фермента.
- 9. Факторы, влияющие на каталитическую эффективность ферментов Напряжение и деформация, как субстрата, так и фермента, приводящие к
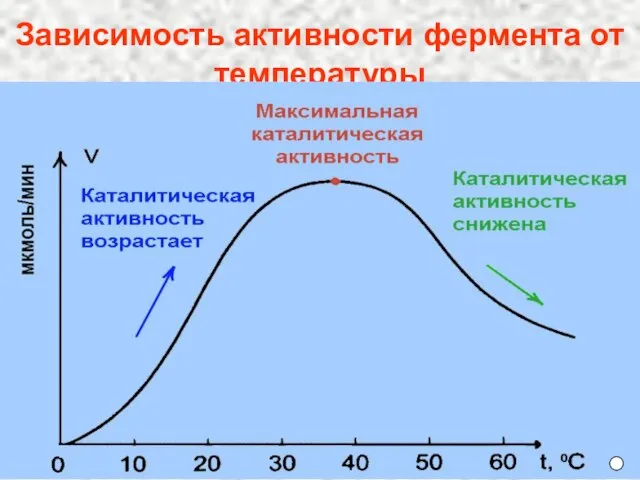
- 10. Зависимость активности фермента от температуры
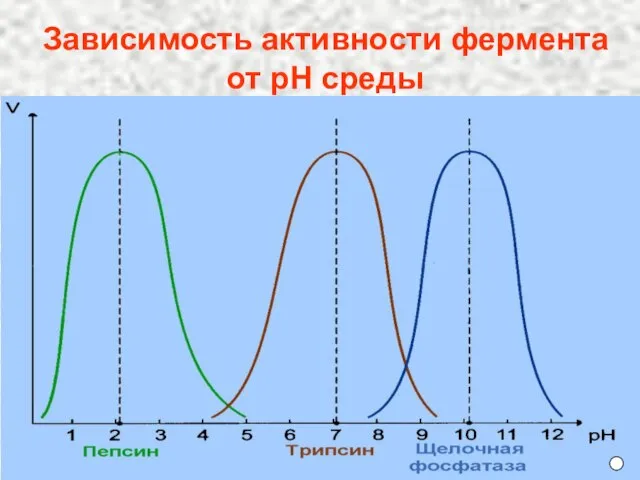
- 11. Зависимость активности фермента от рН среды
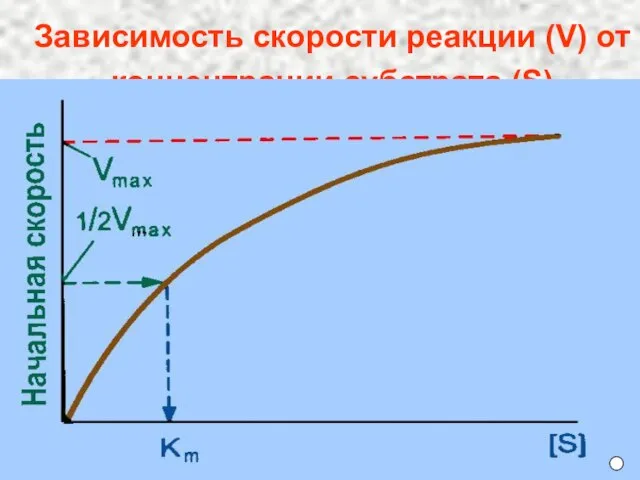
- 12. Зависимость скорости реакции (V) от концентрации субстрата (S)
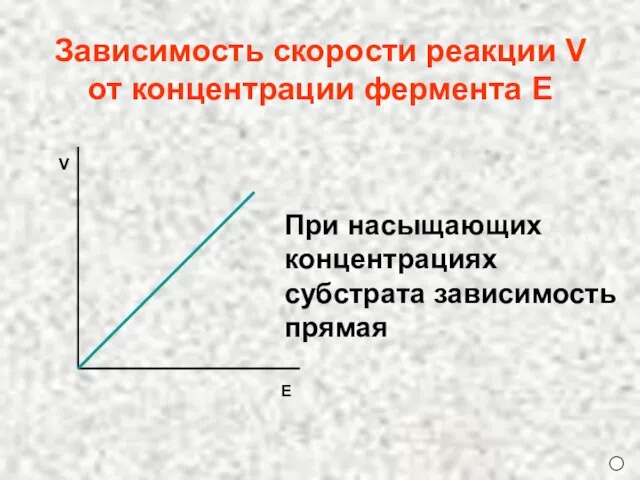
- 13. Зависимость скорости реакции V от концентрации фермента E При насыщающих концентрациях субстрата зависимость прямая V Е
- 14. Определение активности фермента Активность ферментов определяют: по скорости убывания субстрата по скорости накопления продукта
- 15. 1 катал (кат) соответствует такому количеству фермента, которое превращает 1 моль субстрата в 1 с. 1
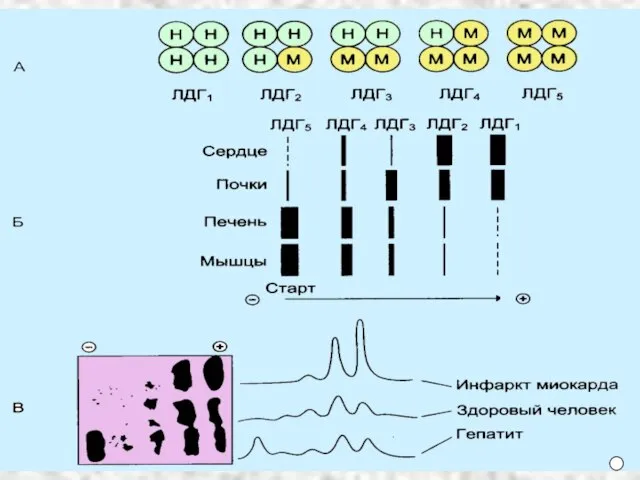
- 16. Изоферменты - это разновидности ферментов, катализирующие одну реакцию, но отличающиеся по своему составу и физико-химическим свойствам.
- 17. Изоферменты различаются 1. По кинетическим параметрам (Vмакс и Км). 2. Тканевой локализации. 3. Электрофоретической подвижности. 4.
- 19. Аллостерический механизм регуляции Регулятор действует на аллостерический центр. Аллостерический центр – это участок фермента, пространственно не
- 20. Изменение химической структуры фермента путем присоединения или отщепления за счет ковалентных связей каких-либо химических групп в
- 21. Химическая или ковалентная модификация Может осуществляться путем: - фосфорилирования - дефосфорилирования; - метилирования - деметилирования; -
- 22. Это процесс отщепления какой-либо части фермента в виде олиго- или полипептида. В результате формируется активный центр.
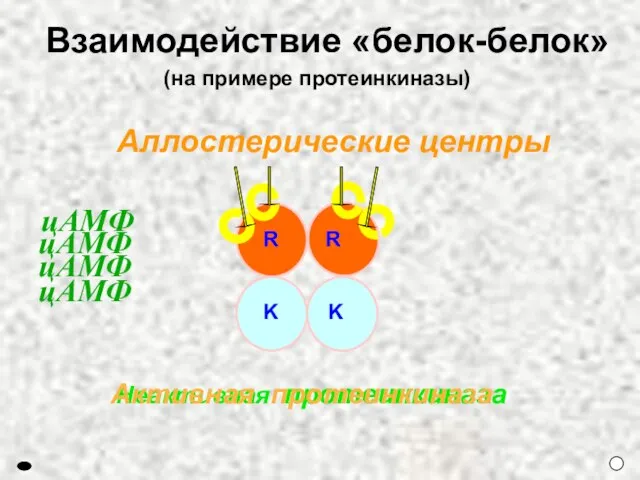
- 23. цАМФ цАМФ Неактивная протеинкиназа Аллостерические центры Взаимодействие «белок-белок» (на примере протеинкиназы) Активная протеинкиназа R R цАМФ
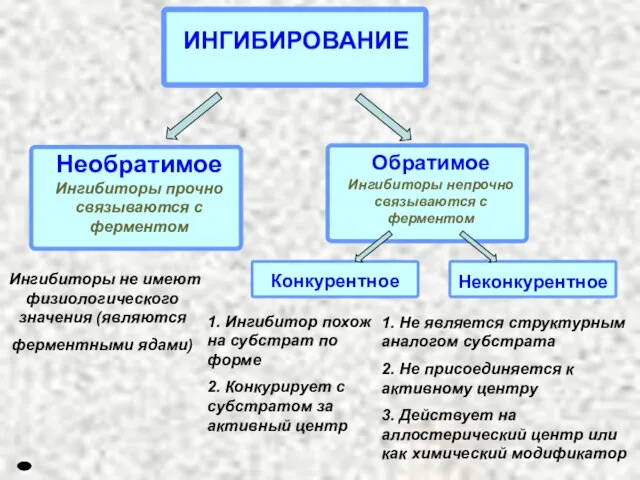
- 24. Ингибиторы не имеют физиологического значения (являются ферментными ядами) ИНГИБИРОВАНИЕ 1. Ингибитор похож на субстрат по форме
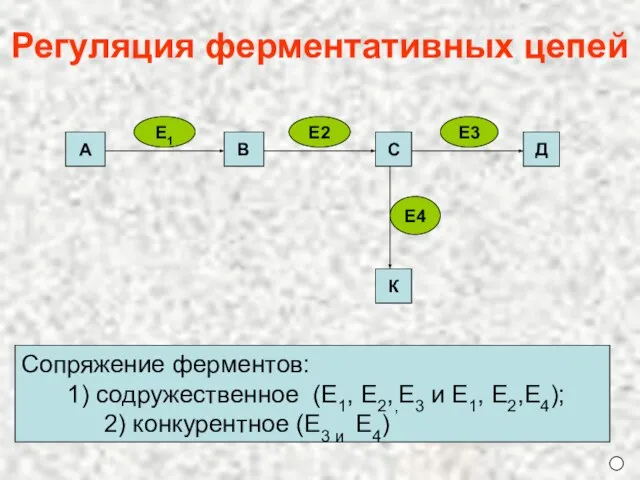
- 25. Сопряжение ферментов: 1) содружественное (Е1, Е2,,Е3 и Е1, Е2,Е4); 2) конкурентное (Е3 и Е4) Регуляция ферментативных
- 26. Ключевыми ферментами являются: а) фермент, стоящий в начале цепи; б) лимитирующий фермент (имеет наименьшую скорость в
- 27. 1. Оксидоредуктазы – катализируют окислительно- восстановительные реакции. 2. Трансферазы – катализируют реакции переноса химических групп. 3.
- 28. Значение ферментов в медицине Энзимо-патология Энзимо-диагностика Изучает значение нарушений активности ферментов в развитии заболеваний. 1. Определение
- 29. Энзимотерапия. Использование ферментов в качестве лекарств: при нарушении пищеварения (фестал, энзистал, креон, мезим-форте и другие); для
- 30. Энзимодиагностика 1. Применение ферментов для определения различных веществ в биологических жидкостях. - глюкозооксидазу используют для определения
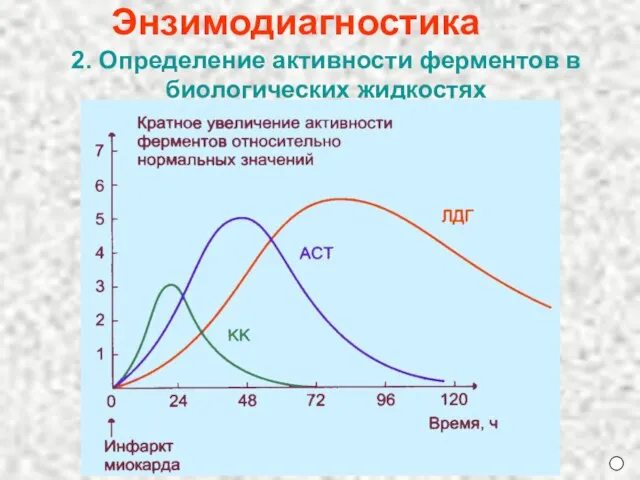
- 31. Энзимодиагностика 2. Определение активности ферментов в биологических жидкостях
- 32. Общие сведения Окисление - это отщепление от вещества электронов; восстановление - это присоединение электронов. Метаболизм -
- 33. Способы передачи электронов Fe2+ + Cu2+ → Fe3+ + Cu+ Прямой перенос электронов: Перенос электронов в
- 34. Отличия биологического окисления от окисления в неживой природе Процесс передачи водорода на кислород происходит поэтапно, через
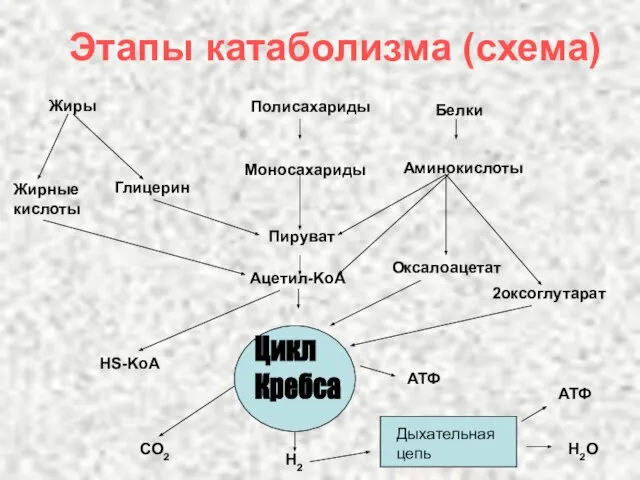
- 35. Этапы катаболизма (схема) Цикл Кребса Дыхательная цепь Жирные кислоты Жиры Полисахариды Белки Моносахариды Аминокислоты Глицерин Пируват
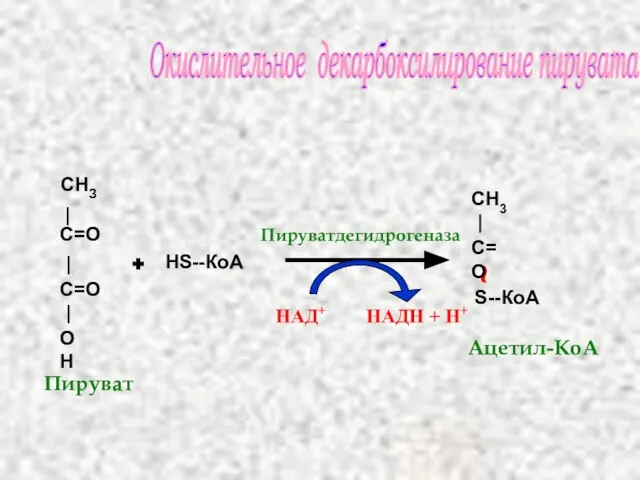
- 36. Окислительное декарбоксилирование пирувата НS--КоА НАД+ НАДН + Н+ Пируватдегидрогеназа + Ацетил-КоА Пируват
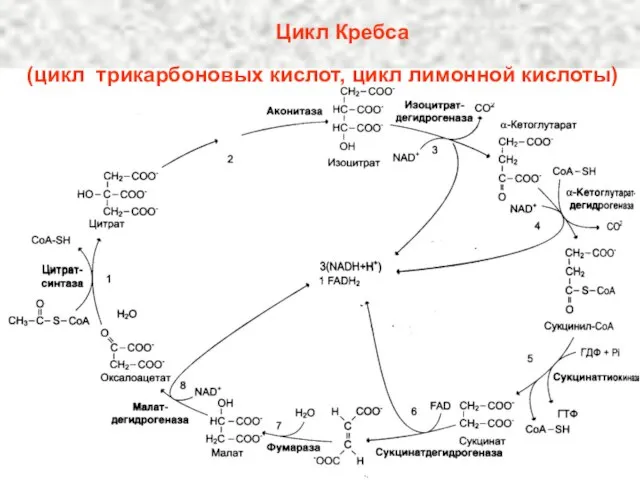
- 37. Цикл Кребса (цикл трикарбоновых кислот, цикл лимонной кислоты)
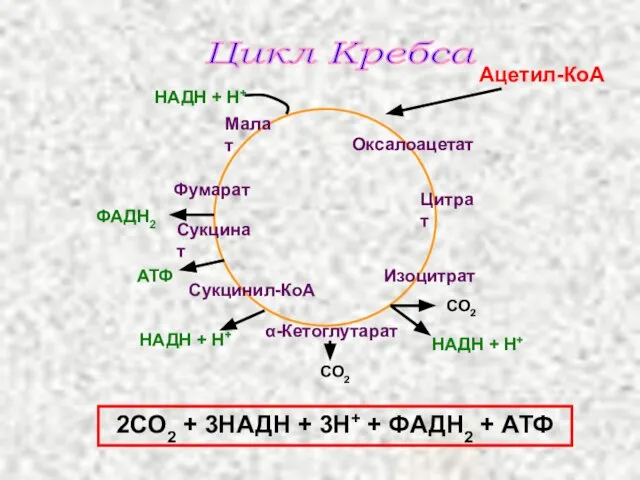
- 38. Ацетил-КоА ФАДН2 Оксалоацетат Малат Цитрат Изоцитрат α-Кетоглутарат Сукцинил-КоА Сукцинат Фумарат НАДН + Н+ АТФ НАДН +
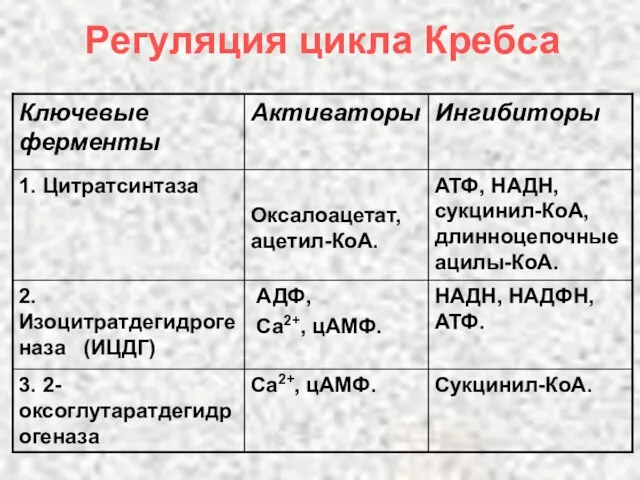
- 39. Регуляция цикла Кребса
- 40. Регуляция цикла Кребса Регуляция гормонами Активируют цикл Кребса: инсулин, катехоламины, глюкагон, йодтиронины.
- 41. Значение цикла Кребса 1. Катаболическое и энергетическое Общий заключительный этап распада всех классов органических соединений Образование
- 42. Значение цикла Кребса 3. Регуляторное (метаболиты - цитрат и АТФ - регуляторы других процессов: активируют синтез
- 43. Дыхательная цепь Дыхательная цепь (цепь переноса электронов) - это цепь сопряженных окислительно-восстановительных реакций, в ходе которых
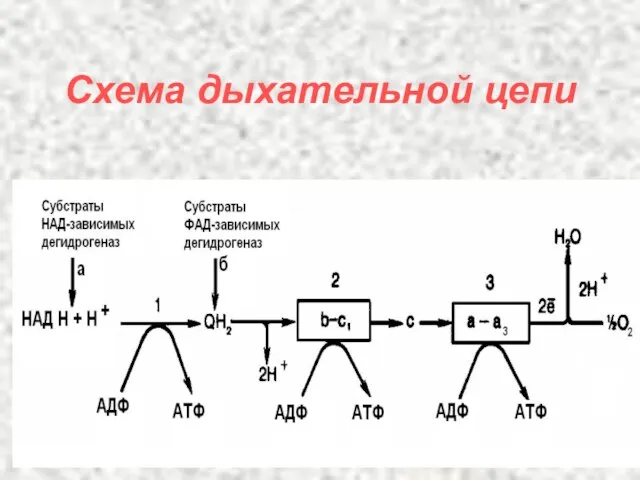
- 44. Схема дыхательной цепи
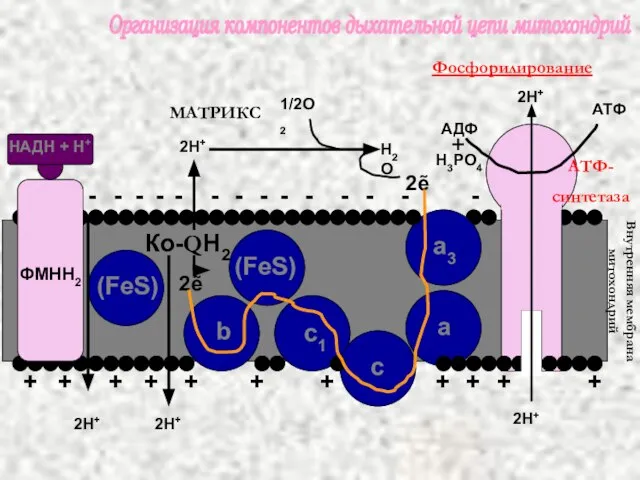
- 45. Организация компонентов дыхательной цепи митохондрий 2ẽ 1/2О2 2ẽ Н2О АТФ 2Н+ 2Н+ 2Н+ 2Н+ 2Н+ АТФ-
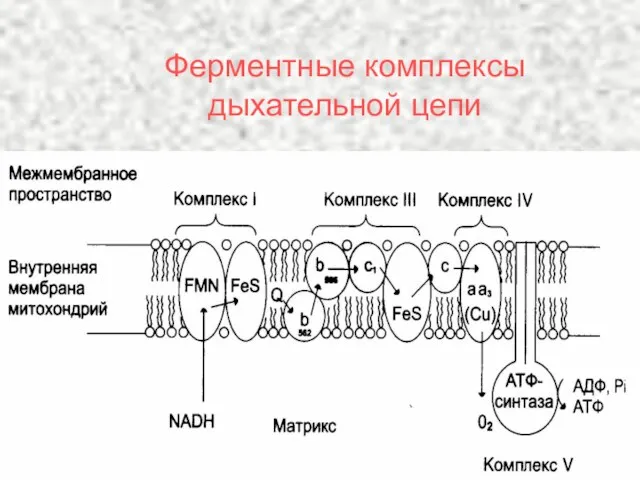
- 46. Ферментные комплексы дыхательной цепи
- 47. Пункты сопряжения окисления и фосфорилирования Синтез АТФ, сопряженный с переносом электронов по дыхательной цепи, называется окислительным
- 48. Пункты сопряжения окисления и фосфорилирования 1. между НАДН и КоQ, 2. на участке цитохромов b -
- 49. Сопряжение и разобщение в дыхательной цепи Сопряжение в дыхательной цепи - это такое состояние, когда окисление
- 50. Сопряжение и разобщение в дыхательной цепи Разобщители: 2,4-динитрофенол яды промышленного производства токсины ионофоры жирные кислоты (естественные
- 51. Регуляция дыхательной цепи АДФ стимулирует работу дыхательной цепи. Это явление называется дыхательным контролем. АТФ тормозит работу
- 52. Блокаторы дыхательной цепи Ротенон блокирует дыхательную цепь на участке НАДН – КоQ. Амитал, антимицин - на
- 53. Нефосфорилирующее (свободное) окисление Это окисление без образования АТФ. Ферменты свободного окисления: - оксидазы, - оксигеназы, -
- 54. Значение свободного окисления: терморегуляция; образование биологически важных соединений (катехоламинов, стероидных гормонов, коллагена, активного витамина Д и
- 55. Тканевые и возрастные особенности окислительных процессов Анаэробные ткани получают энергию без кислорода. Анаэробные ткани: Скелетные мышцы,
- 57. Скачать презентацию


































 Не убивай!
Не убивай! My life
My life Radio
Radio  Презентация на тему Измерение физических величин
Презентация на тему Измерение физических величин Работа с мультимедийным оборудованием: проектор, интерактивная доска, веб-камера, аудио-оборудованиеПериферийное оборудование: п
Работа с мультимедийным оборудованием: проектор, интерактивная доска, веб-камера, аудио-оборудованиеПериферийное оборудование: п Имена прилагательные, близкие и противоположные по смыслу
Имена прилагательные, близкие и противоположные по смыслу Предмет астрономии. Астрономия в древности.
Предмет астрономии. Астрономия в древности. Структурные типы данных
Структурные типы данных ABBYY TestReader 5.2Новое в версии 5.2
ABBYY TestReader 5.2Новое в версии 5.2 Прощай, начальная школа! Здравствуй, 5 класс!
Прощай, начальная школа! Здравствуй, 5 класс! Психология рисунка
Психология рисунка «ДОКУМЕНТЫ НУЖНО НЕ ТОЛЬКО ХРАНИТЬ…»
«ДОКУМЕНТЫ НУЖНО НЕ ТОЛЬКО ХРАНИТЬ…» Подарок. Умей благодарить
Подарок. Умей благодарить Реализация региональных проектов информатизации здравоохранения
Реализация региональных проектов информатизации здравоохранения Mary Jane Ansel
Mary Jane Ansel 1С-Битрикс: Корпоративный портал
1С-Битрикс: Корпоративный портал Презентация на тему Романтизм в музыке
Презентация на тему Романтизм в музыке  RISC V – новая эра процессоров
RISC V – новая эра процессоров Психологические особенности взрослого человека в период поздней взрослости: когнитивные особенности, аффективная сфера
Психологические особенности взрослого человека в период поздней взрослости: когнитивные особенности, аффективная сфера ?????
????? Cоциология поведения экономических агентов на финансовых рынках: роль культуры и социальных институтов
Cоциология поведения экономических агентов на финансовых рынках: роль культуры и социальных институтов Стильная классика Title
Стильная классика Title Интерактивный урок
Интерактивный урок Презентация на тему Культ личности И.В.Сталина
Презентация на тему Культ личности И.В.Сталина  In our region people wear…
In our region people wear… Способы работы с цветом: Гуашь
Способы работы с цветом: Гуашь Юридическое агентство «ЮС КОГЕНС»
Юридическое агентство «ЮС КОГЕНС» Лекарственные растения. Команда Весёлые огородники
Лекарственные растения. Команда Весёлые огородники