Содержание
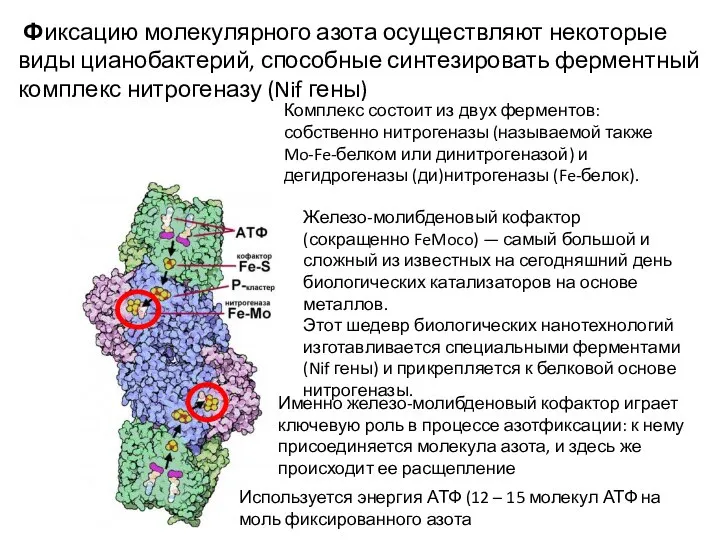
- 2. Комплекс состоит из двух ферментов: собственно нитрогеназы (называемой также Mo-Fe-белком или динитрогеназой) и дегидрогеназы (ди)нитрогеназы (Fe-белок).
- 3. Новые данные (на основе молекулярно-генетических методов): Процесс азотфиксации «стартовал» по крайней мере 3–3,5 млрд лет назад,
- 4. Гетероцисты – результат клеточной дифференциации. Дезактивация ФС2: хл-белковые комплексы и компоненты ФС2 разрушаются (активность ФС1 сохраняется);
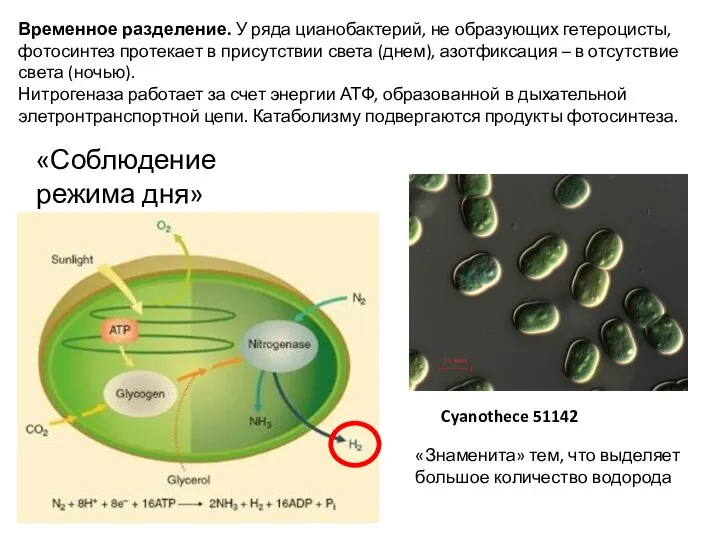
- 5. Cyanothece 51142 Временное разделение. У ряда цианобактерий, не образующих гетероцисты, фотосинтез протекает в присутствии света (днем),
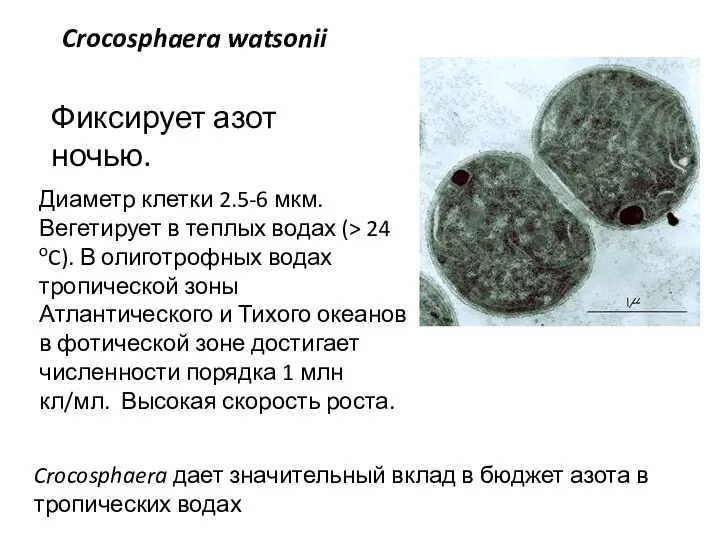
- 6. Диаметр клетки 2.5-6 мкм. Вегетирует в теплых водах (> 24 оC). В олиготрофных водах тропической зоны
- 7. Trichodesmium spp. Цианобактерии Trichodesmium фиксируют азот ТОЛЬКО на свету и при этом у них НЕТ гетероцист
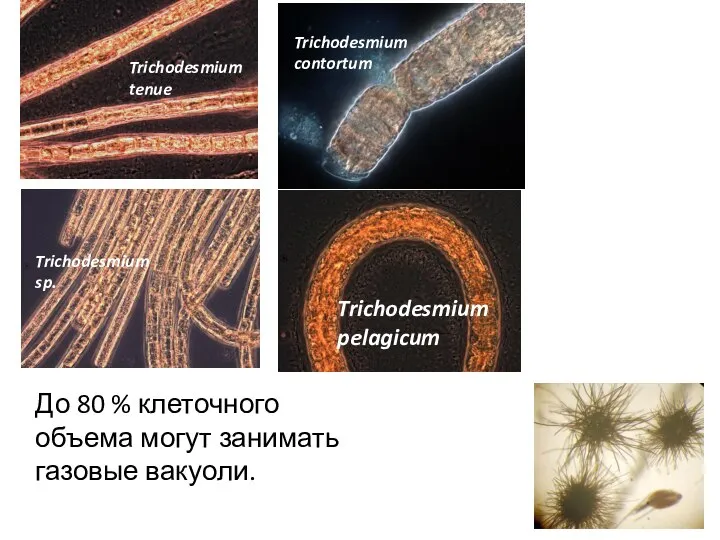
- 8. Trichodesmium tenue Trichodesmium sp. Trichodesmium contortum Trichodesmium pelagicum До 80 % клеточного объема могут занимать газовые
- 9. Как же осуществляется защита нитрогеназ от фотосинтетически выделяемого кислорода у Trichodesmium? Как экспрессия Nif генов, так
- 10. Разделение азотфиксации и фотосинтеза в пространстве у Trichodesmium Окраска специфическим красителем Nif белков Фиксация азота идет
- 11. Разделение азотфиксации и фотосинтеза во времени у Trichodesmium Суточный ритм регулирует транскрипцию nif генов, синтез de
- 12. Способность к фиксации СО2 также снижается в диазоцитах Trichodesmium во время полуденной депрессии, при этом возрастает
- 13. Механизмы предотвращения блокировки нитрогеназ фотосинтетически выделяемым кислородом, ПРЕДПОЛОЖИТЕЛЬНО, также включают: тетразол Формирование в диазоцитах восстановленных зон
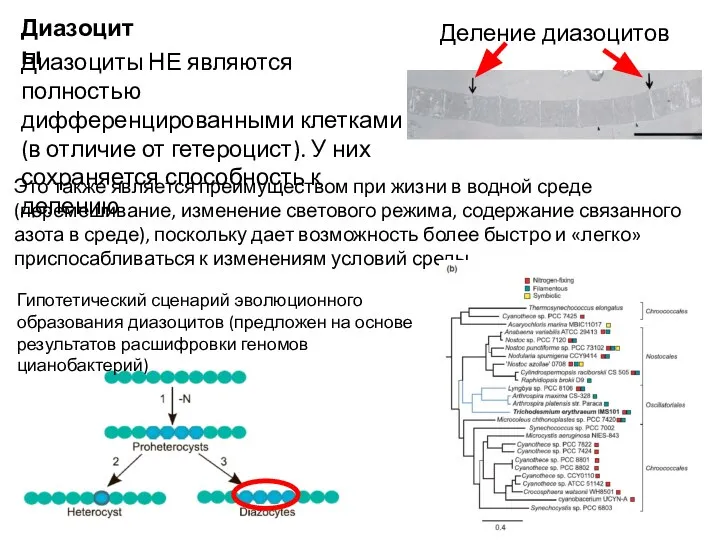
- 14. Гипотетический сценарий эволюционного образования диазоцитов (предложен на основе результатов расшифровки геномов цианобактерий) Диазоциты Диазоциты НЕ являются
- 15. Дальнейшая ассимиляция глутамата, образованного при азотфиксации, происходит в глутаминсинтетазо - глутамин оксоглутарат аминотрансферазном (ГС-ГОГАТ) метаболитном цикле
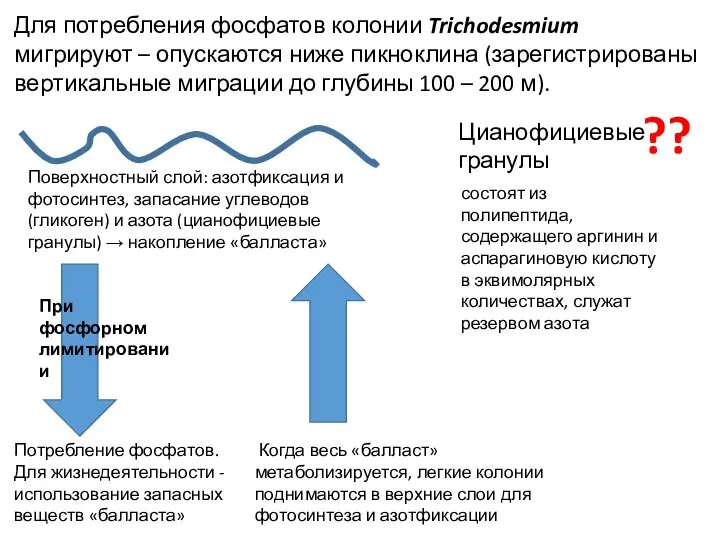
- 16. Для потребления фосфатов колонии Trichodesmium мигрируют – опускаются ниже пикноклина (зарегистрированы вертикальные миграции до глубины 100
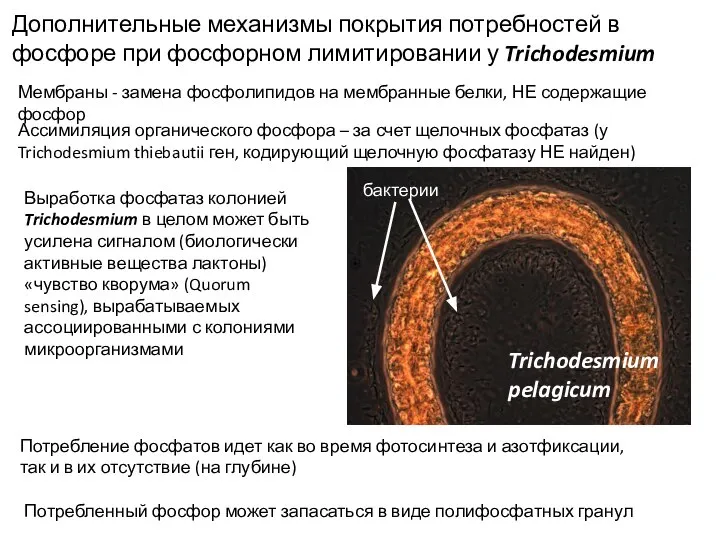
- 17. Дополнительные механизмы покрытия потребностей в фосфоре при фосфорном лимитировании у Trichodesmium Мембраны - замена фосфолипидов на
- 18. Обеспечение потребностей в железе у Trichodesmium В клетках Trichodesmium высокое содержание Fe. Учитывая, что массовое развитие
- 19. Лимитирование недостатком железа ведет к снижению числа диазоцитов и скорости азофиксации А вот фотосинтетическая активность продолжает
- 20. Экосистемная роль Trichodesmium Пределы температурной толерантности для роста и азотфиксации у Trichodesmium: 20 – 34 оС,
- 21. Цветение Trichodesmium. Большой барьерный риф побережья Австралии. Снимок NASA Цветение Trichodesmium. Красное море Снимок NASA Массовое
- 22. Для цветений Trichodesmium характерно как прижизненное выделение значительно количества органического вещества, так и при отмирании клеток
- 23. Это довольно НЕОЖИДАННЫЙ результат, поскольку Trichodesmium синтезирует токсины, вызывающие гибель копепод, таких как Acartia tonsa, а
- 24. Прогнозы динамики Trichodesmium при наблюдаемом климатическом тренде Есть все основания полагать, что повышение температуры и концентрации
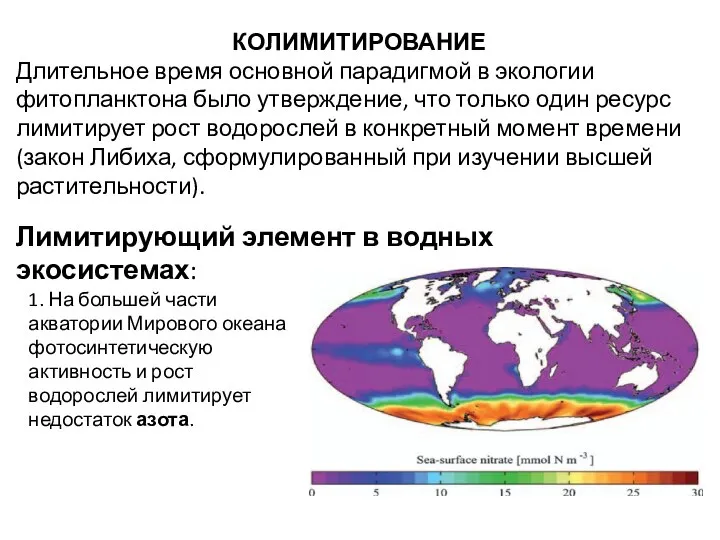
- 25. КОЛИМИТИРОВАНИЕ Длительное время основной парадигмой в экологии фитопланктона было утверждение, что только один ресурс лимитирует рост
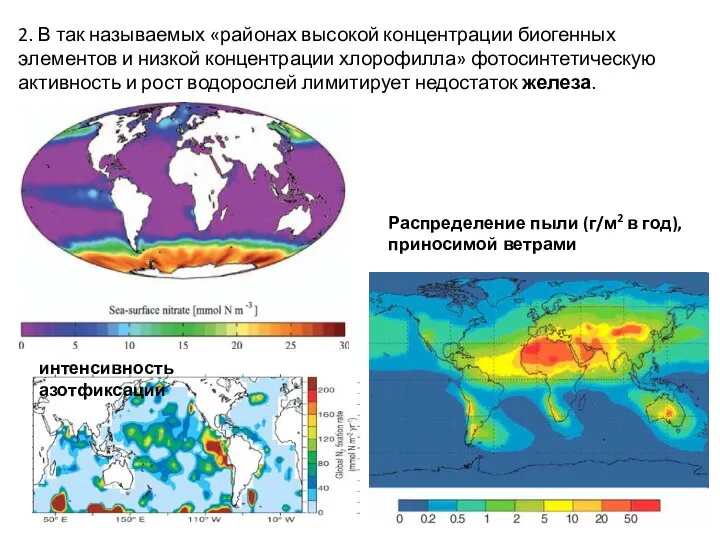
- 26. 2. В так называемых «районах высокой концентрации биогенных элементов и низкой концентрации хлорофилла» фотосинтетическую активность и
- 27. 3. В ряде районов Мирового океана (Северная Атлантика, Средиземное море, Бискайский залив, норвежские фиорды, Белое море)
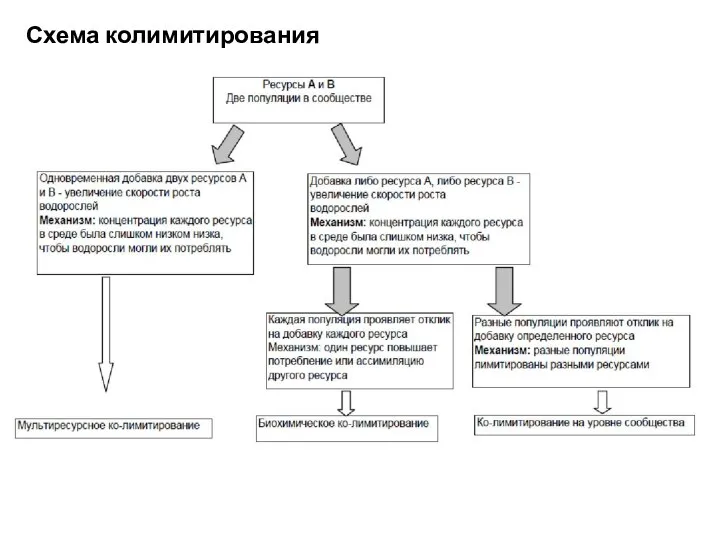
- 28. Мультиресурсное ко-лимитирование. Два ресурса в такой низкой концентрации (ниже порогового уровня), что их потребление уже невозможно.
- 29. Колимитирование на уровне сообщества. Добавка ресурса А стимулирует рост одной популяции, добавка ресурса В стимулирует другую.
- 30. Схема колимитирования
- 31. На следующей лекции: Пространственно-временная изменчивость первичной продукции в Мировом океане Вопросы?
- 33. Скачать презентацию




















 Причины позднего прихода подростка домой
Причины позднего прихода подростка домой Цифровые устройства обработки информации
Цифровые устройства обработки информации Психология менеджмента
Психология менеджмента a
a Птицы: ворона
Птицы: ворона Состав вооружённых сил России
Состав вооружённых сил России 20140212_istoricheskaya_obuslovlennost_sovremennogo_sostoyaniya_prirodnoy_sredy_urala
20140212_istoricheskaya_obuslovlennost_sovremennogo_sostoyaniya_prirodnoy_sredy_urala Предмет, методология и задачи курса
Предмет, методология и задачи курса Разработка и создание интернет - проектов
Разработка и создание интернет - проектов Солнечная активность и информация с космической обсерватории SOHO
Солнечная активность и информация с космической обсерватории SOHO Методы психологии
Методы психологии Презентация на тему Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников
Презентация на тему Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников 5 ЛЕКЦИЯ
5 ЛЕКЦИЯ «Земля – колыбель, но нельзя же вечно жить в колыбели».
«Земля – колыбель, но нельзя же вечно жить в колыбели». Педагогический совет
Педагогический совет Ежегодно команда юношей принимает участиев межрегиональных соревнованиях среди кадетских корпусов, православных гимназий, дет
Ежегодно команда юношей принимает участиев межрегиональных соревнованиях среди кадетских корпусов, православных гимназий, дет Познаём
Познаём Предложение по международной франшизеDollar
Предложение по международной франшизеDollar Право вибору форм здобуття освіти в Україні
Право вибору форм здобуття освіти в Україні Как путешествует письмо? (1 КЛАСС)
Как путешествует письмо? (1 КЛАСС) ФГОС. Федеральный государственный образовательный стандарт
ФГОС. Федеральный государственный образовательный стандарт 20220929_Konstruktionsrückmeldungen_Slawa
20220929_Konstruktionsrückmeldungen_Slawa Тест на тему «Программное обеспечение»
Тест на тему «Программное обеспечение» Пісня, танець, марш переростають у пісенність
Пісня, танець, марш переростають у пісенність Титул
Титул Чемпионат мира по футболу 2018-2022 года – в России
Чемпионат мира по футболу 2018-2022 года – в России Тип губки
Тип губки Виды памяти: назначение, принцип работы
Виды памяти: назначение, принцип работы