Содержание
- 2. Здравствуйте! Здравствуйте, гости дорогие! Чем так опечалены на уроке химии? Расскажите мне скорей: На каком уроке,
- 3. Проверка домашнего задания. По традиции опять Начинаем как обычно Мы «домашку» проверять. Это ведь для нас
- 4. ПРОВЕРОЧНЫЙ ТЕСТ Задание 1: подбери соответствие. 1.Аргентум 2.Аурум 3.Гидраргирум 4.Силициум 5.Натрий 6.Плюмбум 7.Фосфор 8.Кальций 9.Купрум 10.Феррум
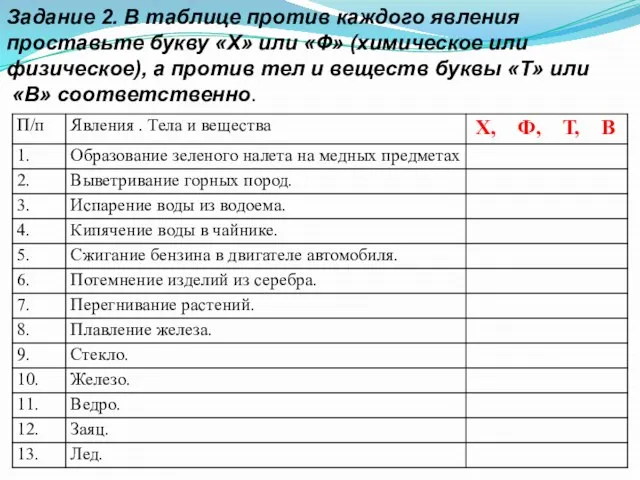
- 5. Задание 2. В таблице против каждого явления проставьте букву «Х» или «Ф» (химическое или физическое), а
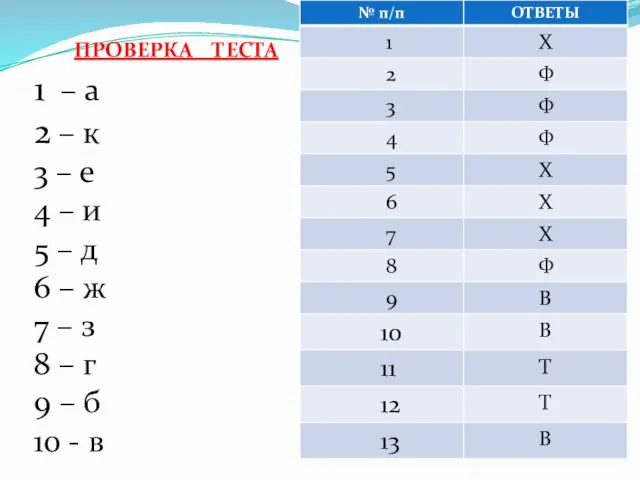
- 6. ПРОВЕРКА ТЕСТА 1 – а 2 – к 3 – е 4 – и 5 –
- 7. Оценки: « 5 » - 20 - 23 балла « 4 » - 16 - 19
- 8. 3.«Формула вещества». Что может формула сказать О разных веществах? Ты сможешь многое узнать, Ведь все в
- 9. ФОРМУЛЫ ВЕЩЕСТВ H - один атом водорода H₂ - одна молекула водорода H₂SO₄ - одна молекула
- 10. Молекул сколько вещества Определишь в момент, Когда внимательно взглянёшь На коэффициент. А где же нам его
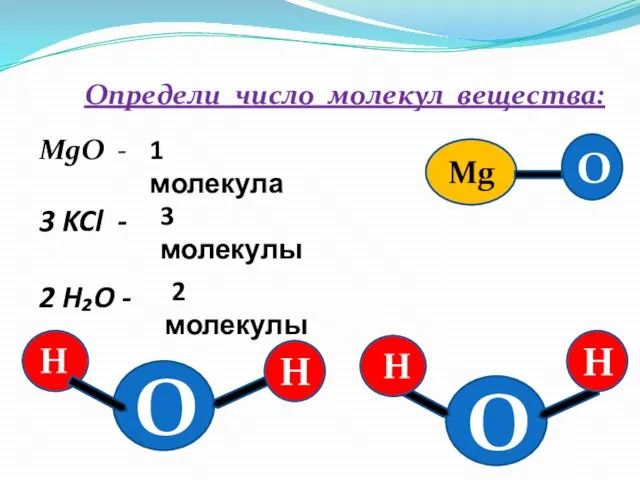
- 11. Определи число молекул вещества: MgO - 3 KCl - 2 H₂O - 1 молекула 3 молекулы
- 12. Число молекул разобрали. А как же с атомами быть? Как нам узнать, что мы не знали:
- 13. Установили разновидность, Давайте дальше продвигаться, Ещё одна необходимость У нас с тобой должна остаться: Какие атомы
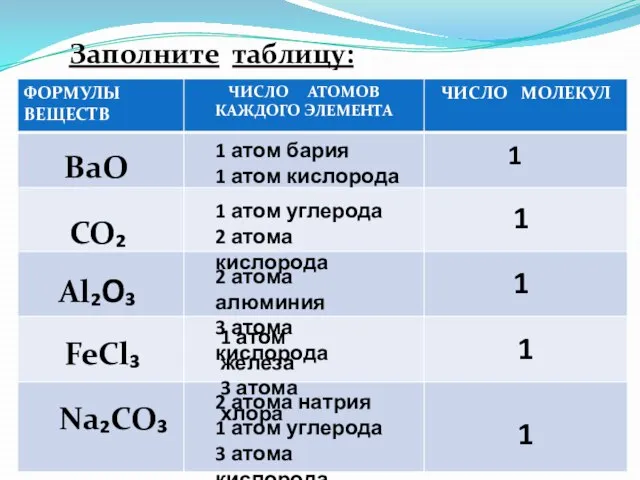
- 14. BaO CO₂ Al₂O₃ FeCl₃ Na₂CO₃ Заполните таблицу: 1 атом бария 1 атом кислорода 1 атом углерода
- 15. Индекс и коэффициент Спутать не так просто, Цифра индекса совсем Маленького роста. А коль молекул много,
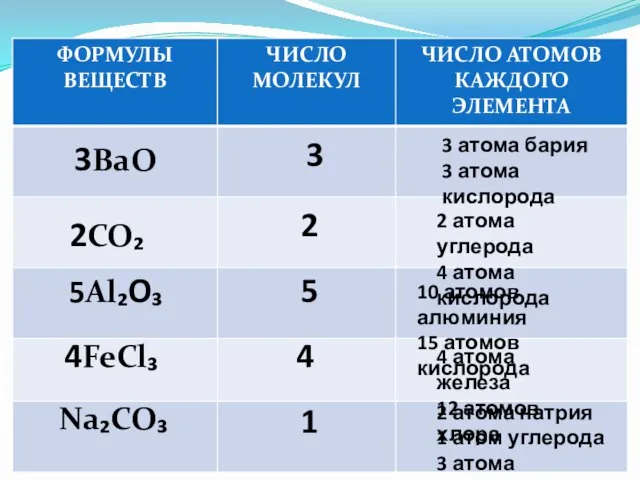
- 16. 3BaO 2CO₂ 5Al₂O₃ 4FeCl₃ Na₂CO₃ 3 2 5 4 1 2 атома натрия 1 атом углерода
- 17. Давайте подведем итог Разобранной тематике, Чтоб каждый без ошибок смог Все формулы внимательно Анализировать, понять И
- 18. 4.Закрепление темы «Формула вещества». Для закрепления теперь Примерчик прорешаем: Два аш-два-эс-о-четыре , Мы всё о ней
- 19. Теперь молекулы считай, Ответ мне правильный давай. - Коэффициент проставлен два. - Соображает голова. Какие атомы
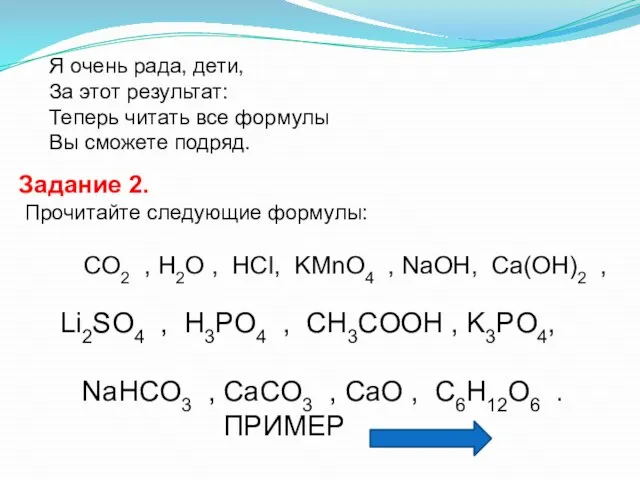
- 20. Я очень рада, дети, За этот результат: Теперь читать все формулы Вы сможете подряд. Задание 2.
- 21. CO2 KМnO4 H3PO4 NaHCO3 C6H12O6 - це-о-два - калий-марганец-о-четыре - аш-три-пэ-о-четыре - натрий-аш-це-о-три - це-шесть-аш-двенадцать-о-шесть
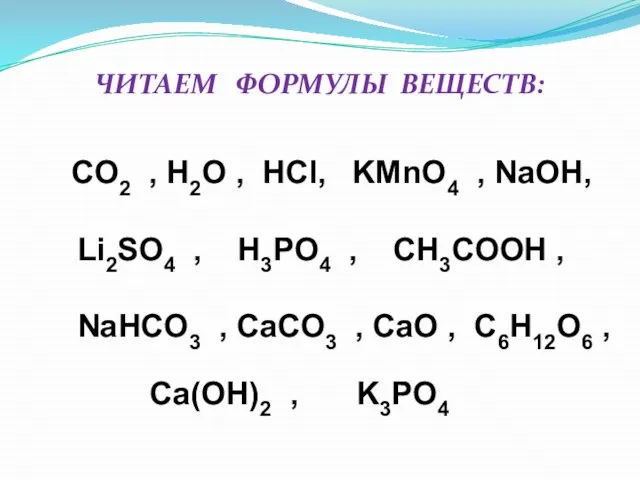
- 22. CO2 , H2O , HCl, KМnO4 , NaOH, Li2SO4 , H3PO4 , CH3COOH , NaHCO3 ,
- 23. 5. «Простые и сложные вещества. Относительная молекулярная масса вещества Все в природе вещества Мы сейчас поделим.
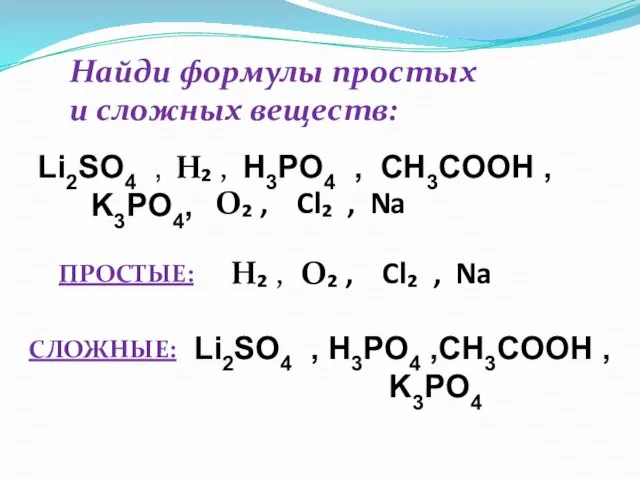
- 24. Найди формулы простых и сложных веществ: Li2SO4 , H3PO4 , CH3COOH , K3PO4, H₂ , O₂
- 25. Масса молекулярная Понятие относительное. Смысл её физический Совсем не удивительный. Массу чтоб молекулы быстренько сравнить, Нужно
- 26. Mr(Na₂O) = 2 · Ar(Na) + Ar(O) = 2 · 23 + 16 = 62 Mr(H₂SO₄)
- 27. 6.Закрепление темы «Простые и сложные вещества. Относительная молекулярная масса вещества». Задание 1. Ниже перечисленные вещества разделите
- 28. 7. Заключительная часть . Ну вот , ребята дорогие, Заканчивается урок. Вы поработали на славу, Трудился
- 29. Ошибку эту я смогу Немедленно исправить. Ну что ж я с вами не прощаюсь, Благодарю всех
- 31. Скачать презентацию




















 Знаковые модели. Моделирование и формализация
Знаковые модели. Моделирование и формализация УРОК ГОРОДА "ГОРОДА-ГЕРОИ"
УРОК ГОРОДА "ГОРОДА-ГЕРОИ" Технологии и инструменты решении проектных задач
Технологии и инструменты решении проектных задач Начальные классы (1-4) система Л.В.Занкова. Программа развивающего обучения.
Начальные классы (1-4) система Л.В.Занкова. Программа развивающего обучения. Эффективные коммуникации
Эффективные коммуникации Кодирование и обработка звуковой информации
Кодирование и обработка звуковой информации Брэйн
Брэйн Пневмонии у детей раннего возраста
Пневмонии у детей раннего возраста Модель Митчелла и Хауса
Модель Митчелла и Хауса Африка
Африка И
И Презентация на тему Сверхпроводимость
Презентация на тему Сверхпроводимость Технология выполнения облицовки поверхностей плитками.
Технология выполнения облицовки поверхностей плитками. ABARUS Market Research
ABARUS Market Research Пруд нашего детства
Пруд нашего детства Восточноукраинский национальный университет им. В. Даля , Луганск, УкраинаОПРЕДЕЛЕНИЯ УДЕЛЬНОЙ ГАММА-АКТИВНОСТИ ПОРОД ШАХТНЫХ
Восточноукраинский национальный университет им. В. Даля , Луганск, УкраинаОПРЕДЕЛЕНИЯ УДЕЛЬНОЙ ГАММА-АКТИВНОСТИ ПОРОД ШАХТНЫХ  Крестьянская реформа 1861 г.
Крестьянская реформа 1861 г. Клуб «Бемби» - школьное лесничество - «Зеленый патруль» - фотостудия - «Марш парков» - сотрудничество с газетой «Эльбрус +»
Клуб «Бемби» - школьное лесничество - «Зеленый патруль» - фотостудия - «Марш парков» - сотрудничество с газетой «Эльбрус +» Управление рисками проекта. Тема 1.6
Управление рисками проекта. Тема 1.6 Презентация на тему Родовые окончания имен существительных
Презентация на тему Родовые окончания имен существительных объединение совладельцев многоквартирных домов- единственный путь реформирования жилищно-коммунального хозяйства города
объединение совладельцев многоквартирных домов- единственный путь реформирования жилищно-коммунального хозяйства города Родительская общественность и органы власти на примере города Магнитогорска
Родительская общественность и органы власти на примере города Магнитогорска Shashki teachvs
Shashki teachvs Размышление учёного мужа, или Смеяться, право, не грешно
Размышление учёного мужа, или Смеяться, право, не грешно Методика: там за поворотом
Методика: там за поворотом Применение ИКТ на уроках в начальной школе
Применение ИКТ на уроках в начальной школе Термообработка стали и чугуна
Термообработка стали и чугуна 22 р.
22 р.