Содержание
- 2. Повторение Определите вид химической связи, составьте электронные формулы образования веществ: NH3, Li3N, Cl2, Na2S, H2S, Mg.
- 3. 5. Какие из приведённых утверждений верны? А. Вещества с молекулярной решёткой имеют низкие температуры плавления и
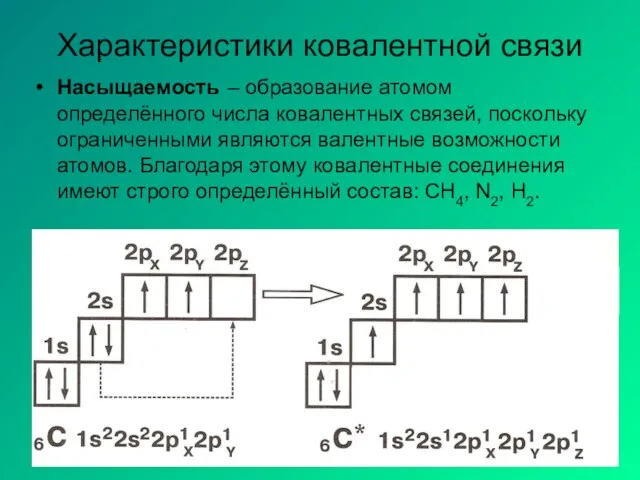
- 4. Характеристики ковалентной связи Насыщаемость – образование атомом определённого числа ковалентных связей, поскольку ограниченными являются валентные возможности
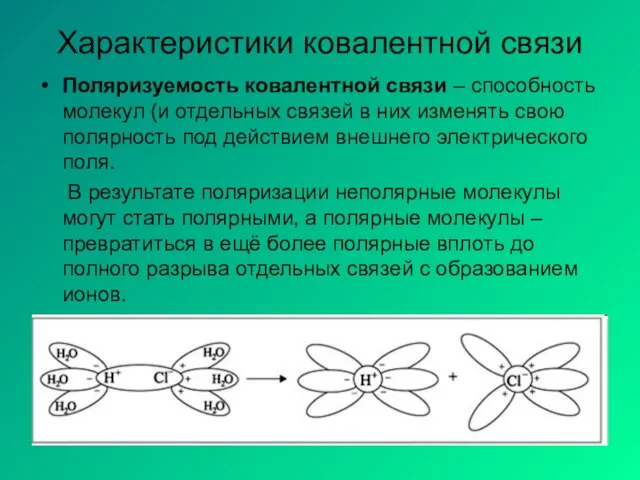
- 5. Характеристики ковалентной связи Поляризуемость ковалентной связи – способность молекул (и отдельных связей в них изменять свою
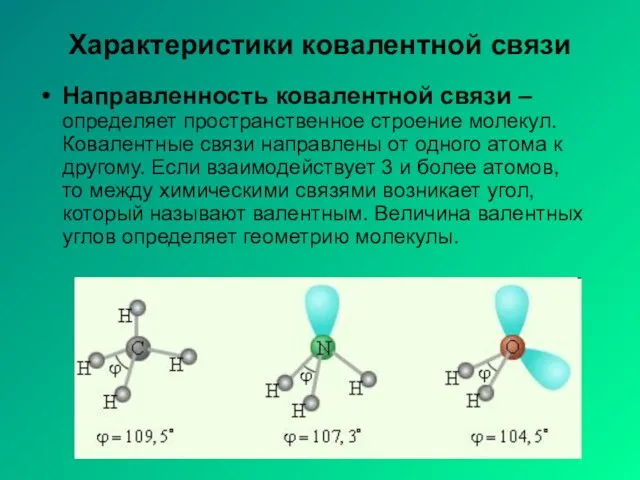
- 6. Характеристики ковалентной связи Направленность ковалентной связи – определяет пространственное строение молекул. Ковалентные связи направлены от одного
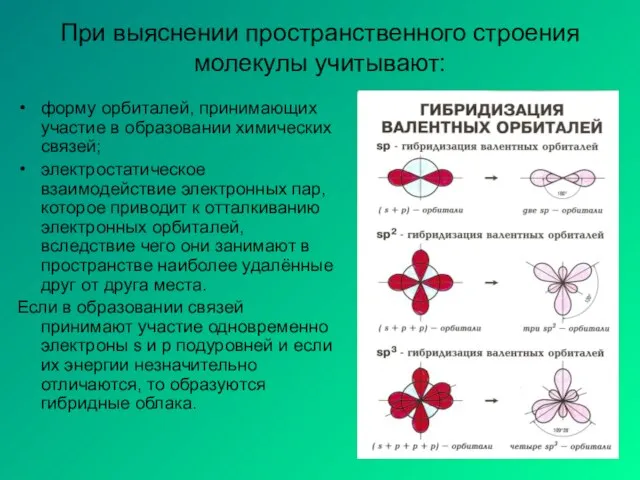
- 7. При выяснении пространственного строения молекулы учитывают: форму орбиталей, принимающих участие в образовании химических связей; электростатическое взаимодействие
- 8. Гибридизация - процесс выравнивания электронных облаков по форме и энергии Основные положения теории гибридизации. Гибридизуются только
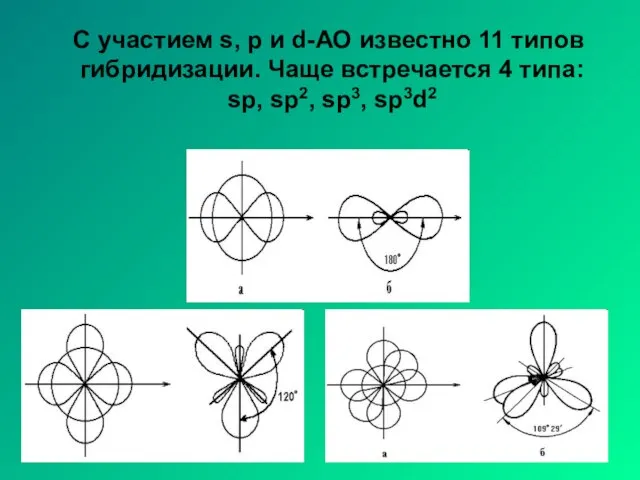
- 9. С участием s, p и d-АО известно 11 типов гибридизации. Чаще встречается 4 типа: sp, sp2,
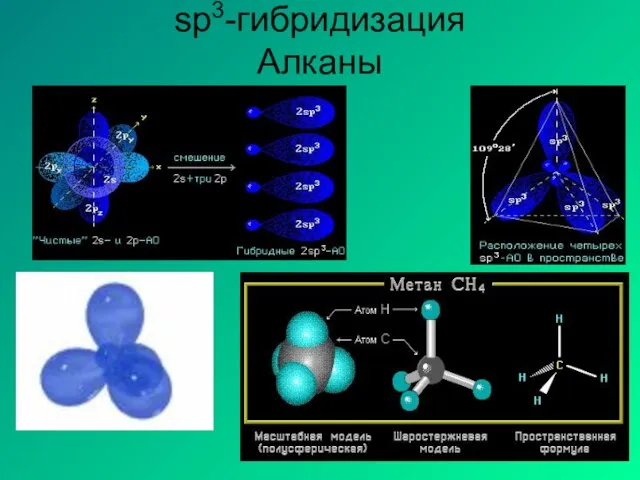
- 10. Определение типа гибридизации на примере молекулы метана. 1.Написать полную структурную формулу вещества. 2.Подсчитать число электронов, предоставляемые
- 11. sp3-гибридизация Алканы
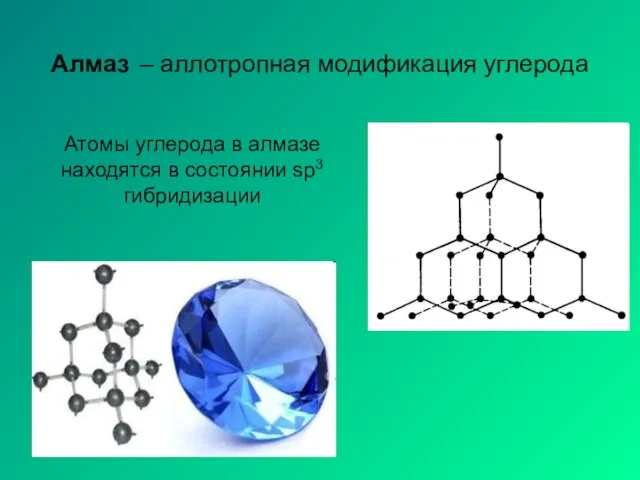
- 12. Алмаз – аллотропная модификация углерода Атомы углерода в алмазе находятся в состоянии sp3 гибридизации
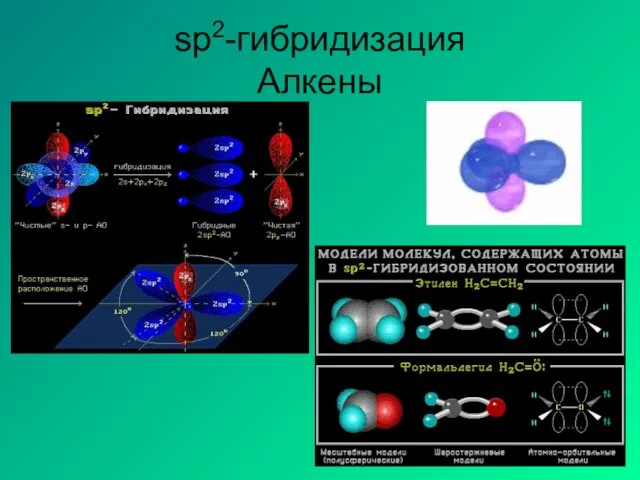
- 13. sp2-гибридизация Алкены
- 14. Графит – аллотропная модификация углерода. Атомы углерода в молекуле графита находятся в состоянии sp2 гибридизации.
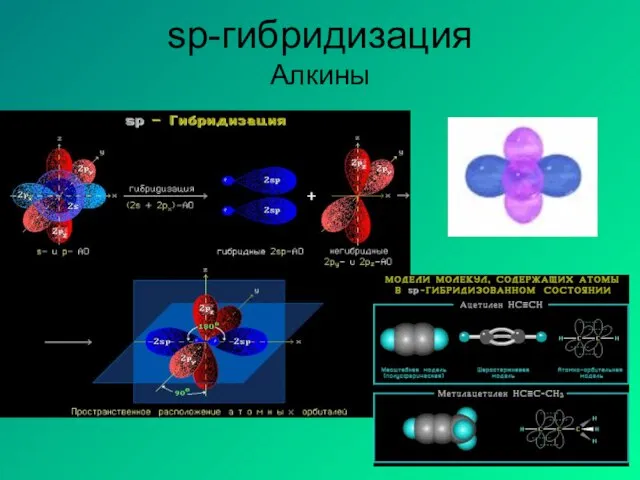
- 15. sp-гибридизация Алкины
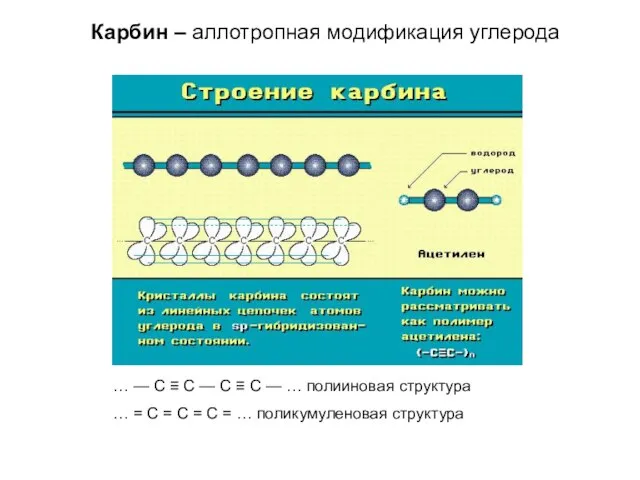
- 16. Карбин – аллотропная модификация углерода … — С ≡ С — С ≡ С — …
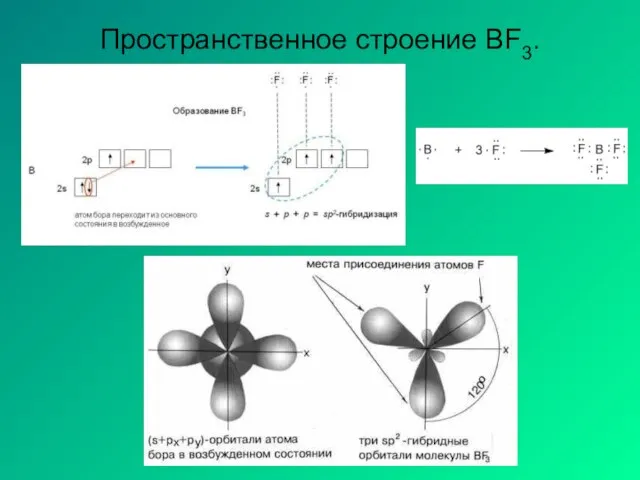
- 17. Пространственное строение BF3.
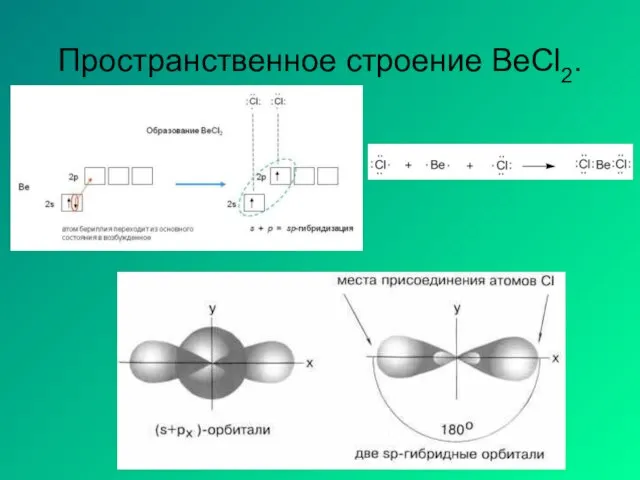
- 18. Пространственное строение BeCl2.
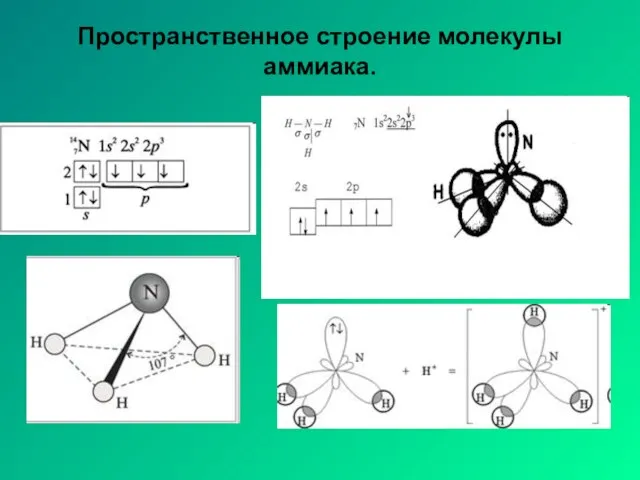
- 19. Пространственное строение молекулы аммиака.
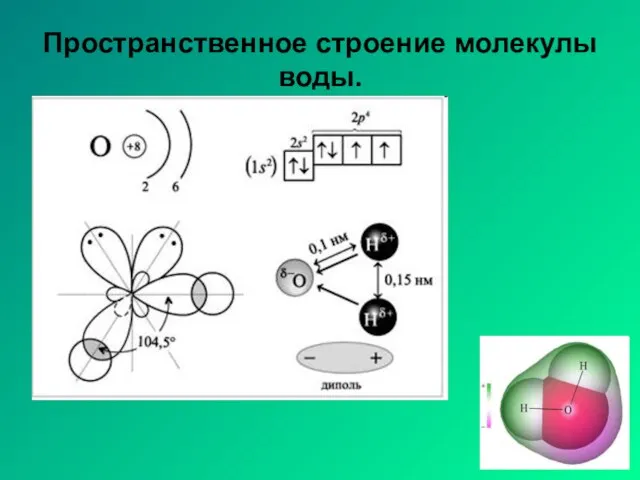
- 20. Пространственное строение молекулы воды.
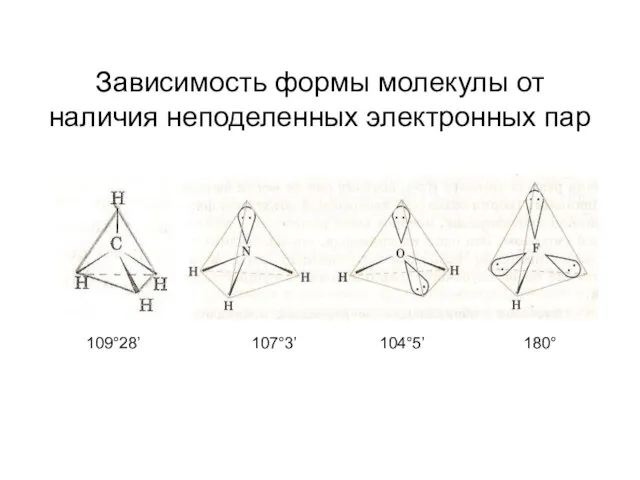
- 21. Зависимость формы молекулы от наличия неподеленных электронных пар 109°28’ 107°3’ 104°5’ 180°
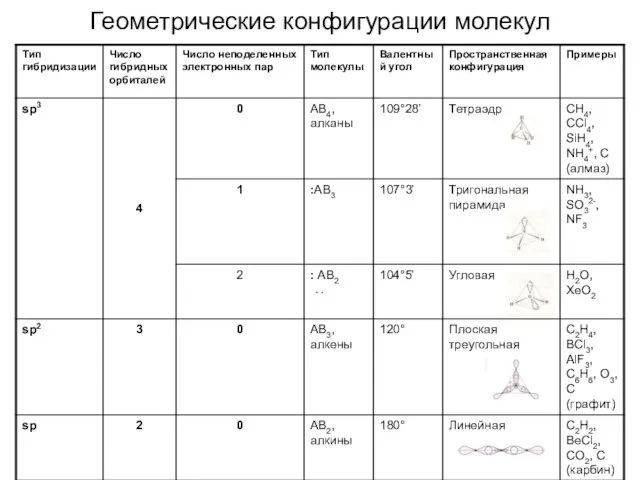
- 22. Геометрические конфигурации молекул
- 23. Вопросы для закрепления Даны формулы веществ: а) C2H4; г) Н2О; ж) С (алмаз); к) C2H2; б)
- 24. 3. Анионы PO43-, SO42-, ClO4- имеют тетраэдрическое строение. Анионы BO33-, CO32-, NO3- имеют форму плоского треугольника.
- 26. Скачать презентацию







 Фитоценозы
Фитоценозы Международный образ Деда Мороза
Международный образ Деда Мороза Пинки Пай
Пинки Пай 2
2 Изобразительное искусство как способ влияния на эмоциональное и физическое состояние человека
Изобразительное искусство как способ влияния на эмоциональное и физическое состояние человека B1
B1 Пальчиковая гимнастика "Ворона и червячки"
Пальчиковая гимнастика "Ворона и червячки" XXVII летняя универсиада в России
XXVII летняя универсиада в России ОБЪЕМНЫЕ МЕТОДЫ АНАЛИЗА
ОБЪЕМНЫЕ МЕТОДЫ АНАЛИЗА Расстройство симпатического и парасимпатического механизмов сердечной деятельности
Расстройство симпатического и парасимпатического механизмов сердечной деятельности Интерактивная раскраска - тренажёр
Интерактивная раскраска - тренажёр Надкласс Рыбы учитель биологии И.И. Иванченко
Надкласс Рыбы учитель биологии И.И. Иванченко Формы обучения персонала
Формы обучения персонала Mathematica
Mathematica Классный час «Поговорим о доброте»
Классный час «Поговорим о доброте» Портрет – (франц, англ.portrait,нем. Bildnis) – жанр изобразительного искусства, посвященный изображению конкретного человека или группы
Портрет – (франц, англ.portrait,нем. Bildnis) – жанр изобразительного искусства, посвященный изображению конкретного человека или группы  Викторина
Викторина Structure and Functions of Biomembranes
Structure and Functions of Biomembranes  Современные информационные технологии в документационном обеспечении управления
Современные информационные технологии в документационном обеспечении управления гмо
гмо Работы учащихся изостудии Зеркало г. Златоуст
Работы учащихся изостудии Зеркало г. Златоуст Подтверждение стажа свидетельскими показаниями
Подтверждение стажа свидетельскими показаниями Арабы
Арабы ПОРТФОЛИО
ПОРТФОЛИО Пластилиновая мастерская А.Веселовой
Пластилиновая мастерская А.Веселовой Плавание, как жизненно важное умение
Плавание, как жизненно важное умение Экзамен
Экзамен Сохраняя традиции вкуса, используя уникальные современные технологии, мы создали для Вас столовые приборы, которые сделают Вашу ж
Сохраняя традиции вкуса, используя уникальные современные технологии, мы создали для Вас столовые приборы, которые сделают Вашу ж