Слайд 2Распространенность металлов в природе
Содержание некоторых металлов в земной коре:
Алюминий 8,2%
Железо 5,0%
Кальций 4,1%
Натрий

2,3%
Магний 2,3%
Калий 2,1%
Слайд 3Распространенность металлов в природе
Содержание некоторых металлов в морской воде:
Na+ 1,05%
Mg 2+ 0,12%

Слайд 4В природе металлы могут встречаться
Только в свободном (самородном) виде (благородные металлы -

золото, платина);
В самородном виде и в виде соединений (металлы малой активности – серебро, медь, ртуть, олово);
Только в виде соединений (металлы, стоящие в ряду напряжений до олова).
Слайд 11Чаще всего металлы встречаются в виде
Солей неорганических кислот
Оксидов

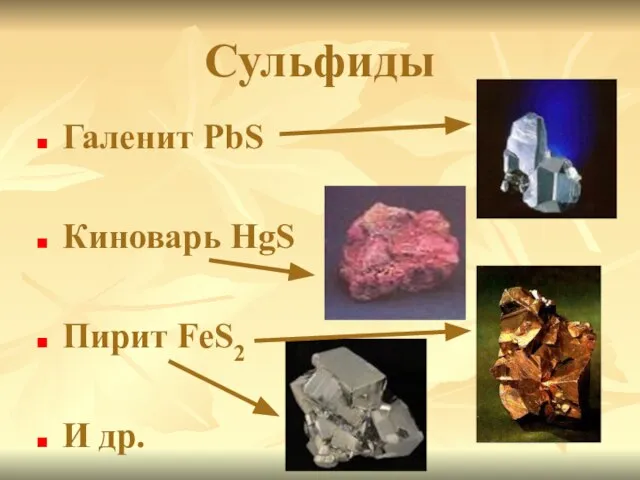
Слайд 12Сульфиды
Галенит PbS
Киноварь HgS
Пирит FeS2
И др.
Слайд 13Хлориды
Сильвин KCl
Галит NaCl
Сильвинит KCl • NaCl
Карналлит
KCl • MgCl2 • 6H2O
И

др.
Слайд 14Сульфаты, фосфаты, карбонаты
Барит BaSO4
Апатит Ca5(PO4)3(F,CI)
Мрамор CaCO3
Магнезит MgCO3
Малахит Cu2(OH)2CO3
И др.

Слайд 15Оксиды
Магнетит Fe3O4
Гематит Fe2O3
Каолин Al2O3 • 2SiO2 • 2H2O
И др.

Слайд 16
Минералы и горные породы, содержащие металлы и их соединения и пригодные для

промышленного получения металлов, называются рудами.
Отрасль промышленности, занимающаяся получением металлов из руд, называется металлургией.
Слайд 181. Пирометаллургия
Восстановление металлов из руд при высоких температурах с помощью восстановителей.
Соль

→ оксид
Соли кислородсодержащих кислот – термическое разложение:
CuCO3 = CuO + CO2
Соли бескислородных кислот- обжиг:
2ZnS + ЗО2 = 2ZnО + 2SО2
Слайд 19Восстановление углем или угарным газом:
CuO + C → Cu + CO
CuO +

CO → Cu + CO2
Водородотермия:
Cr2O3 + H2 → Cr + H2O
Металлотермия:
Fe2O3 + Al → Fe + Al2O3
t
t
t
t
Слайд 202. Гидрометаллургия
Получение металлов из растворов их солей.
Перевод нерастворимого соединения в раствор:
CuO +

H2SO4 = CuSO4 + H2O
Восстановление металла из раствора:
CuSO4 + Fe = FeSO4 + Cu.
Слайд 21Электрометаллургия – это способы получения металлов с помощью электрического тока (электролиза).
2NaCl

→ 2Na + Cl2
MgBr2 → Mg + Br2
Микробиологические методы получения металлов.



















 Общий анализ сложившейся правоприменительной практики арбитражных судов в условиях COVID-19
Общий анализ сложившейся правоприменительной практики арбитражных судов в условиях COVID-19 «Свободная цена»: решение для независимых музыкантов и НКО
«Свободная цена»: решение для независимых музыкантов и НКО Образование болот
Образование болот Прием переписного персонала
Прием переписного персонала Инфекционные болезни 4
Инфекционные болезни 4 Геометрические фигуры 4 класс
Геометрические фигуры 4 класс Профессиональные функции и умения старшего воспитателя ДОУ
Профессиональные функции и умения старшего воспитателя ДОУ История причёсок
История причёсок Информация по экологии
Информация по экологии Цицерон - философ Древнего Рима
Цицерон - философ Древнего Рима Unit 1 Speaking about seasons and weather
Unit 1 Speaking about seasons and weather “Привлечение общественности и поддержка гражданского общества в реализации Орхуской конвенции” EuropeAid/122449/C/SER/Multi
“Привлечение общественности и поддержка гражданского общества в реализации Орхуской конвенции” EuropeAid/122449/C/SER/Multi ЭЛЕКТРОННЫЙ ЖУРНАЛ ПЕДАГОГА
ЭЛЕКТРОННЫЙ ЖУРНАЛ ПЕДАГОГА Орфография. Морфемика. Словообразование
Орфография. Морфемика. Словообразование Открытый урок по теме: ДНК-носитель генетического материала.
Открытый урок по теме: ДНК-носитель генетического материала. КАФЕДРА УПРАВЛЕНИЯ И ЗАЩИТЫ В ЧРЕЗВЫЧАЙНЫХ СИТУАЦИЯХ
КАФЕДРА УПРАВЛЕНИЯ И ЗАЩИТЫ В ЧРЕЗВЫЧАЙНЫХ СИТУАЦИЯХ Свобода в деятельности человека
Свобода в деятельности человека Сенсорная характеристика как составляющая качества продуктов. Лекция 1
Сенсорная характеристика как составляющая качества продуктов. Лекция 1 Освободительная война в Нидерландах
Освободительная война в Нидерландах  пицца
пицца Софизмы.
Софизмы. Бактерии в жизни человека
Бактерии в жизни человека Программирование на языке Q Basic
Программирование на языке Q Basic Путешествие по Вселенным. Часть 1
Путешествие по Вселенным. Часть 1 Психологическая подготовка боксеров-юношей
Психологическая подготовка боксеров-юношей Как разрушить жизнь, когда вы молоды
Как разрушить жизнь, когда вы молоды Теологическая парадигма: И. Т. Посошков – аргументы в пользу правого суда
Теологическая парадигма: И. Т. Посошков – аргументы в пользу правого суда Презентация на тему Как вести себя в транспорте
Презентация на тему Как вести себя в транспорте