Содержание
- 2. Содержание Эволюция взглядов на строение вещества. Основные понятия и определения молекулярно-кинетической теории : Молекулярная физика Макроскопические
- 3. Еще задолго до нашей эры, в период расцвета древних культур, возникло учение о мельчайших частицах, из
- 4. Древнегреческие философы Анаксагор и Демокрит (в IV веке до нашей эры) считали, что любое вещество состоит
- 5. Взаимодействуют атомы давлением и ударом. Воззрения Демокрита, весьма далекие от современных, сыграли очень важную роль в
- 6. Атомисты считали, что разнообразие веществ, имеющихся в природе, объясняется не разнообразием различных сортов атомов, но разнообразием
- 7. Эпоха средневековья не продвинула вперед учение об атомах и молекулах. В XVII столетии, когда были заложены
- 8. Этим вращательным движением Ломоносов объяснил тепловые явления. Он утверждал, что «должна существовать наибольшая степень холода, состоящая
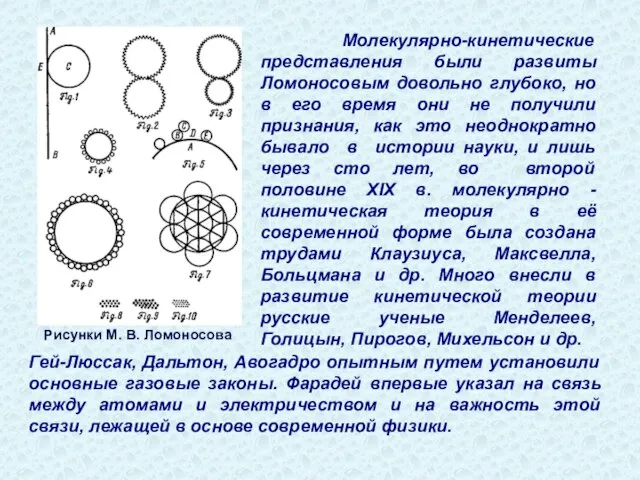
- 9. Рисунки М. В. Ломоносова Молекулярно-кинетические представления были развиты Ломоносовым довольно глубоко, но в его время они
- 10. Свойства вещества, которые обусловлены его молекулярным строением, изучает Молекулярная физика – раздел физики, в котором рассматриваются
- 11. Цель молекулярно-кинетической теории – объяснение свойств макроскопических тел и закономерностей тепловых процессов на основе представлений о
- 12. Макроскопические тела (от греч. «макрос» – большой) - это все тела, которые нас окружают: дома, машины,
- 13. Все вещества состоят из молекул и атомов. Молекула – наименьшая электронейтральная частица вещества, сохраняющая его свойства.
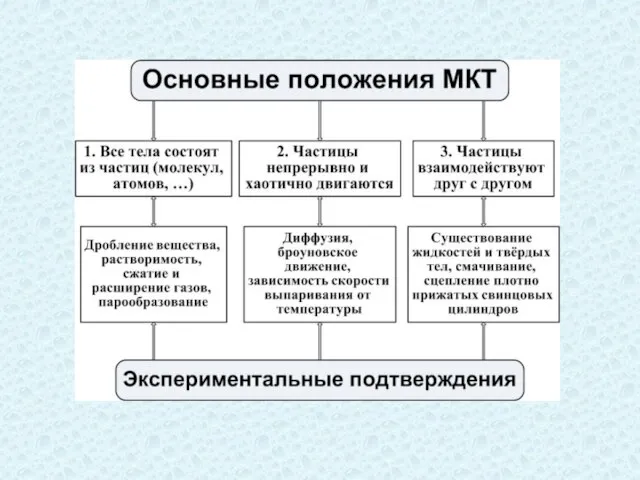
- 15. Каждое из положений МКТ строго доказано исследовательским путём. Реальное существование молекул подтверждается экспериментально. В качестве примеров
- 16. Платина в электронном микроскопе Молекулы нафталина в ионном микроскопе Изображение предварительно отполированной, а затем подвергнутой ионной
- 17. Сканирующий электронно-ионный микроскоп. Ионный микроскоп JEM-ARM200F Рассказ про ионный микроскоп здесь Ионный микроскоп - электронно-оптический прибор,
- 18. Ионный микроскоп
- 19. Наиболее убедительными доказательствами реального существования молекул являются броуновское движение и диффузия. БРОУНОВСКОЕ ДВИЖЕНИЕ
- 20. Это явление открыто Р. Броуном в 1827 г., когда он проводил исследования пыльцы растений. Шотландский ботаник
- 21. Последовательные положения через каждые 30 секунд трех броуновских частиц – шариков гуммигута размером около 1 мкм.
- 22. Объяснить броуновское движение невозможно, если не предположить, что молекулы воды находятся в беспорядочном, никогда не прекращающемся
- 23. Броуновское движение
- 24. Диффузия Для наблюдения явления диффузии бросим несколько крупинок краски в высокий сосуд с водой. Они опустятся
- 25. Существование жидкостей и твёрдых тел, газов Агрегатное состояние — состояние вещества, характеризующееся определёнными качественными свойствами, например,
- 26. Газ стремится занять весь объём, ему предоставленный. Атомы или молекулы газа ведут себя относительно свободно, расстояния
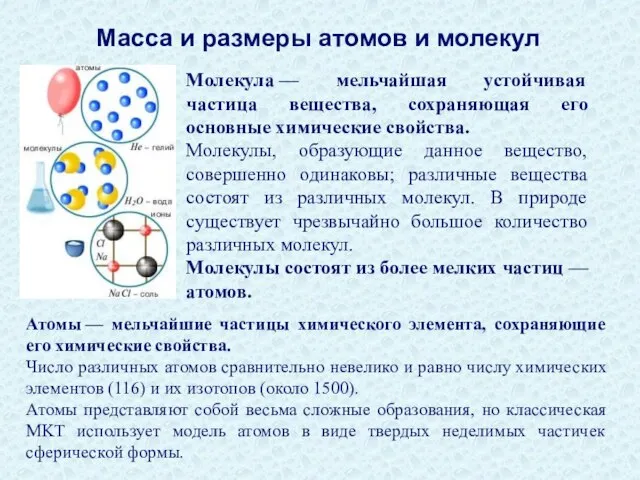
- 27. Молекула — мельчайшая устойчивая частица вещества, сохраняющая его основные химические свойства. Молекулы, образующие данное вещество, совершенно
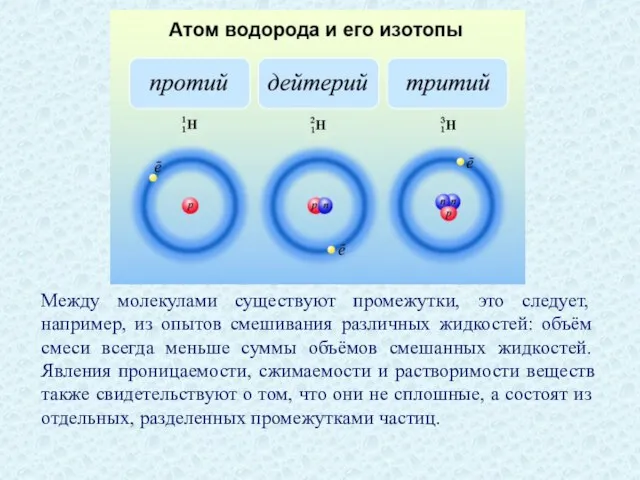
- 28. Между молекулами существуют промежутки, это следует, например, из опытов смешивания различных жидкостей: объём смеси всегда меньше
- 29. Несколько интересных фактов: ... разведя 1 мл чернил в 1 л воды, а затем 1 мл
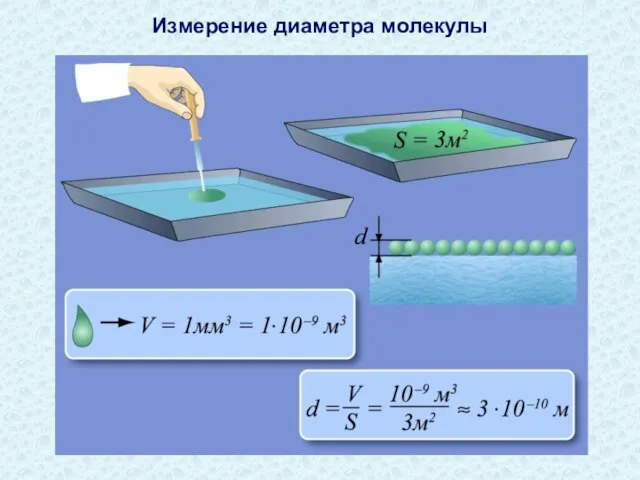
- 30. Измерение диаметра молекулы
- 31. Размеры молекул и атомов чрезвычайно малы. Так, линейные размеры молекул кислорода составляют 3∙10-10 м, воды –
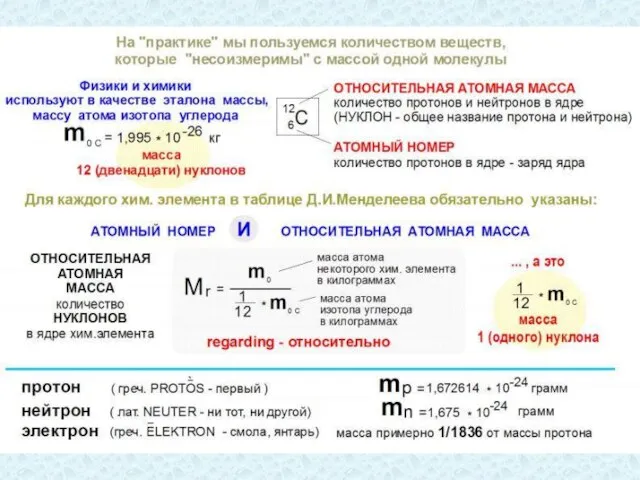
- 32. Немного истории Понятие атомной массы ввёл Джон Дальтон в 1803 году, единицей измерения атомной массы сначала
- 33. Масса нейтрона mn = 1,674929∙10-27 кг масса протона mp = 1,672623∙10-27 кг В ядре атома углерода
- 34. Масса произвольного атома может быть выражена в атомных единицах массы или в килограммах: Относительная атомная масса
- 35. Количеством вещества ν называется физическая величина, определяющая число молекул (или атомов, ионов) в данном теле. Количество
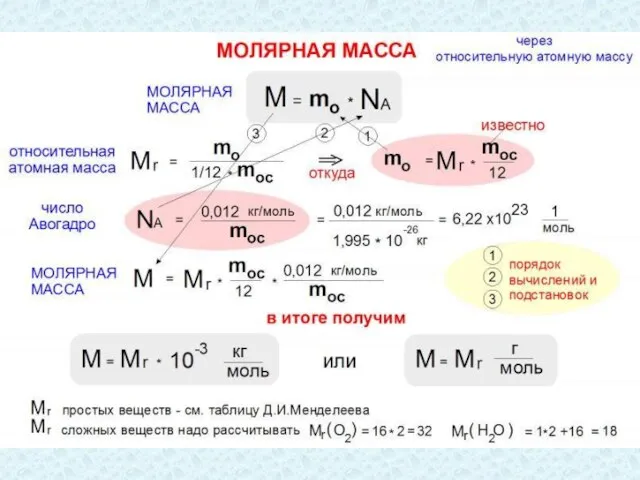
- 36. Молярная масса Масса вещества m связана с его молярной массой M и количеством вещества ν формулой
- 37. Постоянная Авогадро Амедео Авогадро Итальянский физик и химик 9 августа 1776 г. – 9 июля 1856
- 45. Скачать презентацию



































 Презентация на тему Весенние праздники русского народа
Презентация на тему Весенние праздники русского народа Предложение по международной франшизеDollar
Предложение по международной франшизеDollar Степень числа. Квадрат и куб числа
Степень числа. Квадрат и куб числа Презентация на тему Устный счет до десяти
Презентация на тему Устный счет до десяти  ПАТОЛОГИЯ ВСПОМОГАТЕЛЬНОГО АППАРАТА ГЛАЗА
ПАТОЛОГИЯ ВСПОМОГАТЕЛЬНОГО АППАРАТА ГЛАЗА ЗНАНИЯ И ОСНОВНЫЕ МОДЕЛИ ИХ ПРЕДСТАВЛЕНИЯ
ЗНАНИЯ И ОСНОВНЫЕ МОДЕЛИ ИХ ПРЕДСТАВЛЕНИЯ Что такое текст?
Что такое текст? Holidays go round and round
Holidays go round and round Линия. Штрих
Линия. Штрих Образы античной мифологии
Образы античной мифологии Past Continuous Прошедшее продолженное время
Past Continuous Прошедшее продолженное время « Использование И К т на уроках окружающего мира »
« Использование И К т на уроках окружающего мира » Современное состояние науки
Современное состояние науки Политическая система Великобритании
Политическая система Великобритании Долобене гель
Долобене гель Изготовления гусеницы из пластилина (2 класс)
Изготовления гусеницы из пластилина (2 класс) ПЕЙЗАЖ НАСТРОЕНИЯ
ПЕЙЗАЖ НАСТРОЕНИЯ Гранит Карелии
Гранит Карелии Рисунки Людмилы Тумановой
Рисунки Людмилы Тумановой Ответственность за нарушение требований охраны труда
Ответственность за нарушение требований охраны труда Физико-механические свойства горных пород
Физико-механические свойства горных пород Из опыта проектирования реальных объектов:проблемы и решения
Из опыта проектирования реальных объектов:проблемы и решения Программа «Гармония»под редакцией Н.Б. Истоминой
Программа «Гармония»под редакцией Н.Б. Истоминой Филимоновская игрушка. История игрушки
Филимоновская игрушка. История игрушки 10 причин отмечать День Рождения
10 причин отмечать День Рождения Как вести себя, если вы стали заложником террористов
Как вести себя, если вы стали заложником террористов факты о Jacquot Компания «JACQUOT» создана во Франции в 1920 году. Семейное предприятие Годовой оборот более – 160 млн.$ Объем производства –
факты о Jacquot Компания «JACQUOT» создана во Франции в 1920 году. Семейное предприятие Годовой оборот более – 160 млн.$ Объем производства –  Экскурсия по Москве
Экскурсия по Москве