Слайд 2Наследственные болезни эндокринной системы обусловлены мутациями в генах гормонов,
их рецепторов, а

также ферментов биосинтеза и метаболизма
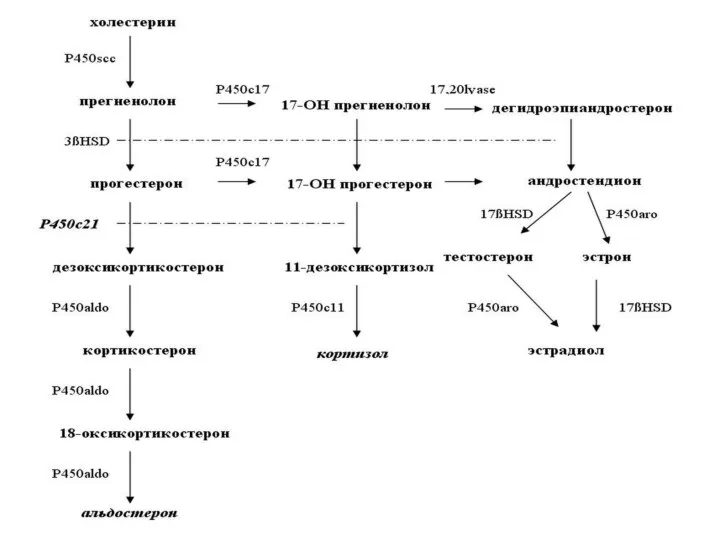
Слайд 3Так, различные синдромы гиперальдостеронизма и гипоальдостеронизма связаны
с избыточной продукцией или дефицитом

альдостерона
Слайд 4Наследственная недостаточность гормона роста ассоциирована с различными вариантами карликовости, или нанизма.
Нарушения

тиреоидного обмена являются причиной врожденного гипотиреоза.
Генетические нарушения гормональной регуляции запаса энергии в жировой ткани ассоциированы с развитием наследственных форм ожирения
Слайд 5Аутоиммунное поражение островкового аппарата
поджелудочной железы, а также инсулинорезистентность инсулинозависимых тканей приводят

к нарушениям всех видов обмена веществ, и, прежде всего, метаболизма углеводов, обуславливая развитие сахарного диабета
Слайд 6В этиологии большинства случаев сахарного диабета участвуют как средовые, так и генетические

факторы, хотя существуют и моногенные формы этого заболевания (MODY-диабет)
Слайд 7Наследственный
альдостеронизм

Слайд 8Нарушения водно-солевого обмена являются ведущими клиническими проявлениями различных наследственных типов альдостеронизма.
Аутосомно-рецессивный

врожденный гипоальдостеронизм, обусловлен мутациями в гене CYP11B2
Слайд 9Этот ген кодирует полипептид 2 субсемейства 11b митохондриального цитохрома P-450, или альдостеронсинтетазу

— фермент, катализирующий конечный шаг превращения кортикостерона в альдостерон
Слайд 11Как многие другие адреналовые цитохромы P-450, альдостеронсинтетаза
обладает множественной ферментативной активностью.
В

клубочковой зоне надпочечников фермент последовательно выполняет функции кортикостеронметилоксидазы
I типа (КМОI), а затем - II типа (КМОII),
то есть производит соответственно
11-бета-гидроксилирование и
18-гидроксилирование
Слайд 12Мутации, затрагивающие разные активности фермента, приводят к двум аллельным вариантам заболевания с

недостаточностью КМОI или КМОII соответственно. Оба варианта характеризуются выраженной потерей натрия и нарушением водно-солевого обмена
Слайд 13При биохимическом исследовании выявляются гипонатриемия, гиперкалиемия и ацидоз.
При этих заболеваниях, вызывающих

изолированную недостаточность минералокортикоидов, биосинтез глюкокортикоидов не страдает
Слайд 14Недостаточность КМОI и КМОII
ведет к накоплению прямых и отдаленных субстратов блокированных

реакций: дезоксикортикостерона, кортикостерона и
18-гидроксикортикостерона
(в последнем случае только при недостаточности КМОII)
Слайд 15При первом варианте с недостаточностью КМОI болезнь проявляется в неонатальном периоде в

виде частого срыгивания, рвоты, дегидратации, жажды, отказа от пищи, летаргии, судорог.
Подобные кризы в первые недели жизни могут приводить к остановке сердца и гибели больного. Характерны задержка раннего физического развития и отставание в росте. В дальнейшем водно-солевой баланс постепенно нормализуется
Слайд 16При втором варианте заболевания адреналовые кризы с выраженной потерей натрия и воды

и увеличением концентрации калия в крови проявляются уже в неонатальном периоде.
Смерть может наступить в течение первого года жизни.
У выживших детей отмечается задержка роста и ослабление тяжести кризов.
При своевременной диагностике и заместительной гормонотерапии прогноз для жизни при обоих вариантах заболевания благоприятный
Слайд 17Наследственный гиперальдостеронизм является гетерогенной группой заболеваний.
Аутосомно-доминантный семейный гиперальдостеронизм I типа, или

глюкокортикоид-подавляемый гиперальдостеронизм
обусловлен микроструктурными перестройками в области локализации генов
CYP11B1 и CYP11B2
Слайд 18Чаще этот тип гиперальдостеронизма рассматривается к одна из моногенных формам артериальной гипертензии

- дексаметазон-чувствительная гипертония
Слайд 19Аутосомно-доминантный тип III заболевания обусловлен мутациями в гене KCNJ5, кодирующем субъединицу 5

G-чувствительного калиевого канала семейства J. Мутации увеличивают проводимость натрия и приводят к тяжелому альдостеронизму с массивной билатеральной гиперплазией надпочечников
Слайд 20Нарушения в работе других ионных каналов также могут приводить к различным формам

альдостеронизма. Так, первичный альдостеронизм с неврологическими аномалиями, включающими генерализованные тонико-клонические судороги, обусловлен мутациями в гене альфа1-субъединицы потенциал-зависимого кальциевого канала L-типа — CACNA1D
Слайд 21Сопутствующими проявлениями заболевания являются артериальная гипертензия, легочная гипертензия и
врожденные пороки сердца

Слайд 22Синдром Барттера является необычной формой
вторичного гиперальдостеронизма, при котором гипертрофия и гиперплазия

юкстагломерулярных клеток почечных нефронов сочетается с нормальным артериальным давлением, гипокалиемическим алкалозом при отсутствии эдемы и резистентностью к сосудосуживающему действию ангиотензина II
Слайд 23Болезнь развивается вследствие нарушения реабсорбции хлорида натрия в восходящем колене
петли Генле,

где в норме реабсорбируется до 30% фильтрующейся соли
Слайд 24Ведущими клиническими проявлениями заболевания являются задержка роста, гиперактивность ренин-ангиотензиновой системы, гипокалиемия, увеличение

продукции почечных простагландинов, гиперкальциурия и гипомагниемия
Слайд 25Наследственные формы синдрома Барттера – это гетерогенная группа аутосомно-рецессивных заболеваний, вызванных нарушением

работы почечных ионных каналов.
Антенатальный тип 1 заболевания обусловлен мутациями в гене буметанид-чувствительного
Na-K-2Cl котранспортера – SLC12A1
Слайд 26Антенатальный тип 2 синдрома Барттера связан с мутациями в гене
АТФ-чувствительного
калиевого

канала – KCNJ1.
Тип 3 синдрома Барттера вызван мутациями в гене почечного хлорного канала В – CLCNKB.
Младенческий тип 4А обусловлен мутациями в гене барттина - BSND, выполняющего роль транспортера почечных хлорных каналов А и В
Слайд 27 Причиной развития младенческого дигенного типа 4B синдрома Барттера, сочетающегося с нейросенсорной

тугоухостью, является одновременное присутствие мутаций в двух соседних генах CLCNKA и CLCNKB, продуктами которых являются почечные хлорные каналы А и В соответственно
Слайд 28Псевдогипоальдостеронизм I типа обусловлен снижением чувствительности канальцевого эпителия к альдостерону и нарушением

реабсорбции натрия, приводящим к солевому истощению вследствие полиурии и дегидратации.
В анализах крови обнаруживаются высокая концентрация альдостерона, гипонатриемия, повышенная активность ренина плазмы
Слайд 29Типичными для этой патологии являются инфекционные поражения дыхательных путей. Компенсация водно-солевого обмена,

введение натрия и контроль гиперкалиемии оказывают положительный лечебный эффект у детей более старшего возраста
Слайд 30Наследственные формы заболевания генетически гетерогенны.
Аутосомно-доминантная форма псевдогипоальдостеронизма
типа IА с относительно

мягким течением обусловлена мутациями в гене минералокортикоидного рецептора — MCR
Слайд 31Причиной развития
аутосомно-рецессивного псевдогипоальдостеронизма типа IВ являются нарушения работы эпителиальных натриевых каналов,

обусловленные мутациями в генах
SCNN1A, SCNN1B и SCNN1G
Слайд 32Псевдогипоальдостеронизм II типа, известный как синдром Гордона, клинически характеризуется гиперкалиемией, гиперхлоремией, метаболическим

ацидозом, а также психическими расстройствами, которые могут быть компенсированы при приеме тиазидовых диуретиков.
У детей старшего возраста, подростков и взрослых больных часто выявляется артериальная гипертензия при низком уровне ренина плазмы
Слайд 33Наследственные формы заболевания также генетически гетерогенны.
Два аутосомно-доминантных типа заболевания обусловлены мутациями

в генах WNK4 и WNK1, продуктами которых являются две гомологичные серинтреонинкиназы, участвующие в регуляции тиазид-чувствительного Na-Cl—котранспортера
Слайд 34Другим регулятором этого котранспортера является транскрипционный фактор kelch3, кодируемый геном KLHL3.
Мутации

в этом гене найдены у больных с аутосомно-рецессивным типом псевдогипоальдостеронизма IID
Слайд 35Еще один аутосомно-доминантный тип заболевания обусловлен мутациями в гене куллина 3 –

CUL3.
Куллины участвуют в контроле митотического деления и способны образовывать комплексы с продуктами
KLHL-генов
Слайд 36Таким образом, все
генетические формы псевдогипоальдостеронизма
II типа
связаны с нарушением работы

тиазид-чувствительного
Na-Cl—котранспортера
Слайд 38Рост скелета и мягких тканей организма индуцируется гормоном роста (соматотропином),
который синтезируется

соматотропными клетками передней доли гипофиза.
Центральную роль в секреции гормона роста играет
рилизинг-гормон,
который действует путем связывания со специфическим рецептором
Слайд 39После высвобождения из гипотоламуса биологически активный гормон роста связывается со своим трансмембранным

рецептором, который димеризуется и активирует сигнальную цепь, ведущую к синтезу и секреции инсулиноподобного фактора роста 1, или соматомедина
Слайд 40Соматомедины являются членами инсулинового семейства полипептидных факторов роста и выполняют роль аутокринных

регуляторов клеточной пролиферации.
Комплекс соматомедина с рецептором активирует в клетках-мишенях пути сигнальной трансдукции, необходимые для формирования митогенных и анаболических ответов, ведущих к росту
Слайд 41Существует два гена гормона роста: нормальный — GH1, или GHN, и вариантный

— GH2, или GHV,
а также 3 гена
плацентарного лактогена (CSH).
Все они образуют единый кластер из 5 соседних генов, расположенных в области 17q22-q24 —
(5'-GH1-CSHL1-CSH1-GH2-CSH2-3')
Слайд 42В настоящее время в этом кластере генов мутации, ассоциированные с наследственными заболеваниями,

найдены только в гене
гормона роста — GH1.
Они идентифицированы у больных с четырьмя аллельными вариантами карликовости: семейной изолированной недостаточности гормона роста
IA, IB и II типов, а также
синдромом Коварского
Слайд 43Тип заболевания IA является наиболее тяжелой аутосомно-рецессивной формой карликовости, при которой гормон

роста полностью отсутствует.
Причиной развития этого варианта заболевания являются
нонсенс-мутации или делеции со сдвигом рамки считывания
Слайд 44В большинстве случаев задержка роста диагностируется уже в первом полугодии жизни. Часто

у больных детей развивается ожирение, характерен высокий голос. Дети выглядят моложе своих сверстников. Наблюдается отставание костного возраста.
У взрослых больных при осмотре выявляются элементы преждевременного старения в виде тонкой морщинистой кожи
Слайд 45Экзогенный гормон роста при данном типе заболевания неэффективен.
Более того, у больных

в ответ на введение гормона роста вырабатываются антитела, что свидетельствует об его отсутствии в эмбриональном периоде
Слайд 46При варианте недостаточности IВ содержание гормона роста в крови снижено, но все

же определяется. Карликовость менее выражена. Такие больные хорошо отвечают на терапию экзогенным гормоном роста.
Чаще всего у больных обнаруживаются сплайсинговые мутации в гене GH1
Слайд 47При некоторых формах карликовости, сходных по своим клиническим проявлениям с вариантом IВ,

у больных найдены мутации в гене рецептора специфического рилизинг-гормона — GHRHR
Слайд 48Тип II семейной изолированной недостаточности гормона роста наследуется по доминантному типу и

протекает также как тип IВ. Причиной развития этой формы заболевания являются сплайсинговые или миссенс-мутации в гене GH1
Слайд 49При аутосомно-доминантном синдроме Коварского уровень иммунореактивных форм гормона роста сохраняется в пределах

нормы или даже выше, однако его биологическая активность резко снижена, и одновременно наблюдаются аномально низкие уровни соматомедина.
Причиной развития синдрома Коварского являются специфические миссенс-мутации в гене GH1
Слайд 50При этом больные хорошо отвечают на терапию препаратами соматотропного гормона. Оказалось, что

мутантный гормон роста, хотя и способен связываться с рецептором, но это не приводит к его димеризации, а значит и к активации синтеза соматомедина
Слайд 51Мутации в гене
рецептора гормона роста – GHR – также приводят к

карликовости, известной как синдром Ларона, или нечувствительность рецептора гормона роста.
При этом содержание соматотропина и его активность сохраняются в пределах нормы, но снижено содержание соматомедина
Слайд 52При синдроме Ларона наблюдается выраженная задержка роста, которая может быть очевидна уже

при рождении.
Кроме того, к проявлениям заболевания относятся ожирение, голубые склеры, лицевой дизморфизм, задержка прорезывания зубов, позднее закрытие родничка, высокий голос, а также гипокалиемия
Слайд 53Болезнь наследуется по аутосомно-рецессивному типу и чаще всего обусловлена мутациями с преждевременной

терминацией трансляции.
Среди них нонсенс-мутация R43X является мажорной
Слайд 54Инактивирующие мутации в генах инсулиноподобного фактора роста 1 (IGF1) и его рецептора

(IGF1R) приводят к двум тяжелым формам аутосомно-рецессивной карликовости, которая в первом случае сочетается с тугоухостью и умственной отсталостью.
Некоторые мутации в гене IGF1R могут оказывать ингибирующее действие на рост даже в гетерозиготном состоянии
Слайд 55У таких больных наблюдается нормальный уровень гормона роста и его рецептора в

сочетании с высоким уровнем соматомедина и снижением количества или чувствительности рецептора соматомедина
Слайд 56Пангипопитуитарная карликовость,
или низкий рост в сочетании с дефицитом гормона роста, гонадотропинов,

адренокортикотропного и тиреотропного гормонов,
встречается довольно часто и в большинстве случаев объясняется не наследственными причинами, например, краниофарингеомой
Слайд 57Наряду с этим, описаны моногенные формы пангипопитуитаризма, обусловленные, в частности, нарушением регуляции

синтеза и секреции гормонов роста.
В дифференцировке соматотропных клеток участвуют гены транскрипционных факторов POU1F1, PROP1, LHX3,
LHX4, HESX1, OTX2 и др.
Слайд 58Мутации в этих генах приводят к комбинированной недостаточности гипофизарных гормонов (КНГГ), при

которой у больных наблюдается снижение продукции гормона роста и одного или нескольких других гормонов гипофиза
Слайд 59Так, полное отсутствие
гормона роста и пролактина
в сочетании с частичной недостаточностью

тиреотропного гормона
может быть обусловлено присутствием инактивирующих мутаций в гене POU1F1
Слайд 60У больных с раннего детского возраста наблюдается грубая задержка роста,
у некоторых

развивается тяжелая умственная отсталость.
При магнитно-резонансной томографии может быть обнаружена гипоплазия гипофиза.
В лечении больных используется комбинированная терапия препаратами соматотропного гормона и L-тирозином
Слайд 61Другой аутосомно-рецессивный тип пангипопитуитарной карликовости, сочетающийся с гипогонадизмом, является результатом мутаций в

гене PROP1.
У таких больных, наряду с отсутствием гормона роста, наблюдается недостаточность гонадотропинов, тиреотропного и адренокортикотропного гормонов
Слайд 62Причем подобная гормональная недостаточность у разных больных может появляться в разном возрасте

При тяжелой гипоплазии гипофиза и атрофии надпочечников больные погибают в периоде новорожденности.
У некоторых больных могут развиваться гипогликемические судороги, которые в неонатальном периоде также нередко приводят к летальному исходу
Слайд 63Однако в большинстве случаев болезнь проявляется карликовостью, сходной с синдромом Ларона, в

сочетании с выраженной задержкой репродуктивного развития.
При этом комплексная гормональная заместительная терапия дает положительные результаты
Слайд 64Мутации в гене LHX3 приводят к дефициту гормона роста и гонадотропина.
Клинически

болезнь проявляется в форме гипофизарного инфантилизма, сочетающегося с ригидностью шейного отдела позвоночника и варьирующей по степени тяжести нейросенсорной тугоухостью
Слайд 65Остальные типы пангипопитуитарной карликовости наследуются по аутосомно-доминантному типу. Мутации в гене LHX4

приводят к недостаточности соматотропина в сочетании со снижением продукции тиреоид-стимулирующего и адренокортикотропного гормонов. При этом у больных, наряду с задержкой роста, выявляются пороки развития гипофиза и мозжечка, малые размеры турецкого седла
Слайд 66Недостаточность гормонов гипофиза в сочетании с пороками развития ЦНС характерна для одного

из наиболее распространенных типов пангипопитуитарной карликовости, обусловленной мутациями в гене HESX1. При аутосомно-доминантном типе заболевания, обусловленном мутациями в гене OTX2, гипофизарная дисфункция может сочетаться с микроофтальмией или дистрофией сетчатки
Слайд 67Наследственные болезни тиреоидного обмена

Слайд 68Одной из причин снижения функции щитовидной железы является врожденный гипотиреоз. Болезнь может

развиваться еще во внутриутробном периоде из-за недостаточности тиреотропных гормонов и, прежде всего, вследствие дефицита циркулирующего тироксина
Слайд 69При этом нарушается обмен мукополисахаридов и в тканях накапливается большое количество креатинина

и муцинозного вещества, приводящих к слизистому отеку – микседеме.
Следствием этих процессов является отставание нервно-психического и физического развития ребенка
Слайд 70Однако при раннем назначении больным гормонов щитовидной железы, в частности L-тироксина, можно

предотвратить развитие инвалидизирующей симптоматики и значительно улучшить состояние больного.
Это обусловливает необходимость ранней диагностики заболевания путем биохимического неонатального скрининга
Слайд 71Тяжелая форма врожденного гипотиреоза выявляется сразу после рождения ребенка из-за присутствия микседемы

в сочетании с брадикардией, пупочной грыжей, повышенной сухостью и ломкостью волос, вялостью и сонливостью
Слайд 72Для больных характерны большая масса тела, увеличение языка, сухость, шелушение и бледность

кожных покровов, холодных на ощупь. Голос низкий, «каркающий». При отсутствии лечения отставание психического и физического развития неуклонно прогрессируют, в последующем формируется олигофрения
Слайд 74Наиболее яркая картина врожденного гипотиреоза проявляется к 4-6 месяцам жизни, особенно при

естественном вскармливании.
Дети начинают резко отставать в росте, весе, психическом развитии, вяло реагируют на различные раздражители, перестают узнавать родителей
Слайд 75В 85% случаев причиной наследственного врожденного гипотиреоза является агенезия, гипоплазия или чаще

эктопическая локализация щитовидной железы.
В последнем случае тиреоидная ткань может располагаться в основании языка.
В некоторых случаях болезнь протекает бессимптомно — так называемый компенсированный гипотиреоз
Слайд 76Аутосомно-доминантные типы врожденного незобного гипотиреоза генетически гетерогенны.
Высокий уровень тиреотропного гормона и

снижение содержания тиреоидных гормонов наблюдается у больных с мутациями в генах рецепторов тиреотропного гормона –TSHR и THRA, а также бета-субъединицы тиреоид-стимулирующего гормона – TSHB
Слайд 77Мальформации щитовидной железы характерны для типов заболевания, обусловленных мутациями в генах транскрипционных

факторов –
PAX8 и CSX.
Pax8, участвует в дифференцировке тироксин-продуцирующих фолликулярных клеток щитовидной железы
Слайд 78Продуктом гена CSX является кардиоспецифический транскрипционный фактор NKX2-5. Наследственные нарушения в его

работе чаще всего обнаруживаются у больных с врожденными пороками сердца.
Однако некоторые специфические мутации в гене CSX приводят к дисгенезии щитовидной железы, что и объясняет патогенез данного типа врожденного гипотиреоза
Слайд 79Другие наследственные болезни тиреоидного обмена могут быть обусловлены нарушением органификации, транспорта или

рециркуляции йода, а также генерализованной тканевой резистентностью к тиреоидным гормонам или нарушением их внутриклеточного транспорта и метаболизма
Слайд 81При ожирении наблюдается патологическое увеличение массы тела за счет жировой ткани.
Этому

способствует положительный энергетический баланс в сочетании с избытком поступающих углеводов, которые накапливаются в организме в виде триглицеридов
в жировой ткани
Слайд 82Важная роль в поддержании энергетического равновесия принадлежит гормонам.
Ожирение может развиваться при

уменьшении затрат энергии, повышении эффективности усвоения питательных веществ, недостаточной возможности мобилизовать недостающую энергию из жировых энергетических депо.
В контроле каждого из этих уровней участвуют как генетические, так и средовые факторы
Слайд 83Поэтому ожирение может быть результатом как наследственных нарушений энергетического метаболизма, так и

неправильного образа жизни, касающегося, в первую очередь, характера питания
Слайд 84Предполагается, что изменчивость массы жира у человека на 30-50% обусловлена генетическими факторами.

В большинстве случаев у больных наблюдается повышенная наследственная предрасположенность к развитию ожирения, которая формируется за счет присутствия функциональных полиморфных аллелей во многих генах
Слайд 85Гены-кандидаты, ассоциированные с ожирением, во многих случаях участвуют в контроле сигнального пути,

ответственного за регуляцию количества энергии, запасаемой в виде жира в организме.
Начинается этот путь с гормона лептина, вырабатываемого адипоцитами
Слайд 86Действие лептина противоположно действию «гормона голода» - грелина. Количество лептина пропорционально объему

жировой ткани.
Из жировой ткани лептин попадает в кровь и достигает специфических рецепторов в гипотоламусе
Слайд 87При этом активизируется метаболическая цепь, которая заканчивается выработкой меланокортина, снижающего потребление человеком

пищи. Генетические нарушения любого из участников этой цепи ведут к развитию синдрома ожирения
Слайд 88Мутации в гене лептина (LEP) и его рецептора (LEPR) приводят к редким

аутосомно-рецессивным формам ожирения.
Примерно у 1% больных с наследственными формами ожирения обнаруживается специфическая мутация Arg236Gly
в гене проопиомеланокортина (POMC3)
Слайд 89Этот прогормон является предшественником, по крайней мере, шести гормонов, включая АКТГ, липотропин,

мелано-стимулирующие гормоны (альфа- и бета-меланотропин, а также меланокортин), эндорфин
Слайд 90У больных, наряду с ожирением, которое наблюдается уже в течение первых месяцев

жизни, как правило, выявляется недостаточность АКТГ в сочетании с рыжим цветом волос
Слайд 91К сходной форме ожирения приводят рецессивные мутации в гене
прогормоновой конвертазы 1,

участвующей в процессинге АКТГ и меланокортина (PCSK1)
Слайд 92В этом случае у больных развивается гиперпроинсулинемия, так как эта конвертаза участвует

в биогенезе инсулина, переводя проинсулин в активный инсулин в клетках поджелудочной железы. Сопутствующими проявлениями аутосомно-рецессивных форм ожирения могут быть гипогонадотропный гипогонадизм, гипоадренализм и низкий рост
Слайд 93Однако наиболее частым является аутосомно-доминантный тип ожирения, обусловленный мутациями в гене рецептора

4 меланокортина – MC4R .
Он составляет около 6% всех случаев наследственного ожирения.
В многочисленных исследованиях подтверждена ассоциация
индекса массы тела с генетическими маркерами, сцепленными с геном MC4R
Слайд 94Избыточная масса тела является одним из ведущих клинических проявлений многих наследственных синдромов

– Прадера-Вилли, Альстрема, Барде-Бидля и Лоренса-Муна, Коэна и др.
Слайд 95Синдром Прадера-Вилли относится к болезням геномного импринтинга –
у больных инактивированы локализованные

в области 15q11-13 гены отцовского происхождения.
При рождении дети малоподвижны, имеют выраженную мышечную гипотонию, у них снижены сухожильные рефлексы, а также сосательный и глотательный, что затрудняет кормление
Слайд 96После 6-месячного возраста развивается полифагия, ожирение.
В пубертатном периоде отмечается проявление гипогонадотропного

гипогонадизма, снижение когнитивных функций и мягкая олигофрения различной степени выраженности.
Больные доброжелательны и безинициативны
Слайд 98При синдроме Барде-Бидля,
ожирение может сочетаться с деградацией сетчатки глаз, поликистозом почек,

гипогонадизмом, полидактилией и задержкой умственного развития.
У больных наблюдается склонность к развитию диабета, фиброза печени, атаксии, расстройства речи, асимметрии висцеральных органов, патологии зубов, аносмии, потери слуха
Слайд 99Синдром Барде-Бидля–
это гетерогенная группа аутосомно-рецессивных заболеваний.
В настоящее время описаны 19

генетических типов этого синдрома, и все они относятся к цилиопатиям.
В большинстве случаев у больных дефектными являются структурные белки комплекса, необходимого для осуществления цилиогенеза (BBS-белки)
Слайд 100Для многих генетических типов синдрома Барде-Бидля характерно «трехаллельное наследование» – присутствие гомозиготной

или компаунд-гетерозиготной мутации в одном из 6 ассоциированных с заболеванием BBS-локусов, в сочетании с гетерозиготной мутацией в любом другом из этих локусов
Слайд 101При синдроме Альстрема ожирение с гиперинсулинемией сочетается с пигментной дегенерацией сетчатки, прогрессирующей

нейросенсорной тугоухостью, дилатационной кардиомиопатией, сахарным диабетом и нефропатией. Причиной этого аутосомно-рецессивного заболевания являются мутации в гене ALMS1, продукт которого также участвует в цилиогенезе
Слайд 102У больных с аутосомно-рецессивным синдромом Коэна при рождении наблюдается низкая масса тела,

мышечная гипотония.
В дальнейшем развивается умеренное ожирение в сочетании с задержкой психомоторного развития, эпилепсией, атаксией и множественными проявлениями скелетной дисплазии
Слайд 103Отмечаются характерные лицевые особенности – антимонголоидный разрез глаз, высокая спинка носа, постоянно

открытый рот косоглазие. Болезнь обусловлена мутациями в гене VPS13B, продукт которого участвует в везикулоопосредуемом внутриклеточном транспорте белков
Слайд 105Сахарный диабет — это частое хроническое заболевание, которым страдает до 12% населения

в странах Европы,
Северной Америки и Африки.
Согласно существующей классификации различают: сахарный диабет 1 типа, или инсулинзависимый (ИЗСД) и сахарный диабет 2 типа, инсулиннезависимый (ИНСД)
Слайд 106При ИЗСД развивается абсолютная недостаточность инсулина, а особенностью патогенеза ИНСД является относительная

недостаточность инсулина или инсулинорезистентность инсулинозависимых тканей.
При сахарном диабете нарушаются все виды обмена веществ, но главным проявлением болезни является гипергликемия
Слайд 107ИЗСД отличает разнообразие этиологии и патогенеза, при этом в основе развития сахарного

диабета 1 типа лежит аутоиммунное поражение бета-клеток островков Лангерганса поджелудочной железы, что приводит к дефициту синтеза проинсулина и гипергликемии
Слайд 108Характерными проявлениями заболевания являются жажда, полиурия, потеря массы тела, нарастающая общая слабость.

Нередко ИЗСД манифестирует внезапно развитием кетоацидоза и
диабетической комы.
Типичным является наличие осложнений со стороны многих органов, прежде всего, сосудов и почек (диабетические ангиопатии, диабетическая нефропатия)
Слайд 109Конкордантность среди монозиготных близнецов варьирует от 30% до 50%.
Риск развития заболевания

у брата или сестры больного составляет 6%.
Таким образом, в этиологии заболевания участвуют как средовые, так и генетические факторы
Слайд 110Значительная часть наследственной предрасположенности к ИЗСД формируется за счет присутствия специфических полиморфных

аллелей в HLA-локусе. Чувствительность к ИЗСД определяется, главным образом, комбинацией аллелей HLA-DR и HLA-DQ локусов гистосовместимости класса II
Слайд 111Наиболее значимыми предрасполагающими аллелями являются DR3, DR4 и DQ-beta . При наличии

соответствующих гаплотипов риск для сибсов пробанда возрастает до 20%. Некоторые аллели HLA-комплекса (DR2, DR5) оказывают протективный эффект в отношении развития диабета
Слайд 112 Другими значимыми генетическими факторами риска ИЗСД являются полиморфные аллели генов
PTPN2,

C12ORF30, ERBB3, KIAA0350
Слайд 113Сахарный диабет 2 типа обычно развивается в возрасте 40-60 лет. Вместе с

тем, известны случаи развития ИНСД у лиц в возрасте до 35 лет с сохранной функцией поджелудочной железы, так называемый «диабет взрослого типа у молодых», или MODY-диабет
Слайд 114Сопутствующими этиотропными факторами ИНСД являются ожирение и полифагия, обуславливающими повышенную потребность в

инсулине и, как следствие, вызывающими гипертрофию островков поджелудочной железы с последующим их истощением
Слайд 115Это приводит к инсулиновой недостаточности, нарушению толерантности к глюкозе и развитию инсулинорезистентности

тканей. Часто нарушение толерантности к глюкозе или ИНСД, наряду с ожирением, АГ, дислипопротеинемией и ИБС, являются компонентами метаболического синдрома
Слайд 116В этиологии ИНСД генетические факторы могут определять секреторную недостаточность бета-клеток или резистентность

рецепторов инсулина. Это гетерогенная патология, в которую, наряду с многофакторными, входят и моногенные формы.
В 2-3% случаев диабет наследуется по материнскому типу, причем иногда он сопровождается серьезными нарушениями слуха
Слайд 117 Показано, что в основе патогенеза подобных состояний лежат
мутации в мтДНК.

В некоторых семьях с материнским наследованием ИНСД и тугоухости, развивающейся в третьей или четвертой декаде жизни, идентифицирована протяженная делеция размером в 10,4 кб, затрагивающая более 60% всего митохондриального генома
Слайд 118В других семьях причиной наследуемого по материнской линии синдромального ИНСД являются точковые

мутации
в мтДНК.
Во всех этих случаях диабет связан с дефектами митохондриального окислительного фосфорилирования
Слайд 119MODY-диабет
наследуется по аутосомно-доминантному типу.
Он составляет 2-5% всех случаев ИНСД.
Эта

генетически гетерогенная патология связана с наследственными дефектами секреции инсулина
Слайд 120В настоящее время идентифицировано 11 генетических типов
MODY-диабета.
Из них наиболее частым

является MODY2, обусловленный присутствием гетерозиготных мутаций в гене глюкокиназы – GCK
Слайд 121Этот тип заболевания часто обнаруживается у детей с мягкой гипергликемией, а также

у женщин с диабетом беременных и семейной историей диабета. Болезнь часто протекает бессимптомно и корригируется диетой.
Инсулиновая терапия необходима только в 2% случаев
Слайд 122Часто MODY-диабет может быть связан с нарушением транскрипционного контроля, обусловленного мутациями в

генах гепатоцитарных ядерных факторов (HNF4A; HNF1A и HNF1B); панкреатического трансактиватора (PDX1);
транскрипционных факторов, участвующих в нейрогенной дифференцировке (NEUROD1) и других
(KLF11 и PAX4)
Слайд 123При других генетических типах заболевания мутации найдены в генах панкреатического липолитического фермента

(CEL);
инсулина (INS);
нерецепторной тирозинкиназы В-клеток (BLK)
Слайд 124Мутации в гене инсулинового рецептора (INSR) приводят к целой серии аллельных заболеваний,

клинические проявления которых весьма разнообразны.
Среди них ИНСД с черным акантозом, некоторые доброкачественные варианты синдрома инсулинорезистентности А, лепречаунизм и синдром Рабсона-Менденхолла
Слайд 125У больных могут наблюдаться как нарушение толерантности к глюкозе, так и типичная

симптоматика ИНСД.
В ряде случаев развивается сахарный диабет с быстрым летальным исходом
Слайд 126Лепречаунизм может проявляться задержкой внутриутробного развития, низким ростом и маленьким весом при

рождении, отсутствием подкожной жировой клетчатки и лицевым дизморфизмом. Больные дети погибают в первый год жизни от сопутствующих рекуррентных инфекций
Слайд 127Синдром Рабсона-Менденхолла отличается более мягким течением и большей продолжительностью жизни. При инсулинорезистентности

типа А больные доживают до взрослого возраста.
При этом у них наблюдаются выраженная гипергликемия, гиперинсулинемия, черный акантоз и у женщин — гиперандрогенизм, который с возрастом может регрессировать
Слайд 128Такое разное проявление мутаций в одном и том же гене INSR зависит

от характера повреждения инсулинового рецептора.
Оказалось, что при тяжелых вариантах у больных чаще всего присутствуют нонсенс-мутации.
При этом рецептор на мембране либо полностью отсутствует, либо его количество снижено не менее,
чем на 80%
Слайд 129При мягких формах инсулинорезистентности чаще всего находят миссенс-мутации, причем в некоторых случаях

они присутствуют у больных в гетерозиготном состоянии.
Как правило, количество рецепторов сохраняется в пределах нормы, но может быть снижен их аффинитет по отношению к инсулину
Слайд 130Генетические причины развития многофакторного ИНСД очень разнообразны.
В 25% случаев обнаруживается ассоциация

заболевания с аллелями гена PPARG , кодирующего
гамма-рецептор, активируемый пролифератором пероксисом
Слайд 131Продукт этого гена участвует в формировании жировой ткани и перекисном окислении липидов.

Мутации в гене PPARG приводят к тяжелым формам
ожирения и семейной липодистрофии 3 типа
Слайд 132С повышенными частотами у больных присутствуют полиморфные аллели в генах транскрипционного фактора

(PAX4), адипонектина (ADIPOQ), рецептора сульфонилмочевины, имеющего высокое сродство к бета-клеткам (ABCC8), трансмембранного белка, дефектного при синдроме Вольфрама, основными клиническими проявлениями которого является диабет в сочетании с глухотой (WFS1)
Слайд 133Найдена ассоциация сахарного диабета 2 типа с полиморфными аллелями генов калиевых каналов

(KCNQ1 и KCNJ15), транскрипционного фактора
АP2-бета (TFAP2B), интерлейкина-6 (IL6), субстрата 2 инсулинового рецептора - глобулина, связывающего половой гормон (SHBG) и др.
Число полиморфных аллелей, ассоциированных с риском развития ИНСД, достигает нескольких сотен


































































































































 Реконструкция индивидуального теплового пункта зд.5 ЗРИ АО СХК
Реконструкция индивидуального теплового пункта зд.5 ЗРИ АО СХК Топ любимых мемов в интернете
Топ любимых мемов в интернете Методические материалы к проекту
Методические материалы к проекту Жесткий диск
Жесткий диск Система мотивации
Система мотивации 1358658
1358658 Тайна бермудского треугольника
Тайна бермудского треугольника RTS StandardПЕРЕНОС ВРЕМЕНИ ПОСТАВКИ
RTS StandardПЕРЕНОС ВРЕМЕНИ ПОСТАВКИ Ремонт оконных блоков
Ремонт оконных блоков Загадки о цветах
Загадки о цветах Презентация на тему Уголовный закон и его действие
Презентация на тему Уголовный закон и его действие Вопрос в косвенной речи
Вопрос в косвенной речи Подготовка руки ребенка к письму в школе
Подготовка руки ребенка к письму в школе Компьютерные вирусы
Компьютерные вирусы LIEBHERR LTM 1160-5.1Самоходный кран большой грузоподъемности (160 тонн)
LIEBHERR LTM 1160-5.1Самоходный кран большой грузоподъемности (160 тонн) Психодинамические и личностные свойства взрослых людей - выходцев из многодетных семей (по критериям возраста, уровня образовани
Психодинамические и личностные свойства взрослых людей - выходцев из многодетных семей (по критериям возраста, уровня образовани МОУ Гимназия № 2 г. Ярославля
МОУ Гимназия № 2 г. Ярославля Налоги как инструмент государственного регулирования экономики
Налоги как инструмент государственного регулирования экономики Let’s practice
Let’s practice Осень
Осень Исследование рынка труда в области компьютерной лингвистики
Исследование рынка труда в области компьютерной лингвистики Нагрузки и воздействия, учитываемые при расчетах. Тема 2
Нагрузки и воздействия, учитываемые при расчетах. Тема 2 М.Ю.Лермонтов в Тамани
М.Ю.Лермонтов в Тамани MPVF. Шаблон для презентации
MPVF. Шаблон для презентации Вышивание
Вышивание Права литературных героев
Права литературных героев Тульский перепел
Тульский перепел Дизайн и реклама – составляющие художественной культуры
Дизайн и реклама – составляющие художественной культуры