Содержание
- 2. Количество вещества – такое количество вещества, которое содержит 6 . 1023 частиц (т.е. число Авогадро NA=
- 3. Молярная масса – масса одного моля вещества (обозначают М, рассчитывается в г/моль) численно равна относительной молекулярной
- 4. Молярный объем – объем одного моля вещества. Обозначают Vm . В соответствии со следствием закона Авогадро
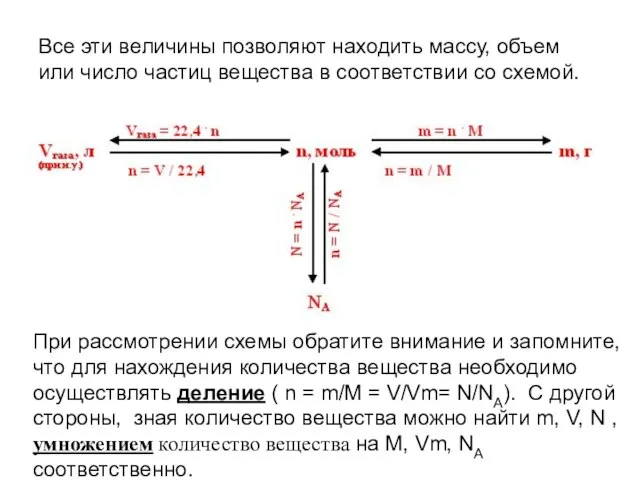
- 5. Все эти величины позволяют находить массу, объем или число частиц вещества в соответствии со схемой. При
- 6. Следующая величина, которая заслуживает внимания это массовая доля. Массовая доля. Обозначается w. Рассчитывается в долях или
- 7. Кроме того для смесей газов или растворов часто используется понятие молярная концентрация, которая рассчитывается по формуле:
- 8. Плотность. Плотность любого вещества рассчитывается по формуле ρ = m/V, измеряется обычно в г/мл или в
- 9. Кроме того, для газов вводиться понятие относительной плотности ( D), которая показывает во сколько раз один
- 10. Плотность газов в задачах по органической химии часто используется для нахождения молярной массы газа: М =
- 11. Одно из очень важных следствий закона Авогадро заключается в том, что: объемы газов при химических реакциях
- 12. Ну и последнее про что хотелось бы сказать – это выход продукта реакции. Как бы нам
- 14. Скачать презентацию










 Правовые основы семьи и брака
Правовые основы семьи и брака Детский писатель Борис Заходер
Детский писатель Борис Заходер Анализ бренда
Анализ бренда Презентация на тему Украинская кухня
Презентация на тему Украинская кухня Технологии нейтрализации агрессивных проявлений у детей и подростков
Технологии нейтрализации агрессивных проявлений у детей и подростков 1 Lec (1)
1 Lec (1) 1
1 Project_A
Project_A Подразделение командных тренингов и мероприятий KORPORATIFF
Подразделение командных тренингов и мероприятий KORPORATIFF Презентация по английскому Парад алфавита
Презентация по английскому Парад алфавита  Об итогах образовательной деятельности государственного казённого образовательного учреждения высшего образования
Об итогах образовательной деятельности государственного казённого образовательного учреждения высшего образования Буква «Ч»
Буква «Ч» Технологии гибки AMB-10031T– гидравлический гибочный пресс
Технологии гибки AMB-10031T– гидравлический гибочный пресс В.Б. Тарасов МГТУ им. Н.Э.Баумана, Кафедра «Компьютерные системы автоматизации производства» e-mail:
В.Б. Тарасов МГТУ им. Н.Э.Баумана, Кафедра «Компьютерные системы автоматизации производства» e-mail:  Портфолио педагога - психолога Вильховой Ксении Леонидовны
Портфолио педагога - психолога Вильховой Ксении Леонидовны Понятие и механизм правотворчества
Понятие и механизм правотворчества Выпускная работа Череп саблезубого тигра
Выпускная работа Череп саблезубого тигра Volkswagen Amarok На Black Sea Cup 2010
Volkswagen Amarok На Black Sea Cup 2010 Главные символы России
Главные символы России Презентация на тему Простые вещества металлы 8 класс
Презентация на тему Простые вещества металлы 8 класс  Понятие, виды обязательств по оказанию услуг
Понятие, виды обязательств по оказанию услуг  Итоговый педсовет МБДОУ "ЦРР-детский сад"Теремок" за 2013-2014 учебный год
Итоговый педсовет МБДОУ "ЦРР-детский сад"Теремок" за 2013-2014 учебный год Идеальная спираль в искусстве
Идеальная спираль в искусстве Результаты стажировки и представление кооперационного проекта
Результаты стажировки и представление кооперационного проекта Особености и трудности, возникающие, при переводе
Особености и трудности, возникающие, при переводе Презентация на тему Формат презентации для защиты диплома
Презентация на тему Формат презентации для защиты диплома Методы научных исследований
Методы научных исследований  Меры защиты организаций от компьютерных преступных посягательств Козюкова М.А., студент гр. ЭиП-434 ЮУрГУ
Меры защиты организаций от компьютерных преступных посягательств Козюкова М.А., студент гр. ЭиП-434 ЮУрГУ