Содержание
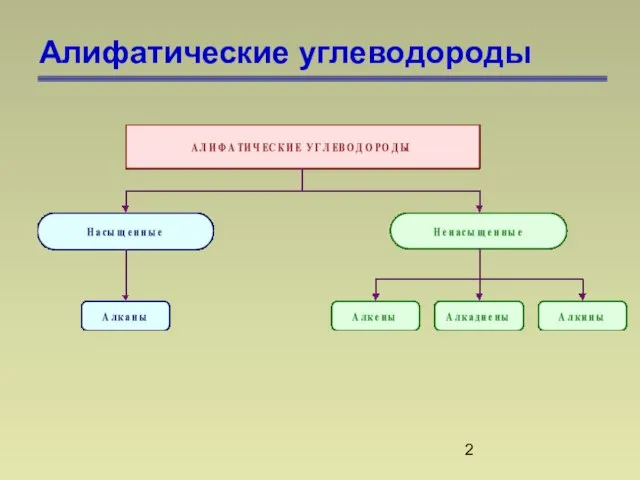
- 2. Алифатические углеводороды
- 3. Алканы Алканами называются насыщенные углеводороды, молекулы которых состоят из атомов углерода и водорода, связанных между собой
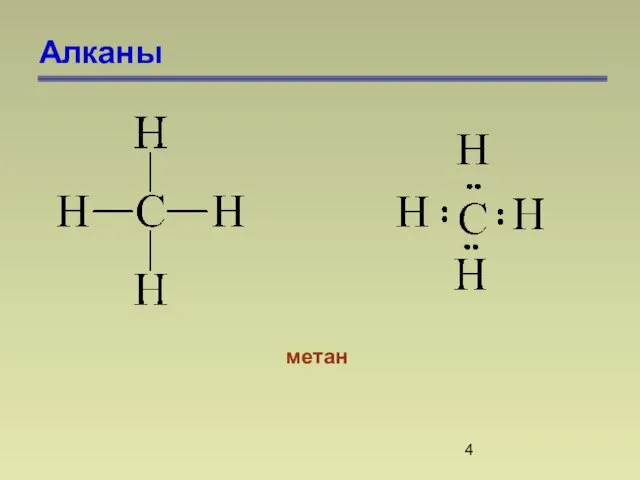
- 4. Алканы метан
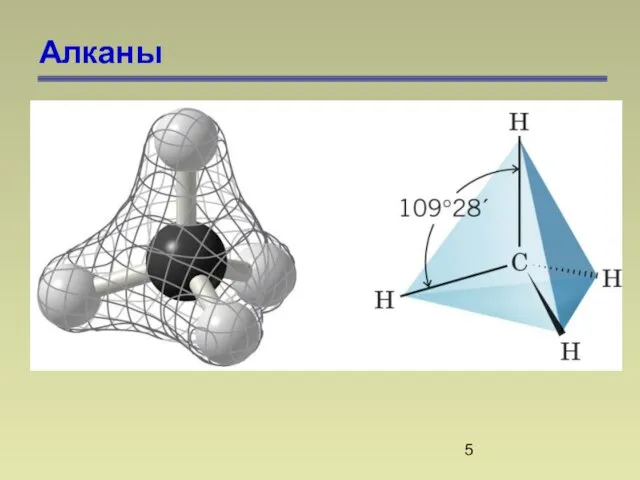
- 5. Алканы
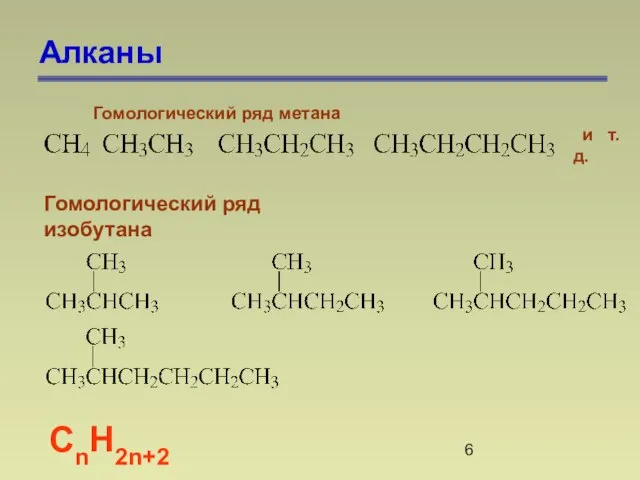
- 6. Алканы СnН2n+2
- 7. Алканы. Номенклатура. Названия нормальных алканов по заместительной номенклатуре
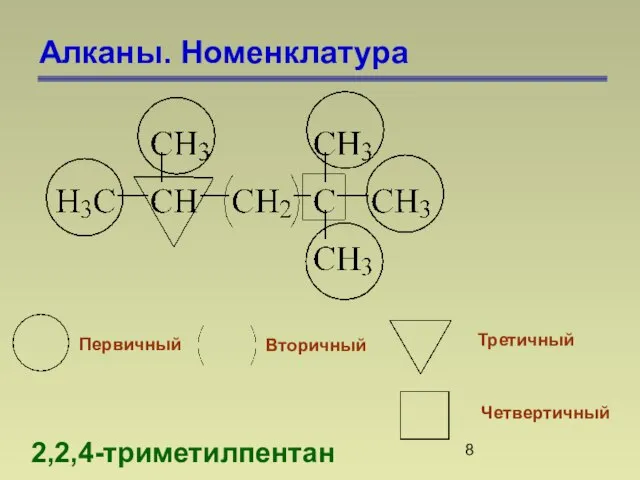
- 8. Алканы. Номенклатура 2,2,4-триметилпентан Первичный Вторичный Третичный Четвертичный
- 9. Алканы. Номенклатура
- 10. Алканы. Номенклатура 1) определяют самую длинную цепь атомов углерода. Число атомов углерода в этой цепи служит
- 11. Алканы. Номенклатура 4) при наличии двух и более заместителей нумерацию цепи производят так, чтобы заместители получили
- 12. Алканы. Номенклатура 3,5-диметил-3-этилоктан
- 13. Алканы. Номенклатура 2,3,4-триметилпентан
- 14. Алканы. Номенклатура 2,3,6-триметилгептан
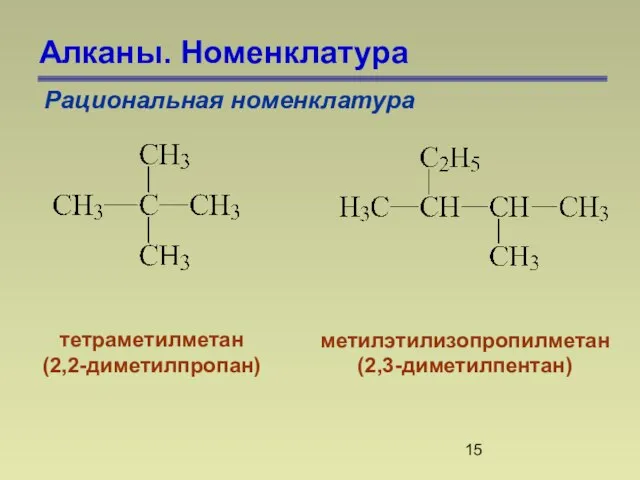
- 15. Алканы. Номенклатура Рациональная номенклатура тетраметилметан (2,2-диметилпропан) метилэтилизопропилметан (2,3-диметилпентан)
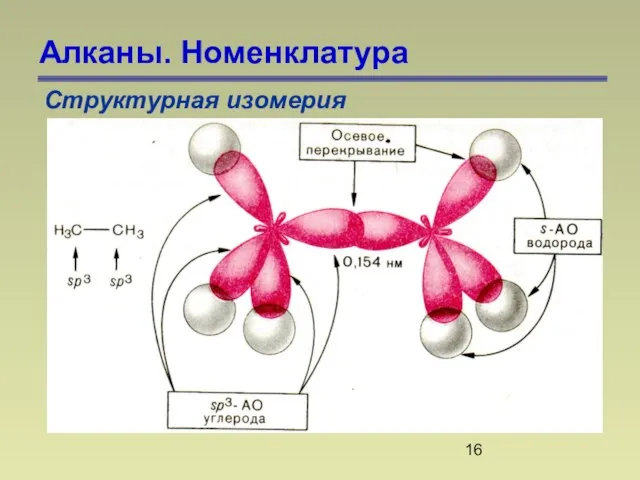
- 16. Алканы. Номенклатура Структурная изомерия
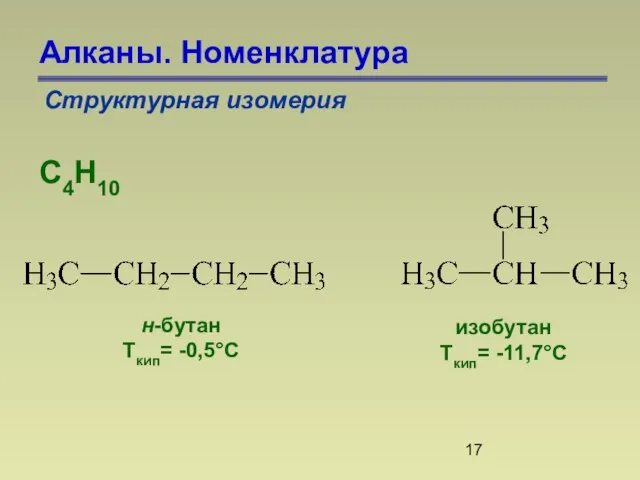
- 17. Алканы. Номенклатура Структурная изомерия С4Н10 н-бутан Ткип= -0,5°С изобутан Ткип= -11,7°С
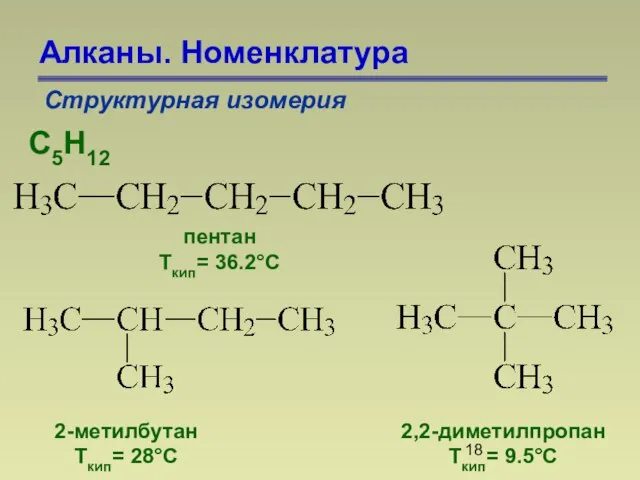
- 18. Алканы. Номенклатура Структурная изомерия С5Н12 пентан Ткип= 36.2°С 2-метилбутан Ткип= 28°С 2,2-диметилпропан Ткип= 9.5°С
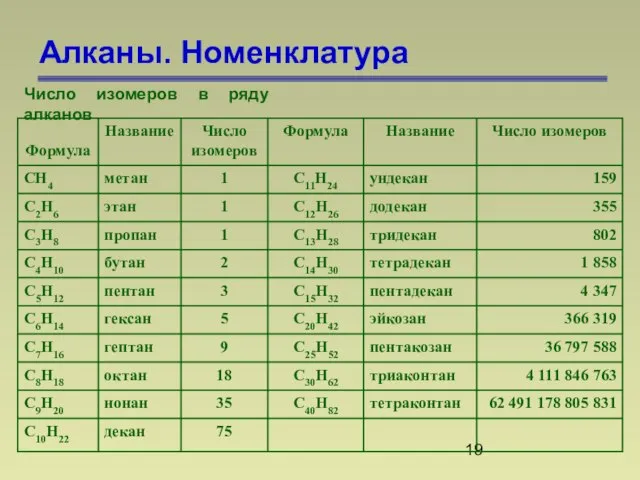
- 19. Алканы. Номенклатура Число изомеров в ряду алканов
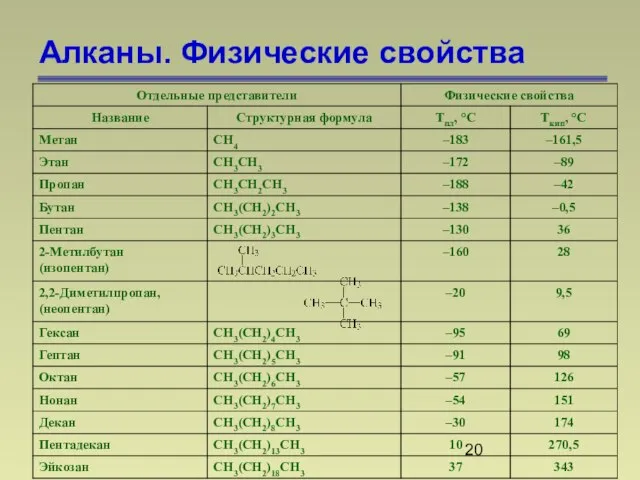
- 20. Алканы. Физические свойства
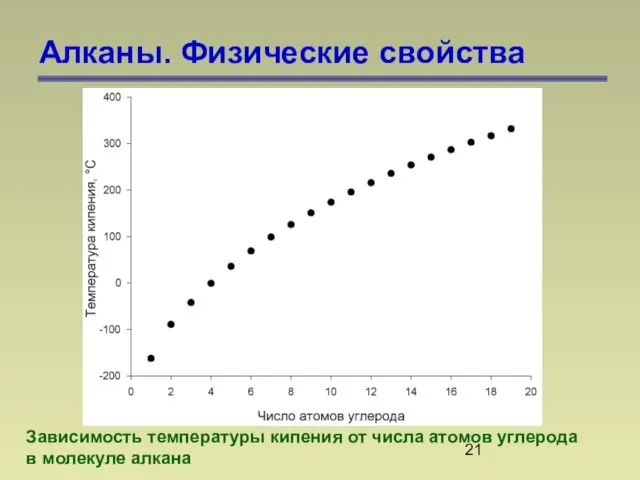
- 21. Алканы. Физические свойства Зависимость температуры кипения от числа атомов углерода в молекуле алкана
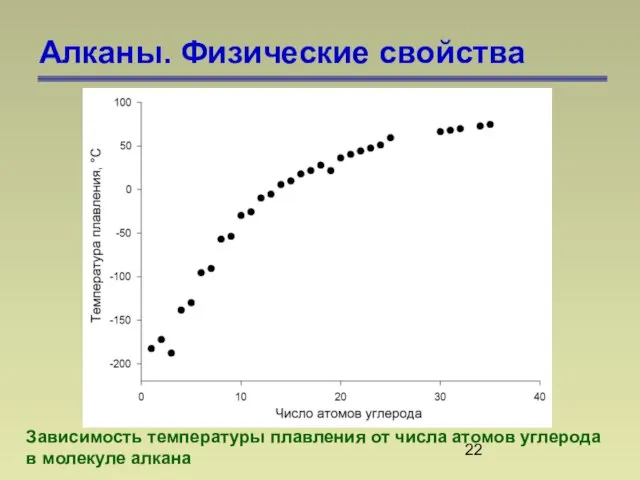
- 22. Алканы. Физические свойства Зависимость температуры плавления от числа атомов углерода в молекуле алкана
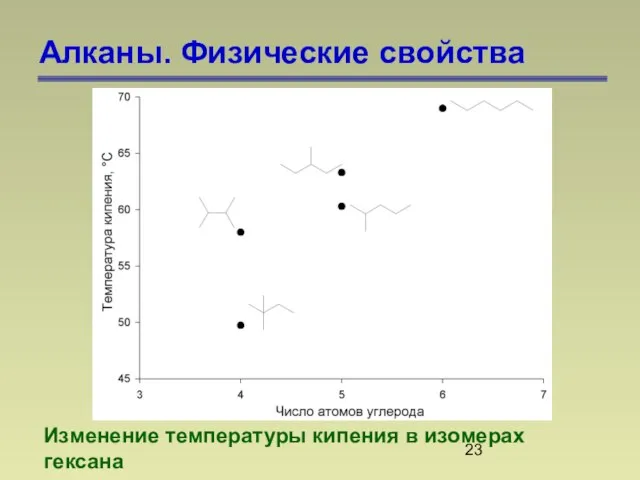
- 23. Алканы. Физические свойства Изменение температуры кипения в изомерах гексана
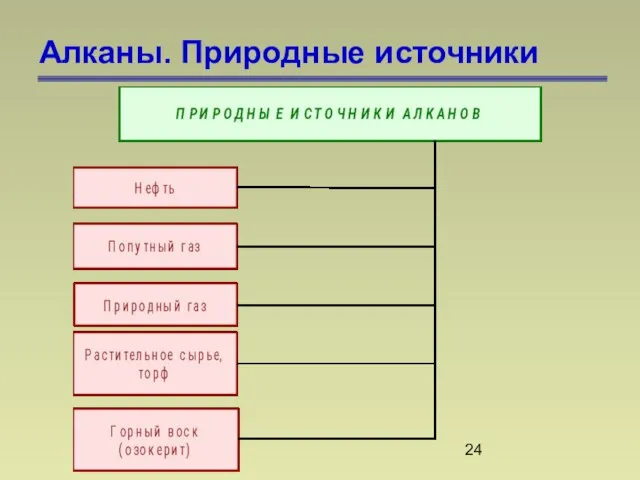
- 24. Алканы. Природные источники
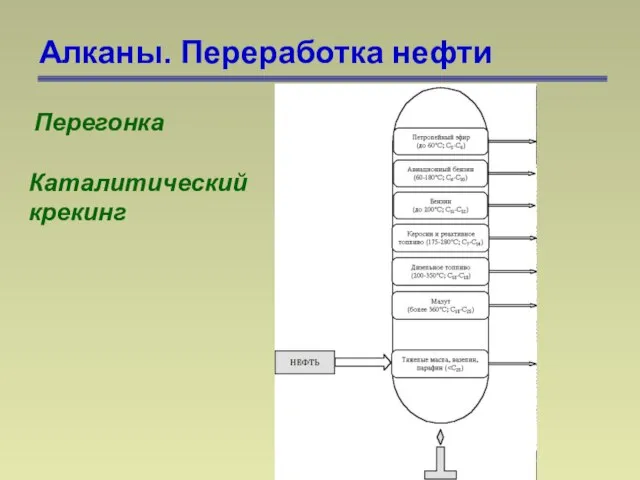
- 25. Алканы. Переработка нефти Перегонка Каталитический крекинг
- 26. Алканы. Способы получения Газофикация угля (Бертло, 1869) Сжижение угля
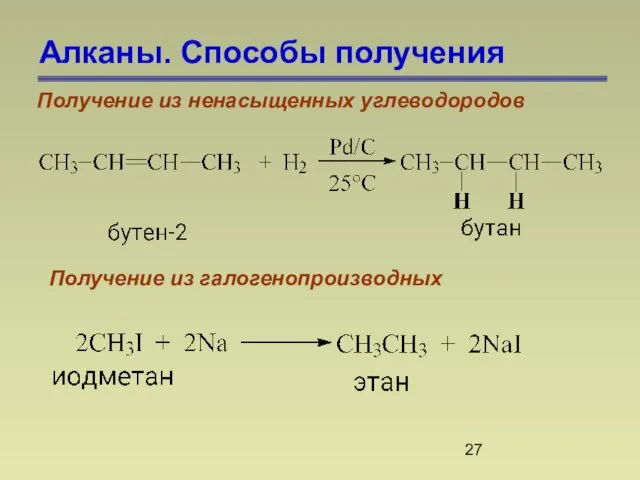
- 27. Алканы. Способы получения Получение из ненасыщенных углеводородов Получение из галогенопроизводных
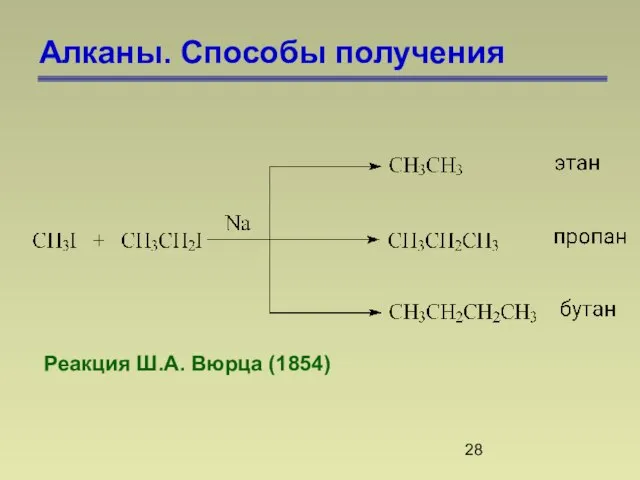
- 28. Алканы. Способы получения Реакция Ш.А. Вюрца (1854)
- 29. Алканы. Способы получения Восстановление галогеналканов
- 30. Алканы. Способы получения Получение из солей карбоновых кислот Электролиз солей щелочных металлов и карбоновых кислот (реакция
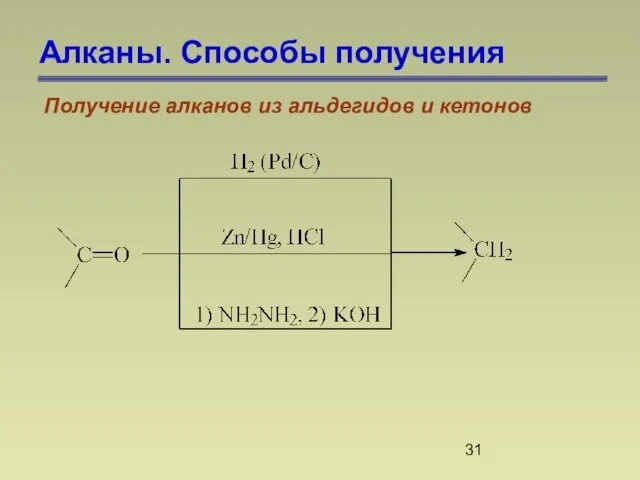
- 31. Алканы. Способы получения Получение алканов из альдегидов и кетонов
- 32. Алканы. Способы получения Гидролиз карбидов металлов 1) Карбиды, при гидролизе, которых образуется метан. (Карбиды алюминия и
- 33. Алканы. Химические свойства Галогенирование
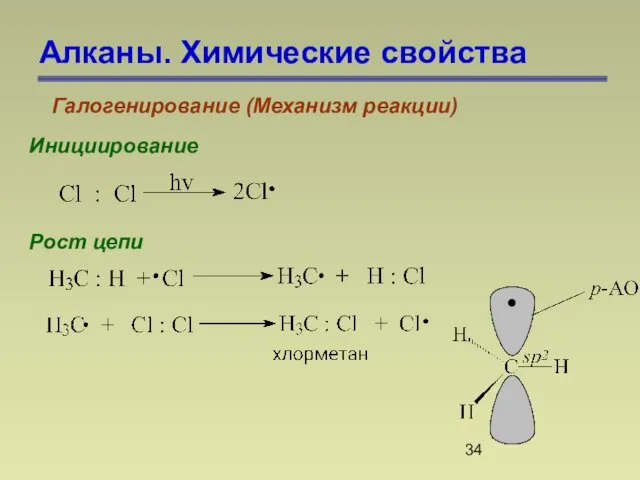
- 34. Алканы. Химические свойства Галогенирование (Механизм реакции) Инициирование Рост цепи
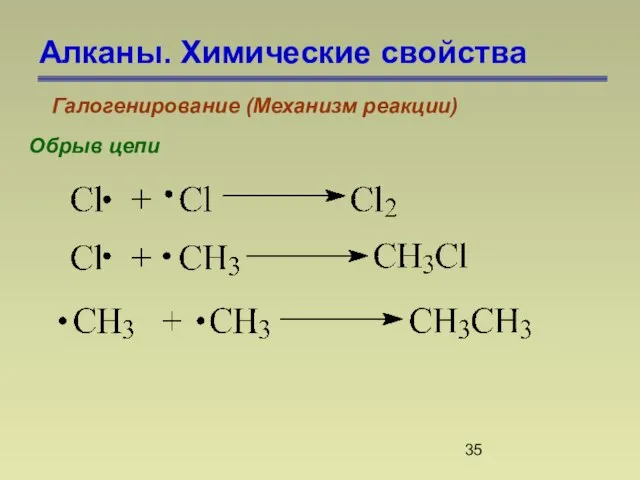
- 35. Алканы. Химические свойства Галогенирование (Механизм реакции) Обрыв цепи
- 36. Алканы. Химические свойства Галогенирование (Механизм реакции) 1.Галогенирование начинается только под действием инициатора радикальных реакций (УФ-свет, радикальные
- 37. Алканы. Химические свойства Галогенирование (Механизм реакции) 4. Реакционная способность водорода у третичного атома углерода выше, чем
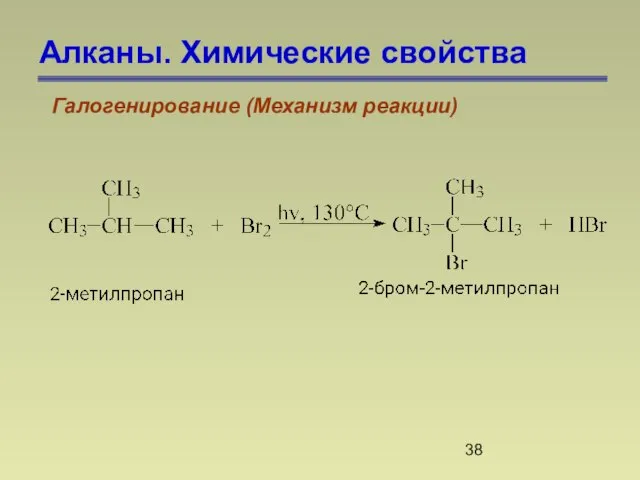
- 38. Алканы. Химические свойства Галогенирование (Механизм реакции)
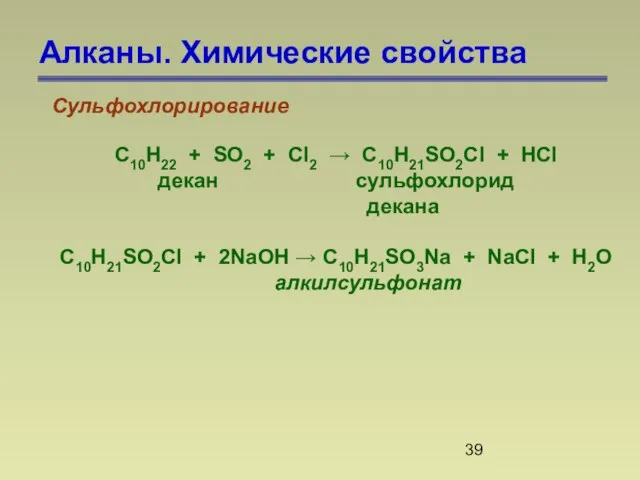
- 39. Алканы. Химические свойства Сульфохлорирование С10H22 + SO2 + Cl2 → C10H21SO2Cl + HCl декан сульфохлорид декана
- 40. Алканы. Химические свойства Нитрование Реакция М.И. Коновалова
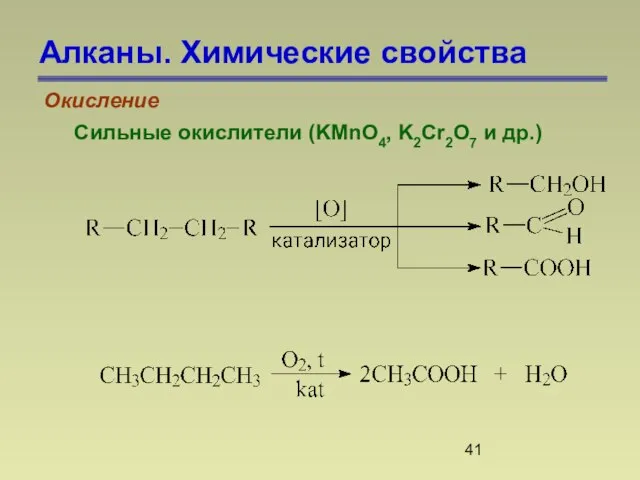
- 41. Алканы. Химические свойства Окисление Сильные окислители (KMnO4, K2Cr2O7 и др.)
- 42. Алканы. Химические свойства Окисление CH4 + H2O → CO + 3H2 CH4 + ½O2 → CO
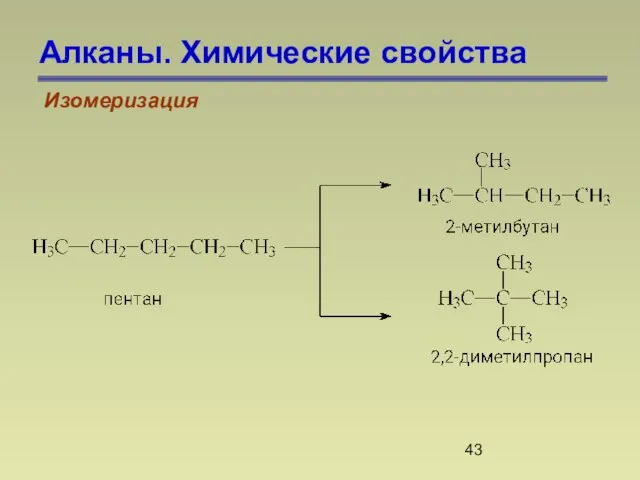
- 43. Алканы. Химические свойства Изомеризация
- 44. Алканы. Химические свойства Термическое разложение (Крекинг) В.Г. Шухов (1891) Температура – 470—650°С; Давление – 7 МПа
- 45. Алканы. Химические свойства Каталитический крекинг Катализаторы – АlСl3, Сr2О3, алюмосиликаты; Температура – 470—500°С; Давление 0,01—0,1 МПа
- 47. Скачать презентацию



















 Презентация на тему Политика и власть
Презентация на тему Политика и власть  6. СВН 2020
6. СВН 2020 The structure of the body
The structure of the body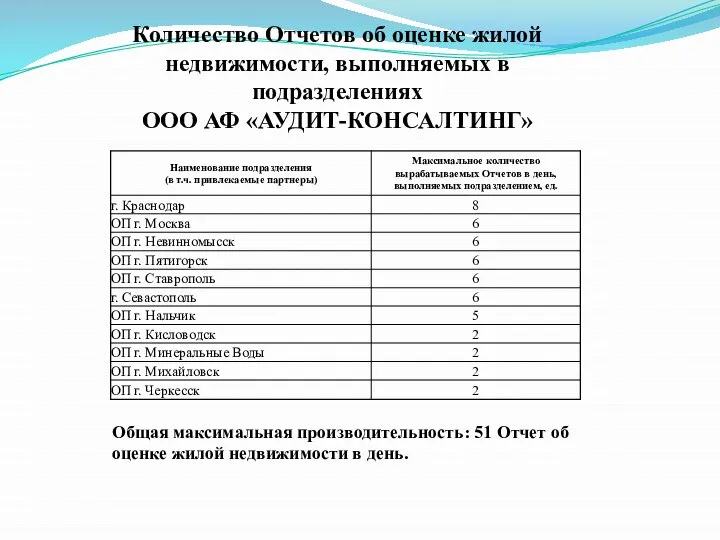 Количество Отчетов об оценке жилой недвижимости, выполняемых в подразделениях ООО АФ АУДИТ-КОНСАЛТИНГ
Количество Отчетов об оценке жилой недвижимости, выполняемых в подразделениях ООО АФ АУДИТ-КОНСАЛТИНГ УПРАВЛЕНЧЕСКИЙКОНСАЛТИНГ
УПРАВЛЕНЧЕСКИЙКОНСАЛТИНГ Презентация на тему орган зрения
Презентация на тему орган зрения Metodiki_yur_AKZS
Metodiki_yur_AKZS Пушкинская карта
Пушкинская карта Мой милый маг, моя Мария, - Мечтам мерцающий маяк. Мятежны марева морские, Мой милый маг, моя Мария, Молчаньем манит мутный мрак … Мне
Мой милый маг, моя Мария, - Мечтам мерцающий маяк. Мятежны марева морские, Мой милый маг, моя Мария, Молчаньем манит мутный мрак … Мне 3 года младший дошкольник
3 года младший дошкольник Правовая защита экологии в Беларуси
Правовая защита экологии в Беларуси Хирургическое_лечение_преждевременной_эякуляции
Хирургическое_лечение_преждевременной_эякуляции Столетие бедствий
Столетие бедствий Памятка по прямым выплатам ФСС
Памятка по прямым выплатам ФСС «Конституция –основной законгосударства»
«Конституция –основной законгосударства» Замечания заказчика
Замечания заказчика Презентация на тему Реализация ФГОС в работе школьной библиотеки. Воспитание культурного и гражданского самосознания учащихся.
Презентация на тему Реализация ФГОС в работе школьной библиотеки. Воспитание культурного и гражданского самосознания учащихся. Характерные особенности тактической подготовки баскетболистов при игре в защите
Характерные особенности тактической подготовки баскетболистов при игре в защите Презентация на тему Великий круговорот жизни 3 класс
Презентация на тему Великий круговорот жизни 3 класс (005)Pulser Test Form
(005)Pulser Test Form Культурные и сорные растения поля
Культурные и сорные растения поля Устное народное творчество Урала.
Устное народное творчество Урала. Презентация на тему Евглена Зеленая
Презентация на тему Евглена Зеленая  Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Землетрясения Подготовила презентацию студентка 1ого курса ЭФ Группы Э112Б Олефир Карина
Землетрясения Подготовила презентацию студентка 1ого курса ЭФ Группы Э112Б Олефир Карина Apģērbs. Apģērba materiāli
Apģērbs. Apģērba materiāli Евгений Гришковец
Евгений Гришковец Вахта памяти в канун 74-й годовщины великой победы
Вахта памяти в канун 74-й годовщины великой победы