Содержание
- 2. Цель презентации: Применить физический закон к различным процессам на основе имеющихся знаний; Работать над формированием сравнивать
- 3. Закон сохранения и превращения энергии, распространённый на тепловые явления, называется первым законом термодинамики Изменение внутренней энергии
- 4. Если учитывать различие только в знаках между работой внешней и внутренней сил А=-А`, получим первый закон
- 5. Невозможность вечного двигателя! Вечный двигатель—устройство, способное совершать неограниченное количество работы без затрат топлива или каких-либо других
- 6. Первый закон термодинамики можно применить к газовым законам При изохорном процессе V=const, поэтому A`=0. Тогда изменение
- 7. 3.При изотермическом процессе Т=const, внутренняя энергия газа не меняется ∆U=0 , переданное газу количество теплоты идёт
- 9. Скачать презентацию






 Утилизация шлама в оксид магния и карналлит
Утилизация шлама в оксид магния и карналлит Суточный биоритм
Суточный биоритм Тазове передлежання плода: ведення вагітності та пологів
Тазове передлежання плода: ведення вагітності та пологів  Методические рекомендации по работе над творческим проектом
Методические рекомендации по работе над творческим проектом Очистители топливной системы, впускного клапана и распылителя форсунки
Очистители топливной системы, впускного клапана и распылителя форсунки до встречи 1 сентября!
до встречи 1 сентября! Welcome box. Наша история
Welcome box. Наша история Кризисные ситуации и методы их преодоления ( нет подростковому суициду)
Кризисные ситуации и методы их преодоления ( нет подростковому суициду) К ЗВЕЗДАМ !
К ЗВЕЗДАМ ! Итальянская школа Геоэкономики
Итальянская школа Геоэкономики ва
ва Искусство – образная модель мира
Искусство – образная модель мира БИБЛИОТЕКА ГОУ ДПО ПОИПКРО
БИБЛИОТЕКА ГОУ ДПО ПОИПКРО Технические регламенты
Технические регламенты открытая тз (2)
открытая тз (2) Логистическая компания АРЭС
Логистическая компания АРЭС The Incredible Sun
The Incredible Sun  Государственная символика РОССИИ и КБР
Государственная символика РОССИИ и КБР Презентация на тему Ограниченность ресурсов. Кривая производственных возможностей
Презентация на тему Ограниченность ресурсов. Кривая производственных возможностей Растения сада
Растения сада Декоративный натюрморт Коми мотив
Декоративный натюрморт Коми мотив Гидроизоляция блочного фундамента (включая демонтаж)
Гидроизоляция блочного фундамента (включая демонтаж)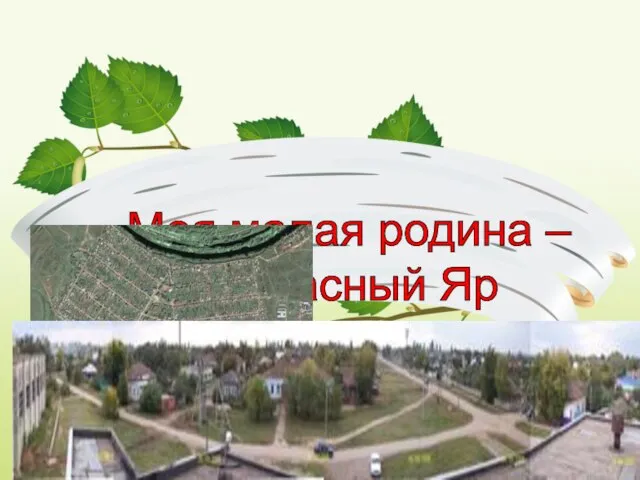 Моя малая родина – село Красный Яр
Моя малая родина – село Красный Яр Рыцари средневековья
Рыцари средневековья Презентация на тему Теория вероятностей
Презентация на тему Теория вероятностей  Модуль вывода унифицированных аналоговых сигналов ТПТС55.1663
Модуль вывода унифицированных аналоговых сигналов ТПТС55.1663 Mykola Platonovich Bazhan
Mykola Platonovich Bazhan Индукционный нагрев
Индукционный нагрев