Содержание
- 3. Кислоты Тема урока: «Химические свойства кислот с позиции теории электролитической диссоциации». «От кислых яблок сразу скисну».
- 4. Кислота, когда здорова, Угостить друзей готова Тем, что ей дала природа - Катионом водорода! Н+ Н+
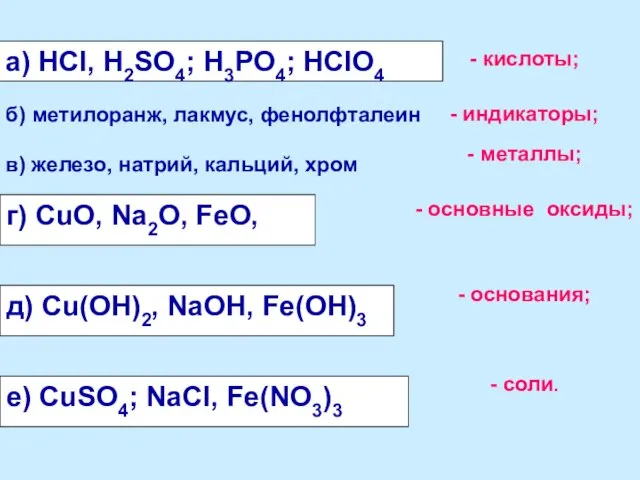
- 5. а) НСl, H2SO4; H3PO4; HClO4 - кислоты; - индикаторы; - металлы; - основные оксиды; - основания;
- 6. Задачи урока Образовательная: изучить химические свойства кислот с позиции теории электролитической диссоциации. 2. Развивающие (формирование и
- 7. Планируемые результаты обучения В результате изучения данного материала учащиеся должны: Знать: а) определение понятий – электролиты,
- 8. Лабораторный опыт №3 Каковы химические свойства кислот? Почему кислоты обладают сходными химическими свойствами?
- 9. Правила техники безопасности Осторожно обращайтесь с химическим оборудованием! Запрещается пробовать вещества на вкус (а); брать вещества
- 10. Цели: проделать реакции, характерные для кислот на примере серной кислоты, соляной кислоты. сделать вывод о химических
- 11. Взаимодействие кислот с индикаторами Красный
- 12. Взаимодействие кислот с металлами
- 13. Взаимодействие кислот с основными оксидами
- 14. Взаимодействие кислот с основаниями
- 15. Взаимодействие кислот с солями
- 16. Содержание I. Определение кислот. II. Химические свойства кислот. Взаимодействие кислот: 1) с индикаторами; 2) с металлами,
- 17. «Воспоминание о лете» Погадаем на ромашке: «Взаимодействует – не взаимодействует?» Задание С какими из веществ взаимодействует
- 18. «Сами трудясь, вы многое сделаете для себя и для близких, а если при труде успеха не
- 19. О кислотных дождях Оксиды азота, серы содержатся в выхлопных газах реактивных двигателей и двигателей внутреннего сгорания,
- 20. Кислотные дожди виноваты в исчезновении рыбы во многих реках и озёрах, так как рыба не выдерживает
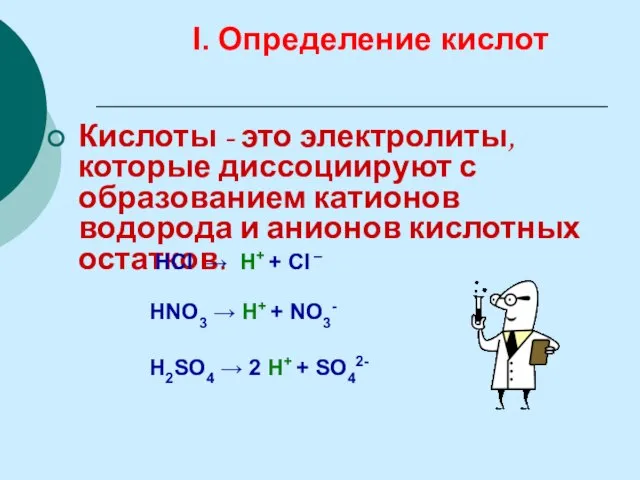
- 21. Кислоты - это электролиты, которые диссоциируют с образованием катионов водорода и анионов кислотных остатков. I. Определение
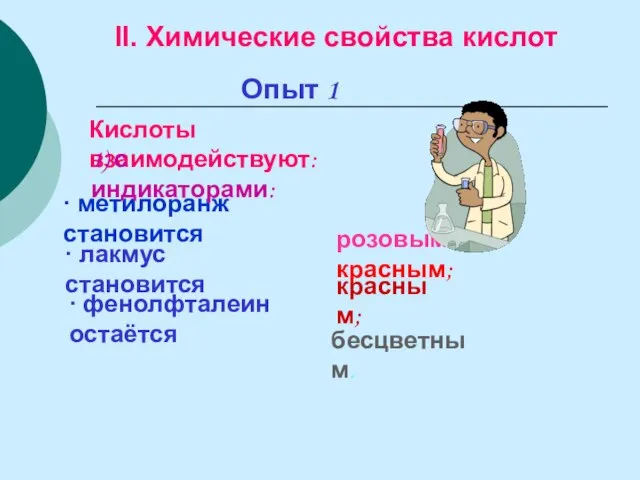
- 22. Опыт 1 Кислоты взаимодействуют: II. Химические свойства кислот ∙ метилоранж становится ∙ фенолфталеин остаётся розовым или
- 23. Опыт 2 2) с металлами, стоящими в ряду напряжений металлов до водорода (исключение составляют азотная и
- 24. 3) с основными оксидами с образованием соли и воды СаО + 2НСl → CaCl2 + H2O
- 25. 4) с основаниями с образованием соли и воды Cu (OH)2 + 2HCl → CuCl2 + H2O
- 26. 5) с солями (реакция возможна, если выпадает осадок или выделяется газ) СаСО3 + 2НСl → CaCl2
- 27. Литература: Мартыненко Б.В. Кислоты – основания. Аликберова Л.Ю.Занимательная химия.-М.:Аст-Пресс, 1999. Савина Л.А. Я познаю мир. Химия.-
- 29. Скачать презентацию























 Презентация на тему Километр (3 класс)
Презентация на тему Километр (3 класс) Известные имена. Софья Ковалевская
Известные имена. Софья Ковалевская Особенности кризиса 2008-2ХХХгг.
Особенности кризиса 2008-2ХХХгг. Графика
Графика Общие вопросы антибактериальной терапии
Общие вопросы антибактериальной терапии Составное глагольное сказуемое
Составное глагольное сказуемое Ch1 - Lecture2
Ch1 - Lecture2 Увеличительные приборы
Увеличительные приборы Болат өндірісінің теориясы мен технологиясы
Болат өндірісінің теориясы мен технологиясы Международные транспортные коридоры
Международные транспортные коридоры Гравюра
Гравюра Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци
Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци Кайнозойская эра
Кайнозойская эра Греция сегодня
Греция сегодня Алгоритм с ветвлением в среде программирования Turbo Pascal
Алгоритм с ветвлением в среде программирования Turbo Pascal ИСКУССТВО ОРИГАМИ
ИСКУССТВО ОРИГАМИ Параметры областного бюджета Тверской области на 2008-2010 годы
Параметры областного бюджета Тверской области на 2008-2010 годы 90 лет ГТО
90 лет ГТО Декоративные народные промыслы
Декоративные народные промыслы Возникновение и развитие логистики
Возникновение и развитие логистики PO
PO Композиция (от лат. compositio)
Композиция (от лат. compositio) Библиотека – как информационная база. Структура библиотеки ВГУЭС
Библиотека – как информационная база. Структура библиотеки ВГУЭС Психологические особенности младших школьников с общим недоразвитием речи
Психологические особенности младших школьников с общим недоразвитием речи Презентация на тему Эра космонавтики
Презентация на тему Эра космонавтики  Чернышов Вадим Геннадьевич. Сертификат участника
Чернышов Вадим Геннадьевич. Сертификат участника САПР ТП ВЕРТИКАЛЬ
САПР ТП ВЕРТИКАЛЬ История развития психопатологии в России
История развития психопатологии в России