Слайд 2Проект урока по теме «Соли»
Комбинированный
урок- практикум

Слайд 3Цели урока:
Знать классификацию солей. Уметь доказывать химические свойства солей, записывать уравнения реакций.
Воспитывать

целеустремленность в умении преодолевать трудности, уважении к творчеству в науке.
Развивать у учащихся логическое мышление, навыки самостоятельной работы.
Слайд 4Задачи урока:
Повторить формулировку определения солей.
Проверить умение учащихся применять знание формулировки в стандартной

ситуации.
Способствовать совершенствованию навыка учащихся составлять названия солей.
Слайд 5Проверка домашнего задания.
Осуществить превращения:
Ca Ca(OH)2 CaCO3

Слайд 6Проверка домашнего задания.
Ca+2 H2O Ca(OH)2+Н2
Налить воды. Подышать над раствором, появится осадок.
Ca(OH)2+ CO2

CaCO3+Н2О
Слайд 7Классификация солей
Нормальные, средние К2СО3,СаС12
Кислые NaHCO3, Ca(HCO3)2
Основные AI(OH)CL2
Двойные K2NaPO4

Слайд 8Физические свойства солей
Даны три соли. Описать внешний вид, определить растворимость.
CuSO4 CaCO3 FeCl3

Слайд 9Физические свойства солей
Даны три соли. Описать внешний вид, определить растворимость.
CuSO4 CaCO3 FeCl3
Голубые

кристаллы Белого цвета комочек Желтые кристаллы
Растворима Нерастворима Растворима
Слайд 10Химические свойства солей.
Соли взаимодействуют с металлами:
CuSO4+Fe FeSO4+Cu
Соли взаимодействуют с кислотами:
СaCO3+ 2Hcl Cacl2

+CO2+H2O
Соли взаимодействуют со щелочами
Fecl3+3NaOH Fe(OH)3+ 3Nacl
Слайд 11Химические свойства солей.
Нерастворимые соли при нагревании разлагаются
СaCO3 CaO+ CO2
Образование кристаллогидратов
CuSO4+ 5H2O CuSO4*5H2O

Слайд 12Тестовые задания.
1.Выписать отдельно по названиям.
1 вариант: хлориды и сульфаты.
2 вариант: нитраты и

карбонаты.
K2CO3, NaNO3, MgSO4, CuS, NaCl, CaCO3,
H2SO3, ZnCl2, Ca(NO3)2, LiNO3, BaSO4, KOH
2.Выберите растворимую соль из данных выше:1 вариант- нитрат, 2 вариант- хлорид.











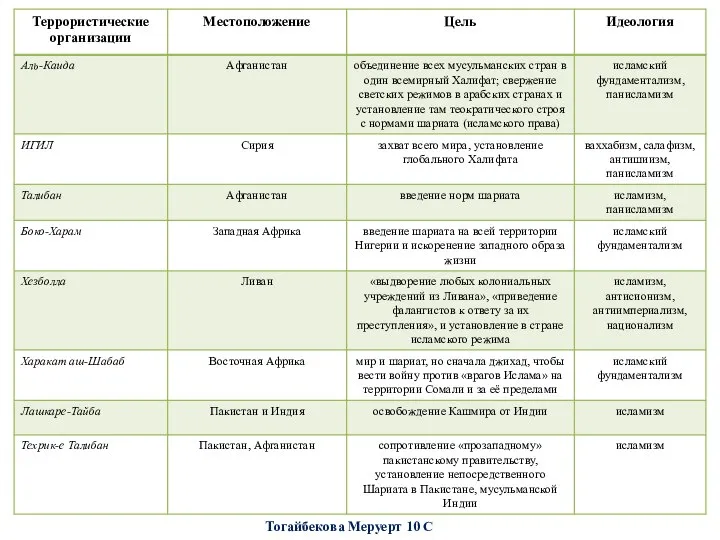 Террористические организации
Террористические организации Викторина по русским народным сказкам и сказкам А.Пушкина
Викторина по русским народным сказкам и сказкам А.Пушкина Какой я
Какой я Развитие психики и сознания
Развитие психики и сознания Рони Ритшель
Рони Ритшель Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия
Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия Защита информации от несанкционированного доступа
Защита информации от несанкционированного доступа Стратегический менеджмент в условиях спонтанных изменений
Стратегический менеджмент в условиях спонтанных изменений Я - личный помощник. Измени себя и свою жизнь
Я - личный помощник. Измени себя и свою жизнь Зодчество Древней Греции.
Зодчество Древней Греции. Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики
Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики  Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В
Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В  Карликовая игрунка или пальчиковая обезьяна (Finger Monkey)
Карликовая игрунка или пальчиковая обезьяна (Finger Monkey) ТЕМА 3
ТЕМА 3 МАТЕРИНСТВО И ОТЦОВСТВО
МАТЕРИНСТВО И ОТЦОВСТВО Глагол. Урок-обобщение
Глагол. Урок-обобщение Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация
Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация Люблю берёзку русскую
Люблю берёзку русскую Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО
Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО Фотоклуб Перспектива
Фотоклуб Перспектива Die Aufgabe “d”
Die Aufgabe “d” Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул
Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул Основы грузовой и коммерческой работы
Основы грузовой и коммерческой работы Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной
Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной  13 признаков учителя
13 признаков учителя Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев
Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев Термические ожоги (5 класс)
Термические ожоги (5 класс) Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя
Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя