Слайд 2Тест
5. Причина свечения белого фосфора….
а)изменение агрегатного состояния вещества
б) химическое явление в) физическое

явление
б) химическое явление
6.Как называются соединения фосфора с металлами
а) сульфаты б)фосфаты в) фосфиды
в) фосфиды
7.Какой тип связи в молекуле фосфина РН3
а) ковалентная неполярная б) ковалентная полярная в) ионная
а) ковалентная неполярная
8) Красный или белый фосфор ядовит?
а) красный б) белый
б) белый
9) Очень ядовит, с неприятным запахом, легко воспламеняется на воздухе, образует болотные блуждающие огни. О каком газе идет речь?
О фосфине РН3
Слайд 3Фосфор
Соединения фосфора
химия 9 класс
Prezentacii.com

Слайд 4План
Оксид фосфора - Р2О5
Фосфорная кислота - Н3РО4
Соли фосфорной кислоты –
Са3

(РО4)3 Са(Н2РО4)2 СаНРО4
Слайд 5Фосфор в природе
В природе фосфор в свободном виде не встречается – только

в виде соединений. Важнейшими природными соединениями фосфора являются минералы фосфориты и апатиты.
Основную их массу составляет фосфат кальция Са3 (РО4)3, из которого и получают в промышленности фосфор.
Слайд 6Кислотный оксид Р2О5
Физические свойства
Белое гигроскопичное порошкообразное вещество.
Хорошо растворимое в воде, образует

несколько кислот.
Используется как осушитель газов и жидкостей, отнимает воду у химических соединений.
Слайд 7Кислотный оксид Р2О5
Химические свойства
1) с водой
Р2О5 + 3 Н2О = 2Н3РО4

(ортофосфорная кислота)
Р2О5 + Н2О = 2НРО3
(метафосфорная кислота)
Р2О5 + 2 Н2О = Н4Р2О7
(пирофосфорная кислота)
Слайд 8Кислотный оксид Р2О5
Химические свойства
2) с основными оксидами
Р2О5 + 3 СаО = Са3
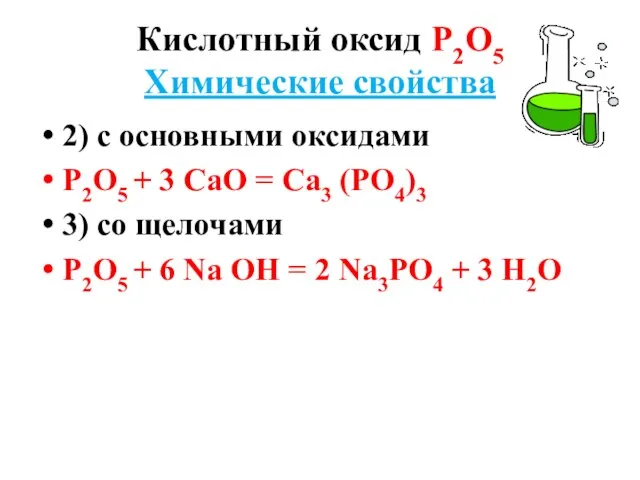
(РО4)3
3) со щелочами
Р2О5 + 6 Nа ОН = 2 Nа3РО4 + 3 Н2О
Слайд 9
Ортофосфорная кислота Н3РО4
Физические свойства
Белые прозрачные кристаллы,
не ядовита
Кислота средней силы
С

водой смешивается в любых соотношениях.
Тплав. = 42 0С, плавиться без разложения, при умеренном нагревании разлагается.
Окислительные свойства не проявляет (отличие от Н2SO4 (конц.), НNO3)
Слайд 10
Ортофосфорная кислота Н3РО4
Является трехосновной кислотой и образует три ряда солей:
1) средние соли,

или фосфаты - Са3 (РО4)3
Которые нерастворимы в воде, кроме фосфатов щелочных металлов
2) Кислые-дигидрофосфаты- Са(Н2РО4)2
Большинство из которых хорошо растворимы в воде
Слайд 11Ортофосфорная кислота Н3РО4
3) Кислые-гидрофосфаты- СаНРО4
Которые малорастворимы в воде (кроме фосфатов натрия,

калия и аммония), т.е. занимают промежуточное положение между фосфатами и дигидрофосфатами по растворимости.
Вывод: с увеличением содержания атомов водорода в молекуле соли, ее растворимость повышается.
Слайд 12
Ортофосфорная кислота Н3РО4
Химические свойства
Н3РО4 проявляет все свойства кислот
Реагирует:
1) со щелочами:

NaOH, КОН
2) с основными оксидами: Li2O, Na2O
3) c солями: К2СО3
4) с металлами не реагирует !!! ?
(см.Таблицу растворимости)
Слайд 13
Ортофосфорная кислота Н3РО4
Химические свойства
Фосфаты всех металлов (КромеЩМе) нерастворимы, поэтому на

поверхности этих металлов образуется нерастворимая пленка, препятствующая их дальнейшему растворению в кислоте.
ЩМе при растворении в кислоте, начинают взаимодействовать с водой.
Слайд 14Ортофосфорная кислота Н3РО4
Химические свойства
Некоторые реакции с металлами протекают в очень разбавленных

растворах:
2 Н3РО4 (разб) + 3 Мg = Мg3(РО4 )2↓ + 3Н2↑
Слайд 15Качественная реакция
на фосфат-ион РО43-
РО43- + 3 Ag+ = Ag3РО4 ↓

(желтый фосфат серебра)
Полученный осадок растворяется в сильных кислотах.
По этому признаку его можно отличить от других нерастворимых солей серебра желтого цвета – AgI, AgBr
AgCl – белого цвета
Слайд 16
Задание
Напишите уравнение диссоциации солей
Фосфата натрия
Гидрофосфата натрия
Дигидрофосфата натрия
Обратите внимание: средние соли диссоциируют

в 1 ступень (сильные электролиты), у кислых солей – несколько ступеней диссоциации.
Слайд 17Диссоциация солей фосфора
Вывод: Каждая последующая ступень диссоциации протекает в меньшей степени, чем

предыдущая.
Слайд 18Источники
Горковенко М.Ю. Поурочные разработки по химии: 9 класс. – М.: ВАКО, 2010.

– 368 с. – (В помощь школьному учителю).
Габриелян О.С. Химия. 9 класс: учеб. Для общеобразоват.учреждений/О.С.Габриелян. – 17-е изд.Б стереотип. –М.: Дрофа, 2010 – 270 с.:ил.

















 ПОРТОВАЯ ОСОБАЯ ЭКОНОМИЧЕСКАЯ ЗОНА НА ТЕРРИТОРИИ МУНИЦИПАЛЬНОГО ОБРАЗОВАНИЯ «ЧЕРДАКЛИНСКИЙ РАЙОН» УЛЬЯНОВСКОЙ ОБЛАСТИ
ПОРТОВАЯ ОСОБАЯ ЭКОНОМИЧЕСКАЯ ЗОНА НА ТЕРРИТОРИИ МУНИЦИПАЛЬНОГО ОБРАЗОВАНИЯ «ЧЕРДАКЛИНСКИЙ РАЙОН» УЛЬЯНОВСКОЙ ОБЛАСТИ Бизнес-центр ВОМЗ
Бизнес-центр ВОМЗ скелет человека
скелет человека Елементи вишивки у сучасному інтер'єрі. 5 клас
Елементи вишивки у сучасному інтер'єрі. 5 клас Презентация на тему Экскурсия в зоопарк
Презентация на тему Экскурсия в зоопарк Газета «Новое поколение »
Газета «Новое поколение » Техника (нормотворческая техника) в сфере правотворчества
Техника (нормотворческая техника) в сфере правотворчества Развивайка Природа
Развивайка Природа История праздника Новый год на Руси
История праздника Новый год на Руси Summer holidays
Summer holidays Presentation china
Presentation china Логические основы компьютера. Логические схемы
Логические основы компьютера. Логические схемы Что такое мужество…
Что такое мужество… 30 Чечель
30 Чечель Эндокринопатии и рак молочной железы
Эндокринопатии и рак молочной железы Выставка декоративно-прикладного творчества инвалидов по зрению Курганской областной
Выставка декоративно-прикладного творчества инвалидов по зрению Курганской областной Веселой Масленицы!
Веселой Масленицы! Масло AOC с перерабатывающей фабрики Le petit olivier
Масло AOC с перерабатывающей фабрики Le petit olivier Скажем нет подростковой преступности
Скажем нет подростковой преступности Технология пайки печатных плат с использованием ИК-нагрева
Технология пайки печатных плат с использованием ИК-нагрева Презентация на тему Зерновые культуры
Презентация на тему Зерновые культуры  Программное обеспечение для поддержки информационной бизнес-аналитики
Программное обеспечение для поддержки информационной бизнес-аналитики Депрессия и подросток
Депрессия и подросток Популяризация статистики в Вологодской области
Популяризация статистики в Вологодской области К вопросу о качестве общего образования:
К вопросу о качестве общего образования: Культура Южной Кореи
Культура Южной Кореи Презентация на тему Условия прорастания семян
Презентация на тему Условия прорастания семян  День России
День России