Содержание
- 2. Гидролиз – это реакции обменного Взаимодействия вещества с водой, приводящие к их разложению. Гидролизу подвергаются соединения
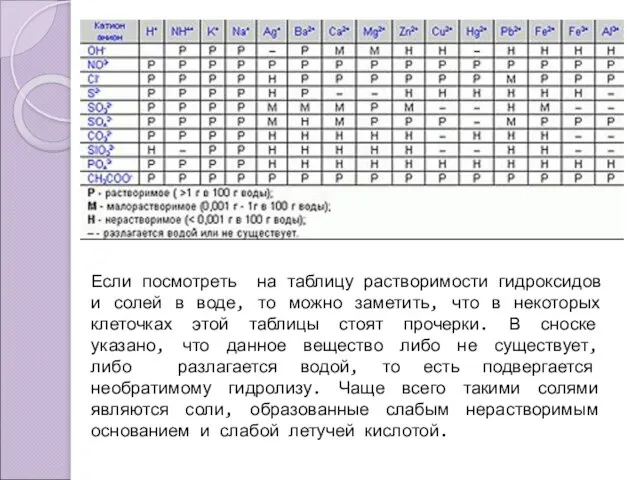
- 3. Если посмотреть на таблицу растворимости гидроксидов и солей в воде, то можно заметить, что в некоторых
- 4. Гидролиз солей Взаимодействие ионов соли с водой, приводящее к образованию молекул слабого электролита, называют гидролизом солей.
- 5. Количественной характеристикой Гидролиза солей может служить степень гидролиза (a), определяемая отношением концентрации гидролизованной части молекул к
- 6. Частичный Гидролиз трёхкальциевого силиката является причиной выделения свободной извести при взаимодействии портландцемента с водой (см. Цемент).
- 7. Различают несколько вариантов гидролиза солей: 1. Гидролиз соли слабой кислоты и сильного основания: Na2CO3 + Н2О
- 8. Гидролиз - процесс обратимый. Повышение концентрации ионов водорода и гидроксид-ионов препятствует протеканию реакции до конца. Параллельно
- 9. При гидролизе жиров в присутствии щелочей получают мыла. Гидролиз жиров в присутствии катализаторов применяется для получения
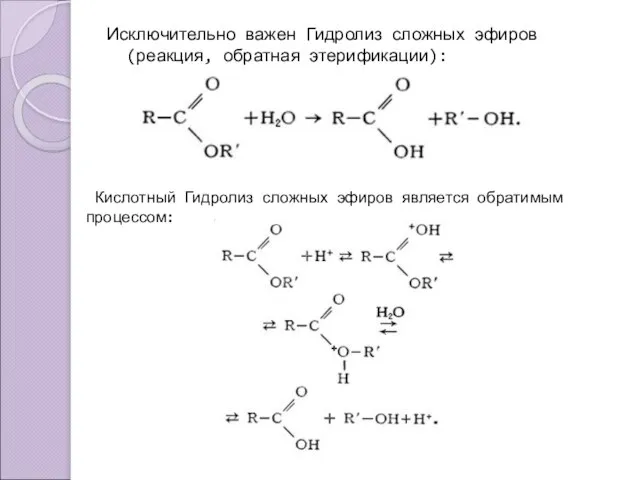
- 10. Исключительно важен Гидролиз сложных эфиров (реакция, обратная этерификации): Кислотный Гидролиз сложных эфиров является обратимым процессом:
- 11. Термин «Гидролиз» обычно применяется в органической химии также по отношению к некоторым процессам, которые более правильно
- 13. Скачать презентацию







 Любимые герои любимых сказок
Любимые герои любимых сказок М.И.Глинка-основоположник русской классической музыки
М.И.Глинка-основоположник русской классической музыки Страховое дело. Лекция 3
Страховое дело. Лекция 3 Песенка seasons
Песенка seasons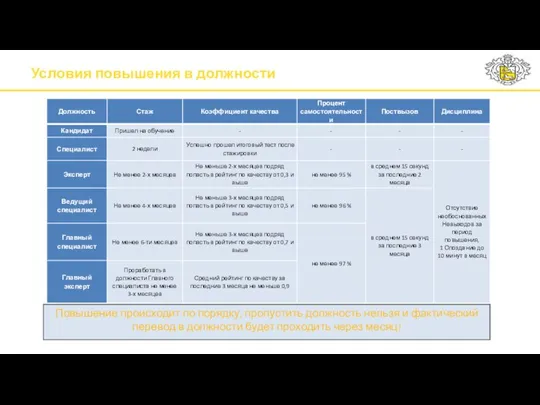 Условия повышения в должности
Условия повышения в должности Океания
Океания Формирование и ведение бюджетной сметы в системе Электронный бюджет
Формирование и ведение бюджетной сметы в системе Электронный бюджет Красная линия «Остановим СПИД вместе»
Красная линия «Остановим СПИД вместе» Презентация на тему Стандартный вид числа
Презентация на тему Стандартный вид числа  Забелина Марина Анатольевна
Забелина Марина Анатольевна Ваше спасение в борьбе с болью в спине. Главная страница Hang Ups
Ваше спасение в борьбе с болью в спине. Главная страница Hang Ups ПРОГРАМНЫЙ ПАКЕТ«ЛОГИКА И СХЕМОТЕХНИКА»
ПРОГРАМНЫЙ ПАКЕТ«ЛОГИКА И СХЕМОТЕХНИКА» Презентация на тему Рождение театра
Презентация на тему Рождение театра «Весь мир у нас в руках, мы звезды континентов», - поют герои легендарного мюзикла «Бременские музыканты». А вместе с ними отлично п
«Весь мир у нас в руках, мы звезды континентов», - поют герои легендарного мюзикла «Бременские музыканты». А вместе с ними отлично п Техника метания малого мяча
Техника метания малого мяча Улучшение диагностики проблем отправки и получения писем
Улучшение диагностики проблем отправки и получения писем Презентация на тему Остров Врангеля
Презентация на тему Остров Врангеля Обзор решения «Транспортная логистика и экспедирование»
Обзор решения «Транспортная логистика и экспедирование» Practical Phonetics Speech Fluency Orthography Pronunciation
Practical Phonetics Speech Fluency Orthography Pronunciation Избирательное право9 класс
Избирательное право9 класс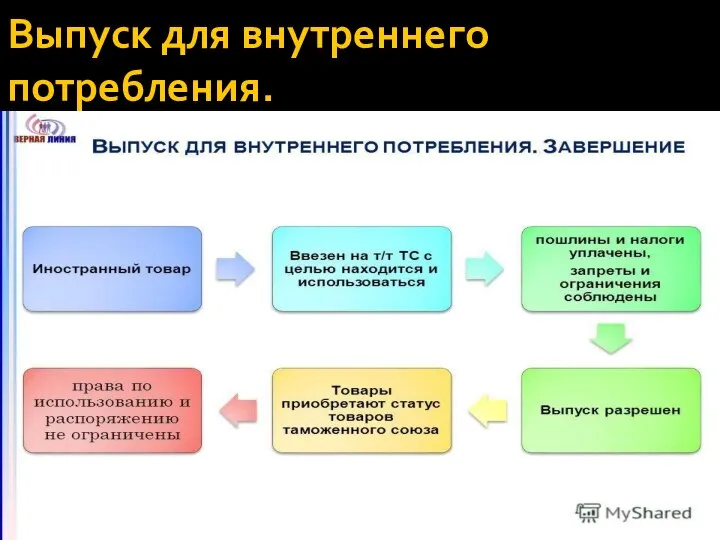 Выпуск для внутреннего потребления
Выпуск для внутреннего потребления Быстрые результаты. Start up. Тайм-менеджмент. Freelance
Быстрые результаты. Start up. Тайм-менеджмент. Freelance Оползни, обвалы, селевые потоки
Оползни, обвалы, селевые потоки Тема урока:Климатообразующие факторы
Тема урока:Климатообразующие факторы Урок литературного чтения в 4 классе
Урок литературного чтения в 4 классе Тактические схемы для урочных и внеурочных занятиях по теме: Нападение через центрового
Тактические схемы для урочных и внеурочных занятиях по теме: Нападение через центрового SMS Alert Gateway Техническая информация
SMS Alert Gateway Техническая информация Танцы народов мира
Танцы народов мира