Содержание
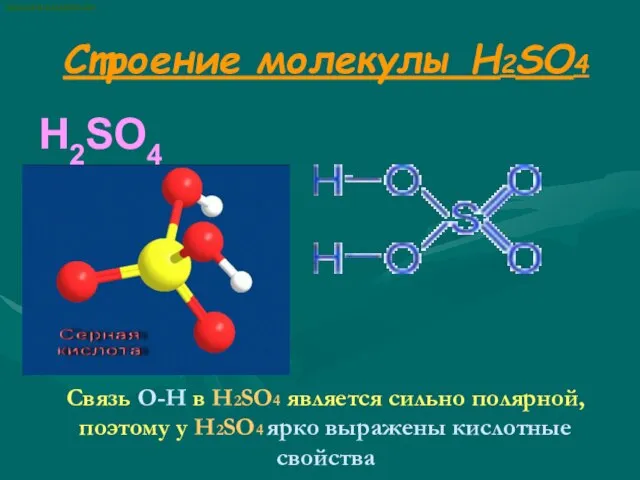
- 2. Строение молекулы H2SO4 H2SO4 Связь О-Н в H2SO4 является сильно полярной, поэтому у H2SO4 ярко выражены
- 3. Производство серной кислоты 1-я стадия. Печь для обжига колчедана. 4FeS2 + 11O2 => 2Fe2O3 + 8SO2
- 4. Физические свойства Тяжелая маслянистая жидкость ("купоросное масло"); p = 1,84 г/см3; Нелетучая, хорошо растворима в воде
- 5. Химические свойства H2SO4 - сильная двухосновная кислота H2SO4 ⬄ H+ + HSO4- ⬄2H+ + SO42- 1)
- 6. 3) с основаниями: H2SO4 + 2NaOH => Na2SO4 + 2H2O H+ + OH- => H2O H2SO4
- 7. ВАСИЛИЙ КАДЕВИЧ 2008 5) концентрированная H2+6SO4 – сильный окислитель; при взаимодействии с металлами (кроме Au, Pt)
- 8. 6) концентрированная H2S+6O4 реагирует при нагревании с некоторыми неметаллами за счет своих сильных окислительных свойств, превращаясь
- 9. 6) Гигроскопичность серной кислоты Концентрированная серная кислота жадно набирает воду отовсюду, образуя гидраты, и способна для
- 10. Концентрированная серная кислота энергично обугливает сахарозу
- 12. Помните! При приготовлении раствора кислоту вливать малыми порциями в воду, а не наоборот!
- 13. В природе встречается 180 минералов сульфатов, и на их долю приходится ~0,5 % массы земной коры.
- 14. Серная кислота в природе Кислые озёра
- 15. Существуют предположения, что кислотное озеро возникло сравнительно недавно в результате извержения, произошедшего незаметно для людей. Тот,
- 16. Серная кислота – очень активная жидкость, особенно концентрированная, которая реагирует со многими неорганическими веществами, также она
- 17. ВАСИЛИЙ КАДЕВИЧ 2008 Применение H2SO4 В производстве пластмассы В производстве синтетического волокна В средствах защиты растений
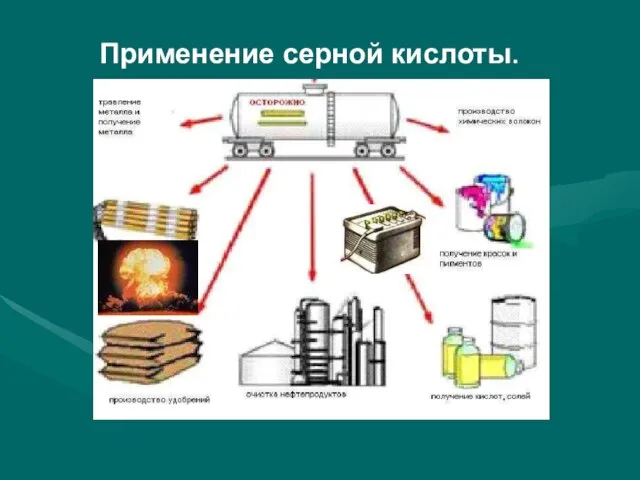
- 18. Применение серной кислоты.
- 19. Сульфат меди
- 20. Сульфат натрия.
- 21. Сульфат натрия.
- 22. СОЛИ СЕРНОЙ КИСЛОТЫ CaSO4• 2H2O - гипс CaSO4• 0,5H2O - алебастр CuSO4• 5H2O – медный купорос
- 23. Домашнее задание Составьте инструкцию по правилам обращения с серной кислотой • для лаборанта кабинета химии; •
- 24. Лабораторный опыт № 7 Исследование химических свойств раствора серной кислоты ВНИМАНИЕ ! При работе с кислотой
- 25. В пробирках в виде растворов представлены вещества: NaCl, NaBr, NaI, NaF, H2SO4, Na2CO3, Na2SO4, NaOH Предложите
- 26. Если эти утверждения верны на Ваш взгляд, то напротив них поставьте знак «+», а если нет,
- 28. Скачать презентацию























 Преференции членов СНО
Преференции членов СНО Презентация на тему Профессии бывают разные
Презентация на тему Профессии бывают разные Ответственность, предусмотренная за нарушение требований трудового права, охраны труда и промышленной безопасности
Ответственность, предусмотренная за нарушение требований трудового права, охраны труда и промышленной безопасности Проблема проекта: Ненадлежащий вид электричек в Москве
Проблема проекта: Ненадлежащий вид электричек в Москве Я и мои права
Я и мои права Лекція 6
Лекція 6 Математика вокруг нас
Математика вокруг нас Афоризмы. Дружба
Афоризмы. Дружба Договор мены
Договор мены Форма государственного правления Российской Федерации
Форма государственного правления Российской Федерации Битумы (от лат. bitumen горная смола), твердые или смолоподобные продукты. Свойства битумов зависят от способов производства, качества
Битумы (от лат. bitumen горная смола), твердые или смолоподобные продукты. Свойства битумов зависят от способов производства, качества  Ata
Ata Юрий Визбор
Юрий Визбор Презентация на тему Становление личностных характеристик ученика начальной школы
Презентация на тему Становление личностных характеристик ученика начальной школы  Дизайн проект помещений пилотного центра занятости ГКУ ЦЗН г. Волгограда
Дизайн проект помещений пилотного центра занятости ГКУ ЦЗН г. Волгограда Still loving you
Still loving you Особенности электроснабжения обогатительных фабрик. Категории качества электроэнергии. Лекция №1
Особенности электроснабжения обогатительных фабрик. Категории качества электроэнергии. Лекция №1 Александр Анатольевич Емельянов Кафедра Математических и инструментальных методов экономики (МиИМЭ) Современные аспекты и раз
Александр Анатольевич Емельянов Кафедра Математических и инструментальных методов экономики (МиИМЭ) Современные аспекты и раз Реконструкция
Реконструкция Римское право
Римское право Город, улица, микрорайон
Город, улица, микрорайон Презентация на тему Перспективы использования интерактивных технологий в учебном процессе
Презентация на тему Перспективы использования интерактивных технологий в учебном процессе О пчелах, колоколах и вечном двигателе
О пчелах, колоколах и вечном двигателе Материнство глазами художников
Материнство глазами художников Как пополнить электронный кошелек «RBK money» через Интернет-банк Банка Русский Стандарт
Как пополнить электронный кошелек «RBK money» через Интернет-банк Банка Русский Стандарт Особенности построения сибирской избы
Особенности построения сибирской избы Презентация на тему Демографические перспективы
Презентация на тему Демографические перспективы 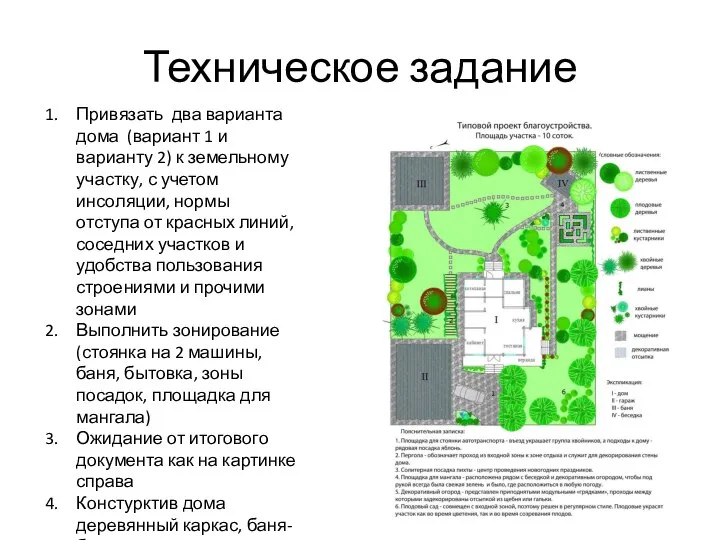 Техническое задание: привязать два варианта дома (вариант 1 и вариант 2) к земельному участку
Техническое задание: привязать два варианта дома (вариант 1 и вариант 2) к земельному участку