Регуляторные аспекты теста «Растворение» в Европейском союзе Конференция по тесту «Растворение», исследованиям биоэквивалентно
Содержание
- 2. План лекции Общие положения Руководство Примеры Заключение
- 3. Общие положения Что такое «Растворение»? Физический смысл: “процесс перехода твердого вещества в раствор” Биофармацевтический смысл: “Количество
- 4. Почему важно проводить тест «Растворение»? Note For Guidance On Development Pharmaceutics (CPMP/QWP/155/96) Кол-во ЛВ, высвободившееся в
- 5. Почему важно проводить тест «Растворение»? Обеспечивает надлежащий контроль за процессом – повышает качество ЛС, что обеспечивает
- 6. Общие положения Почему важно проводить тест «Растворение»? Помогает понять механизм высвобождения для ЛС с модифицированным высвобождением
- 7. Тест «Растворение» во время разработки Для понимания механизма высвобождения ЛФ с модифицированным высвобождением Для валидации производственного
- 8. Общие положения Тест «Растворение» и IVIVC Дискриминирующий метод Установление корреляции In Vitro –In Vivo Тест «Растворение»
- 9. Общие положения Тест «Растворение» и биоэквивалентность Чтобы в некоторых случаях показать сходство между разными ЛФ одного
- 10. Тест «Растворение» и контроль качества Чтобы получить информацию о сериях исследуемого и референтного препарата для исследований
- 11. Тест «Растворение» и качество через разработку (QbD) Отражает клиническое действие ЛС. Позволяет понять, какие критические параметры
- 12. План лекции Общие положения Нормативная документация Примеры Заключение
- 13. Рекомендации Европейской Фармакопеи(5.17.1) аппарат для теста «Растворение» среда растворения (состав, объем и температура) скорость вращения мешалки
- 14. Аппарат для теста «Растворение»(Ph.Eur.) Вращающаяся корзинка Лопастная мешалка Качающийся барабан Проточная ячейка Лопасть над диском Cell
- 15. Рекомендации Европейской Фармакопеи(5.17.1) Среда растворения условия предельного разбавления: объем среды растворения должен превышать объем, необходимый для
- 16. Рекомендации Европейской Фармакопеи(5.17.1) Скорость вращения мешалки или скорость потока обычно от 50 до 100 об/мин не
- 17. Рекомендации Европейской Фармакопеи(5.17.1) Нормы Нормы спецификации приводятся как количество (Q) ЛВ, высвободив-шегося в течение установленного времени,
- 18. Q=75-80% (обычно не более 80%, т.к. надо сделать допущения для норм количественного определения и однородности дозирования).
- 19. 2.9.4. Испытание «Растворение» для трансдермальных ЛФ Лопасть над диском Метод ячейки Вращающийся цилиндр 2.9.42. Испытание «Растворение»
- 20. Достаточная дискриминирующая способность между сериями ЛС с точки зрения критических параметров производства, влияющих на БД Подтверждение
- 21. “…в зависимости от ЛФ такие параметры как растворение…должны рассматриваться на стадии разработки ЛС.” “Разработка исследований должна
- 22. выбор методики теста «Растворение»… должен учитывать результаты исследований in vivo … и по возможности должен состоять
- 23. Данные изменения [от первоначального состава до последующих изменений] могут влиять на свойства ЛС. Поэтому рекомендуется, чтобы
- 24. Дискриминирующая способность теста «Растворение» для рутинного контроля качества может быть установлена путем сравнения данных in vitro
- 25. В большинстве случаев для установления сходства профили растворения необходимо сравнивать. Это можно сделать методами моделей или
- 26. “Спецификация критических показателей качества ЛС, таких как растворение, должна устанавливаться на серии ЛС, для которой подтверждена
- 27. “… установление IVIVC может …помочь в разработке спецификации и применяться для упрощения принятия некоторых регуляторных решений…”
- 28. “В случае установления четкой корреляции между характером высвобождения in vitro и параметрами биодоступности in vivo, in
- 29. ЛФ немедленного высвобождения Обычно как минимум 80% ЛВ высвобождается за установленное время, чаще всего это 45
- 30. Пролонгированные ЛФ Обычно пробы отбирают в 3 и более временных точках (Ph.Eur. 2.9.3 & 5.17.1): 1
- 31. Пролонгированные ЛФ Приемлемые границы (верхняя и нижняя граница процента высвобождения) определяются для каждой точки и могут
- 32. ЛФ с отложенным высвобождением (Ph.Eur. 2.9.3 & 5.17.1): Различный в зависимости от ЛФ (частичное или полное
- 33. ЛФ с отложенным высвобождением Одна единица ЛС для нераспадающихся ЛФ и несколько – для распадающихся Нормы
- 34. План лекции Общие положения Руководство Примеры Заключение
- 35. быстро распадающиеся сублингвальные таблетки быстрое растворение ЛВ в физиологическом диапазоне рН, Установление дискриминирующего теста, применяемого для
- 36. Note For Guidance On Development Pharmaceutics (CPMP/QWP/155/96) “Тест «Растворение» необходимо проводить на стадии разработки ЛС и
- 37. Все серии ЛС для КИ соответствуют нормам спецификации по тесту «распадаемость» ( Пример (1) Сублингвальные таблетки
- 38. Применение: один раз в день Среда растворения: Вода pH 4,5, 0,005% ГПМЦ, натрия лаурилсульфат 0,1% Временные
- 39. Обычно 3 или более временных точек. (Ph.Eur 5.17.1) Чтобы убедиться, что нет преждевременного высвобождения дозы. Чтобы
- 40. Вторая временная точка 1,5 ч не отражает среднего времени высвобождения в течение 24 ч, которое обеспечивает
- 41. ЛФ: таблетки немедленного высвобождения 200 мг и суспензия для внутреннего применения 50 мг/5 мл. Дополнительные дозировки:
- 42. Не обеспечиваются условия предельного разведения ? выбранная методика теста «Растворение» (pH 6,8 и 2 % натрия
- 43. Первоначальное содержание натрия лаурилсульфата 6%. Условия предельного разведения (ЕФ 5.17.1.) ~ четырехкратный объем среды, необходимый для
- 44. Одна среда растворения. Важно подтвердить, что растворение в кислой среде НЕ приводит к преждевременному высвобождению дозы.
- 45. Состав среды растворения должен быть обоснован для дозировок 50 и 100 мг, т.к. натрия лаурилсульфат может
- 46. необходимо показать, что методика теста «Растворение» способная выявить различия между низшими дозировками ЛС. Потому что Существенное
- 47. необходимо показать, что методика теста «Растворение» способная выявить различия между низшими дозировками ЛС. И потому что
- 48. Ужесточение норм теста «Растворение» на средних временных точках должно применяться для дозировок 50 & 100 мг
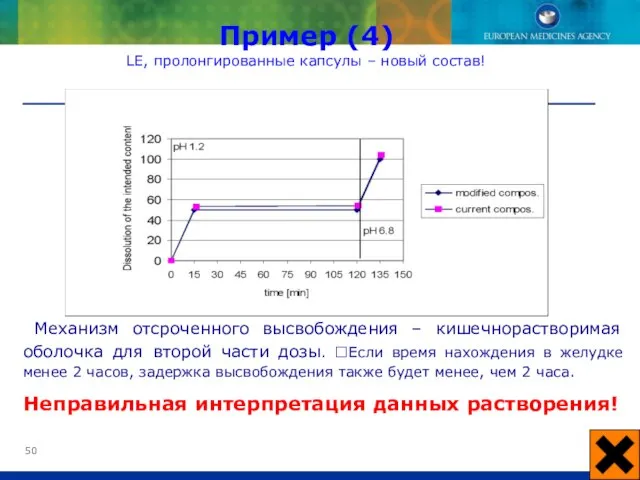
- 49. Капсулы наполняют двумя типами пеллет: 50 % дозы – немедленного высвобождения 50 % - отсроченного высвобождения
- 50. Механизм отсроченного высвобождения – кишечнорастворимая оболочка для второй части дозы. ?Если время нахождения в желудке менее
- 51. Серия ЛВ для исследования биоэквивалентности и 2 более низкие дозировки показали сходные профили растворения при рН
- 52. Сходны ли профили растворения в одинаковых условиях (pH 1,2, pH 2,0, pH 4,5, and pH 6,8)
- 53. Растворение и тестового, и референтного препаратов при рН 4,5 и 6,8 ? следовательно, профили растворения не
- 54. Для контроля качества выбирают наиболее подходящую среду растворения, сходную с условиями растворения in vivo (Выбор среды
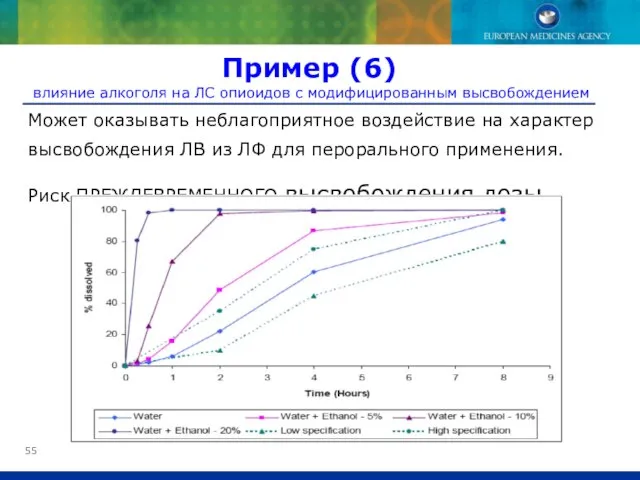
- 55. Может оказывать неблагоприятное воздействие на характер высвобождения ЛВ из ЛФ для перорального применения. Риск ПРЕЖДЕВРЕМЕННОГО высвобождения
- 56. Все ЛС с модифицированным высвобождением должны проверяться на предмет несовместимости с алкогольными напитками Особенно важно для
- 57. План лекции Общие положения Руководство Примеры Заключение
- 58. дискриминирующая методика Позволяет прогнозировать поведение ЛС in vivo (указывать на бионеэквивалентность) Выявляет изменения в составе ЛФ
- 59. На практике Любая методика должна выявлять различия в составе ЛФ (слишком дискримирирующая) Предпочтительная среда растворения -
- 60. “Совет от регуляторных органов” Знай свой продукт! Тщательные выбор метода и его разработка Достаточно детальная информация/четкость
- 62. Скачать презентацию





















![Данные изменения [от первоначального состава до последующих изменений] могут влиять на свойства](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/422662/slide-22.jpg)



































 Shape
Shape Мой кумир - Джессика Альба
Мой кумир - Джессика Альба ЦО № 429 – ресурсный центр инновационной сети «Обучение по индивидуальным учебным планам в старшей школе»
ЦО № 429 – ресурсный центр инновационной сети «Обучение по индивидуальным учебным планам в старшей школе» О РАЗРАБОТКЕ МУНИЦИПАЛЬНЫХ ПРОГРАММ В ОБЛАСТИ ЭНЕРГОСБЕРЕЖЕНИЯ
О РАЗРАБОТКЕ МУНИЦИПАЛЬНЫХ ПРОГРАММ В ОБЛАСТИ ЭНЕРГОСБЕРЕЖЕНИЯ Изображение и реальность
Изображение и реальность Управление качеством в процессе закупок
Управление качеством в процессе закупок С 01 октября 2020 года денежные средства будут перечисляться банками только на карту Мир гражданам, получающим пособия
С 01 октября 2020 года денежные средства будут перечисляться банками только на карту Мир гражданам, получающим пособия Щи - национальное русское блюдо
Щи - национальное русское блюдо Век Просвещения
Век Просвещения Musical Britain
Musical Britain Проект по дизайну в сфере применения
Проект по дизайну в сфере применения «Последнее слово» Ильи Петрова. - презентация
«Последнее слово» Ильи Петрова. - презентация Формирование и развитие материально-технической базы АПК Украины
Формирование и развитие материально-технической базы АПК Украины Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников
Роль фольклора в процессе формирования духовно-нравственных качеств дошкольников Конкурентные стратегииприложение к журналу «ЭТАП: Экономическая Теория, Анализ, Практика»
Конкурентные стратегииприложение к журналу «ЭТАП: Экономическая Теория, Анализ, Практика» ИНСТРУКЦИИ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ НА УРОКАХ ТЕХНОЛОГИИ 5 и 6 классов
ИНСТРУКЦИИ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ НА УРОКАХ ТЕХНОЛОГИИ 5 и 6 классов Презентация на тему Игры на развитие интеллектуальных способностей детей дошкольного возраста посредством ИКТ
Презентация на тему Игры на развитие интеллектуальных способностей детей дошкольного возраста посредством ИКТ The United Nations General Assembly
The United Nations General Assembly  ГРАФИЧЕСКИЕ ИНФОРМАЦИОННЫЕ МОДЕЛИ МОДЕЛИРОВАНИЕ И ФОРМАЛИЗАЦИЯ
ГРАФИЧЕСКИЕ ИНФОРМАЦИОННЫЕ МОДЕЛИ МОДЕЛИРОВАНИЕ И ФОРМАЛИЗАЦИЯ «Секреты выбора кредитных продуктов украинских банков»
«Секреты выбора кредитных продуктов украинских банков» Методика проведения международных маркетинговых исследований Дисциплина: Международный маркетинг Преподаватель: профессор ка
Методика проведения международных маркетинговых исследований Дисциплина: Международный маркетинг Преподаватель: профессор ка Повторение
Повторение Ранний период Христианской философии
Ранний период Христианской философии Бельмондо (фотографии)
Бельмондо (фотографии) Маркетинговое исследование пакетированных соков в городе Новороссийск
Маркетинговое исследование пакетированных соков в городе Новороссийск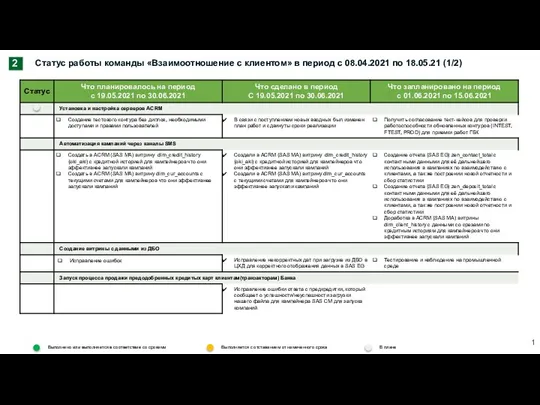 Статус работы команды Взаимоотношение с клиентом в период с 08.04.2021 по 18.05.21
Статус работы команды Взаимоотношение с клиентом в период с 08.04.2021 по 18.05.21 Электронная и цифровая техника в СЦБ
Электронная и цифровая техника в СЦБ Дистрибьюция фармпрепаратов в Украине. Тенденции развития
Дистрибьюция фармпрепаратов в Украине. Тенденции развития