Содержание
- 2. Основные вопросы 1.Истрия открытия и изучения серы. 2. Распространение серы в природе. 3. Аллотропия и физические
- 3. История открытия Дата открытия – известна древним цивилизациям; Греческое название серы тейони (божественный, небесный) указывает на
- 4. Сера в природе Самородная сера Сульфидная сера Сульфатная сера
- 5. Самородная сера
- 6. Сульфидная сера Пирит-FeS2 Fe 46,6%; S 53,4% Киноварь-HgS Hg 86,2%; S 13,8%
- 7. Сульфатная сера Гипс – CaSO4*2H2O Барит – BaSO4
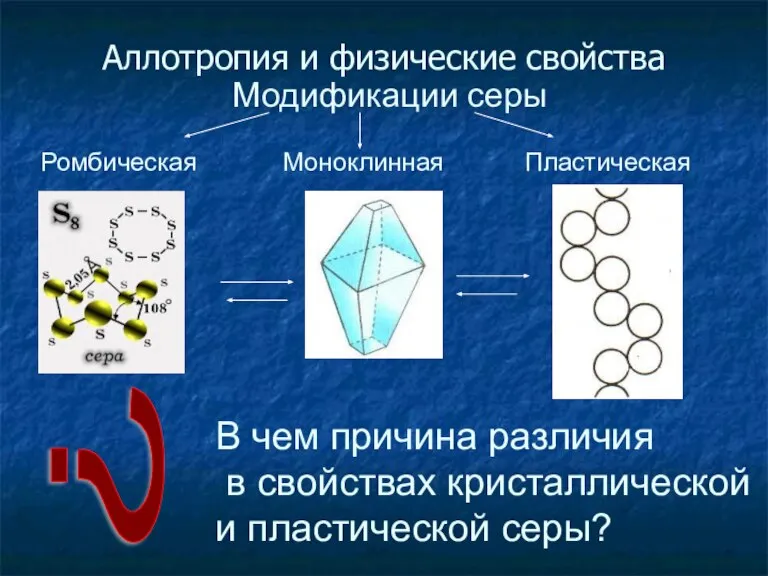
- 8. Аллотропия и физические свойства ? В чем причина различия в свойствах кристаллической и пластической серы? Модификации
- 9. ? Какими свойствами – окислительными или восстановительными обладает сера?
- 10. Применение знаний: 1.Распределение электронов по энергетическим уровням в атоме серы: А. 2, 6. В. 2, 8,
- 11. Применение знаний: 3.Свойство, характерное для серы: А.Хорошо растворима в воде. Б.Имеет металлический блеск. В.Твердое вещество желтого
- 13. Скачать презентацию









 Математика в природе
Математика в природе Официально – деловой стиль речи.
Официально – деловой стиль речи. Храмовый синтез искусств
Храмовый синтез искусств Концепция курса «Основы религиозной культуры и светской этики» и его методическое сопровождение
Концепция курса «Основы религиозной культуры и светской этики» и его методическое сопровождение Баскетбол. Основные элементы техники баскетбола
Баскетбол. Основные элементы техники баскетбола Та ырыпқ Жасанды оректік ортада сетін
Та ырыпқ Жасанды оректік ортада сетін Эпоха Возрождения. Ренессанс
Эпоха Возрождения. Ренессанс Лишь вера одна никогда не бывает одна
Лишь вера одна никогда не бывает одна Сущность и современное понимание геополитики, ее структура, функции и категории
Сущность и современное понимание геополитики, ее структура, функции и категории Ветхозаветная апокалиптика
Ветхозаветная апокалиптика "Ради ясной цели можно отказаться от прав"
"Ради ясной цели можно отказаться от прав" Система 5С
Система 5С Биологическая игра «Первый миллион»Учитель: Шакирова Ф.Ф.
Биологическая игра «Первый миллион»Учитель: Шакирова Ф.Ф. Самопрезентация
Самопрезентация Презентация на тему Три кита в музыке
Презентация на тему Три кита в музыке  Наша помощница - швейная иголочка
Наша помощница - швейная иголочка Комплекс для размещения организованных спортивных групп БАНАНА КЛАБ в Кабардинке (Геленджик)
Комплекс для размещения организованных спортивных групп БАНАНА КЛАБ в Кабардинке (Геленджик) Медь и её сплавы
Медь и её сплавы Основы маркетинга
Основы маркетинга Докладчик: Начальник сектора маркетинга, ценообразования и конкурсных процедур Санкт-Петербургской ДМТО Виноградова Виктория Иг
Докладчик: Начальник сектора маркетинга, ценообразования и конкурсных процедур Санкт-Петербургской ДМТО Виноградова Виктория Иг Есть контакт
Есть контакт История города в людях. Лев Петрович Крымов
История города в людях. Лев Петрович Крымов Структура МСУ и особенности цифрового управления
Структура МСУ и особенности цифрового управления Экономический рост.
Экономический рост. Современные педагогические технологии в рамках подготовки ФГОС второго поколения
Современные педагогические технологии в рамках подготовки ФГОС второго поколения Бизнес-план инвестиционного проекта
Бизнес-план инвестиционного проекта Войсковые звания
Войсковые звания Разнообразие рельефа Земли
Разнообразие рельефа Земли