Слайд 2ЦЕЛЬ УРОКА
познакомить учащихся с новым классом неорганических соединений - кислоты

Слайд 3ПРОВЕРКА ЗНАНИЙ
1. Из предложенного перечня веществ выпишите формулы оснований:
CuO , Mn2O7,

N2O3, HNO3, H2SO3, H2S, Fe(OH)2, NaOH, A1(OH)3, Ca3(PO4)2, ZnI2, Mg(NO2)2.
2. Дайте им название.
3. Составьте формулы оксидов, соответствующие этим основаниям.
Слайд 4На какие группы можно разделить основания?
Как это можно определить, не проводя опыт?

Слайд 6КЛАССИФИКАЦИЯ ОСНОВАНИЙ ПО РАСТВОРИМОСТИ
Слайд 7Каждое вещество имеет свое название! Как правильно дать название основанию?
LiOH –
Fe(OH)3
-
гидроксид лития
гидроксид железа (III)
Слайд 8Каждому основанию соответствует оксид. Что является обязательным условием данного соответствия?
Слайд 9ПРОБЛЕМА
Оксидам металлов соответствуют основания, а оксидам неметаллов?

Слайд 10Лимонная
Яблочная
Муравьиная
Кислоты
кислый вкус
КИСЛОТЫ ВОКРУГ НАС
Слайд 11ИНДИКАТОРЫ
Индикаторы – это вещества, которые изменяют свою окраску в растворах щелочей и

кислот
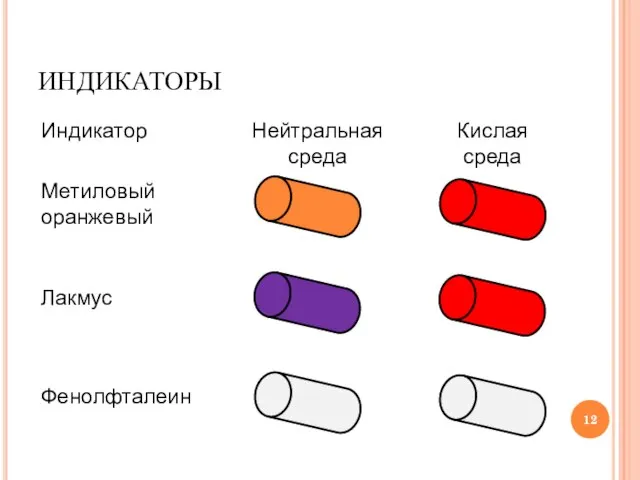
Слайд 12ИНДИКАТОРЫ
Индикатор
Метиловый оранжевый
Нейтральная среда
Кислая среда
Лакмус
Фенолфталеин
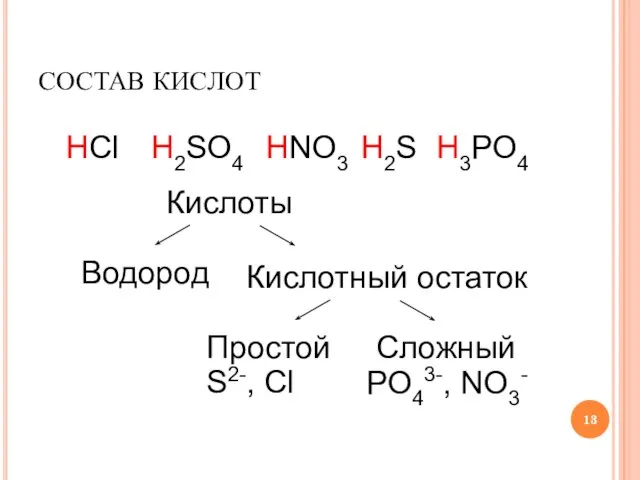
Слайд 13СОСТАВ КИСЛОТ
HCl
H2SO4
HNO3
H2S
H3PO4
Кислоты
Водород
Кислотный остаток
Простой
Сложный
S2-, Cl
PO43-, NO3-
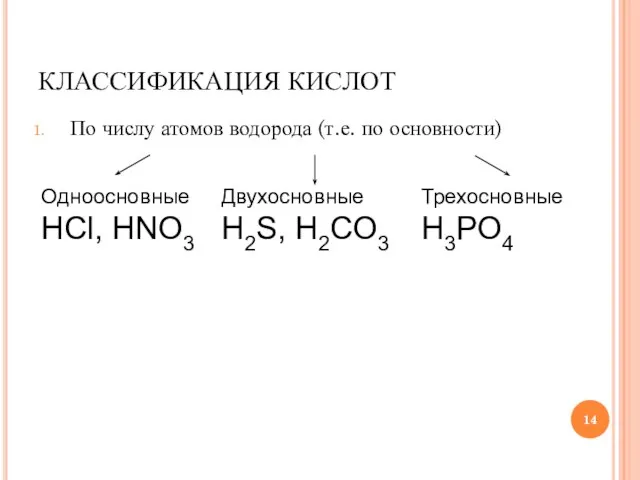
Слайд 14КЛАССИФИКАЦИЯ КИСЛОТ
По числу атомов водорода (т.е. по основности)
Одноосновные
HCl, HNO3
Двухосновные
H2S, H2CO3
Трехосновные
H3PO4
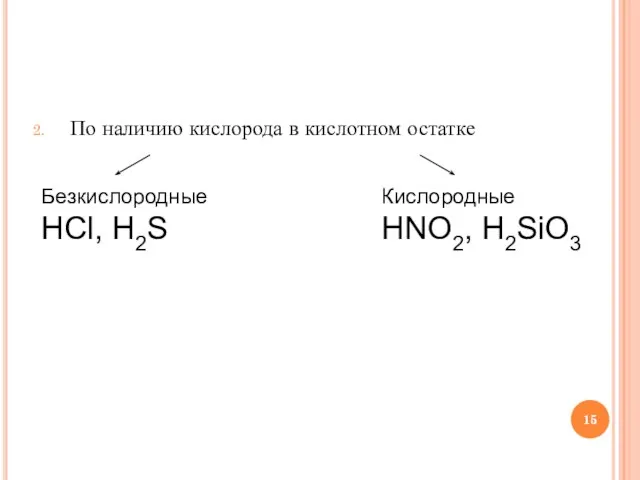
Слайд 15По наличию кислорода в кислотном остатке
Безкислородные
HCl, H2S
Кислородные
HNO2, H2SiO3
Слайд 16По растворимости
Растворимые
H3PO4,H2SO4
Нерастворимые
H2SiO3
Слайд 17ФИЗИЧЕСКИЕ СВОЙСТВА КИСЛОТ
Жидкие: HCl – соляная, H2SO4 – серная.
Твердые: стеариновая, борная
H2CO3 –

угольная кислота
H2SO3 – сернистая кислота
H2CO3 H2O + CO2
H2SO3 H2O + SO2
Слайд 18ОПРЕДЕЛЕНИЕ СТЕПЕНЕЙ ОКИСЛЕНИЯ ЭЛЕМЕНТОВ И ЗАРЯДОВ ИОНОВ КИСЛОТ
Водород в кислотах всегда заряжен

+1.
Численное значение заряда кислотного остатка всегда равно числу атомов водорода в молекуле, т. е. основности данной кислоты.
Примеры:
HNO3 HCl
H2S, Н2СО3
Слайд 19ВАЖНЕЙШИЕ КИСЛОТЫ
Молочная кислота – скисание молока
Щавелевая – в листьях щавеля
Серная H2SO4 Получают
Соляная

HCl искусственным
Азотная HNO3 путем
Наиболее часто используют серную кислоту H2SO4
Слайд 20ПРАВИЛА РАЗБАВЛЕНИЯ КИСЛОТ
Кислоту в воду!!!

Слайд 21ЗАКРЕПЛЕНИЕ
Лабораторный опыт «Определение раствора кислоты с помощью индикатора»




















 «MITSUBISHII HEAVY INDUSTRIES» Теперь в Казахстане.
«MITSUBISHII HEAVY INDUSTRIES» Теперь в Казахстане. Право на труд. Трудовые правоотношения
Право на труд. Трудовые правоотношения Управление технического учета и документирования
Управление технического учета и документирования Презентация
Презентация Власть и влияние
Власть и влияние Гражданские дела (первая инстанция) Урок 1.11. Регистрация решения по кассационной жалобе
Гражданские дела (первая инстанция) Урок 1.11. Регистрация решения по кассационной жалобе «Все, что служит системе образования, служит и будущему нашей страны» Н.А.Назарбаев
«Все, что служит системе образования, служит и будущему нашей страны» Н.А.Назарбаев Камиль Сен-Санс Карнавал животных
Камиль Сен-Санс Карнавал животных Отчет по площадке Июль 2012
Отчет по площадке Июль 2012 Транспорт
Транспорт Madame L’Automne
Madame L’Automne Занятие 1 презентация
Занятие 1 презентация Сельское хозяйство мира
Сельское хозяйство мира Храмы Древней Греции
Храмы Древней Греции Российские изобретения
Российские изобретения Я - сообщение
Я - сообщение Бурение скважин при доразведке золото-рудного месторождения Суздаль
Бурение скважин при доразведке золото-рудного месторождения Суздаль Презентация на тему Физиологические адаптации (9 класс)
Презентация на тему Физиологические адаптации (9 класс) Страна Вопросительных местоимений
Страна Вопросительных местоимений Система Пойнтер. Управление компьютером с помощью взгляда
Система Пойнтер. Управление компьютером с помощью взгляда МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО РАЗРАБОТКЕ ОБРАЗОВАТЕЛЬНЫХ ПРОГРАММ ПОСЛЕВУЗОВСКОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ (интернатура и
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО РАЗРАБОТКЕ ОБРАЗОВАТЕЛЬНЫХ ПРОГРАММ ПОСЛЕВУЗОВСКОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ (интернатура и Презентация на тему Первый космонавт земли Юрий Алексеевич Гагарин
Презентация на тему Первый космонавт земли Юрий Алексеевич Гагарин  Кельнский собор
Кельнский собор «Герой нашего времени»
«Герой нашего времени» СМШ
СМШ Расти глобально, делать локально: международные компании в Казахстане
Расти глобально, делать локально: международные компании в Казахстане кп к уроку 3
кп к уроку 3 Презентация на тему Ф.Бэкон. Обоснование эмпиризма
Презентация на тему Ф.Бэкон. Обоснование эмпиризма