Содержание
- 2. Тромботическая микроангиопатия : ТМА - гетерогенная группа заболеваний, объединенных общностью гистологической картины и клинических проявлений при
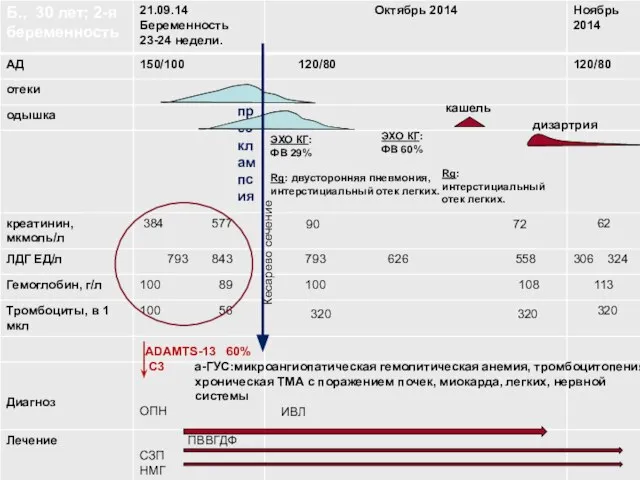
- 3. ADAMTS-13 60% С3 а-ГУС:микроангиопатическая гемолитическая анемия, тромбоцитопения, хроническая ТМА с поражением почек, миокарда, легких, нервной системы
- 4. Moschcowitz E. Hyaline thrombosis of the terminal arterioles and capillaries: a hitherto undescribed disease Proc N
- 5. SINGER K. et al. Thrombotic thrombocytopenic purpura; hemorrhagic diathesis with generalized platelet thromboses Blood. 1947; 2(6):
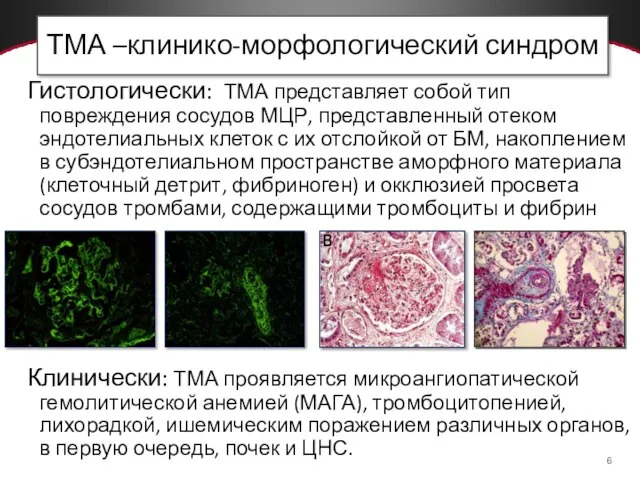
- 6. ТМА –клинико-морфологический синдром Гистологически: ТМА представляет собой тип повреждения сосудов МЦР, представленный отеком эндотелиальных клеток с
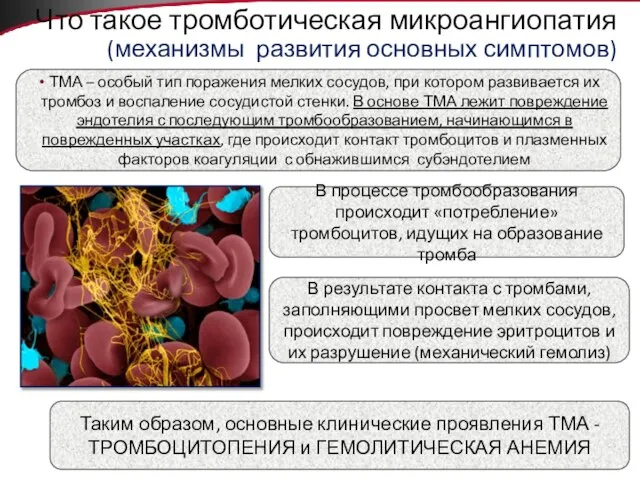
- 7. Что такое тромботическая микроангиопатия (механизмы развития основных симптомов) ТМА – особый тип поражения мелких сосудов, при
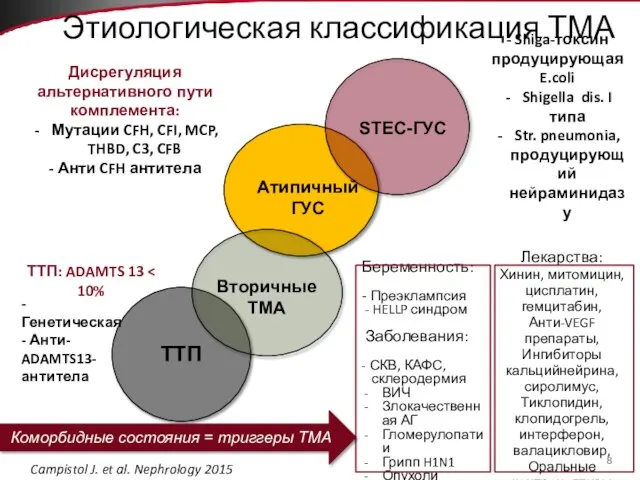
- 8. Этиологическая классификация ТМА STEC-ГУС Атипичный ГУС Вторичные ТМА ТТП ТТП: ADAMTS 13 -Генетическая - Анти- ADAMTS13-
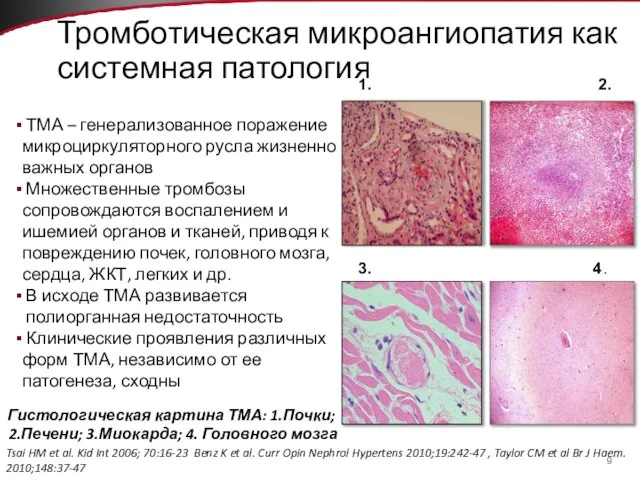
- 9. Тромботическая микроангиопатия как системная патология ТМА – генерализованное поражение микроциркуляторного русла жизненно важных органов Множественные тромбозы
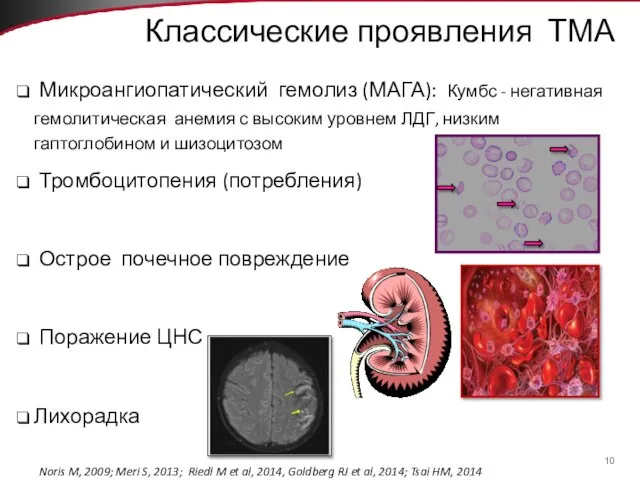
- 10. Классические проявления ТМА Микроангиопатический гемолиз (МАГА): Кумбс - негативная гемолитическая анемия с высоким уровнем ЛДГ, низким
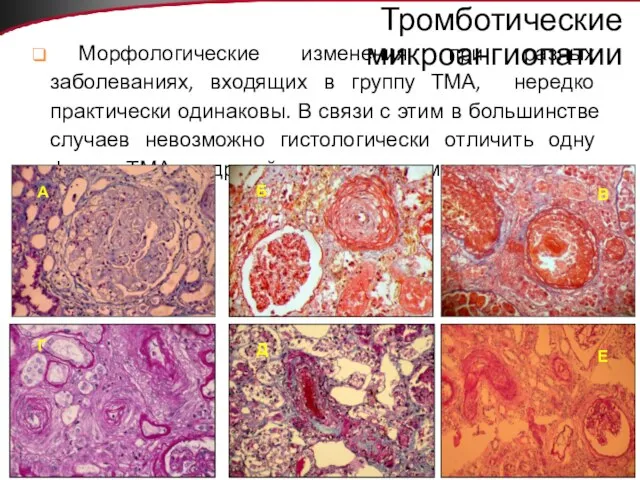
- 11. Тромботические микроангиопатии Морфологические изменения при разных заболеваниях, входящих в группу ТМА, нередко практически одинаковы. В связи
- 12. Тромботическая тромбоцитопеническая пурпура
- 13. Тромботическая тромбоцитопеническая пурпура (ТТП): Классификация ТТП ТТП- системная форма ТМА, в основе которой лежит тромбообразование в
- 14. Veyradier @ Coppo, 2011 кровоток тромбоцит ADAMTS13 ФВ ADAMTS13 расщепляет фактор Виллебранда в плазме крови и
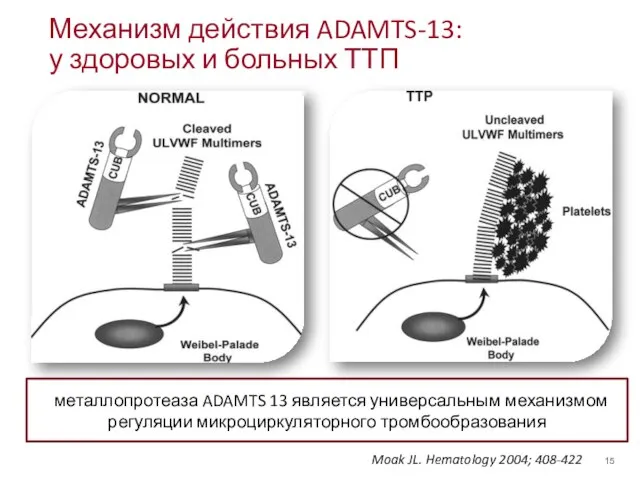
- 15. Механизм действия ADAMTS-13: у здоровых и больных ТТП Moak JL. Hematology 2004; 408-422 металлопротеаза ADAMTS 13
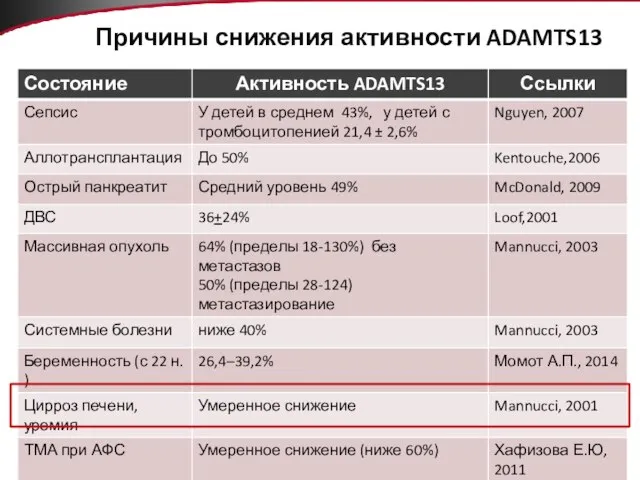
- 16. Причины снижения активности ADAMTS13
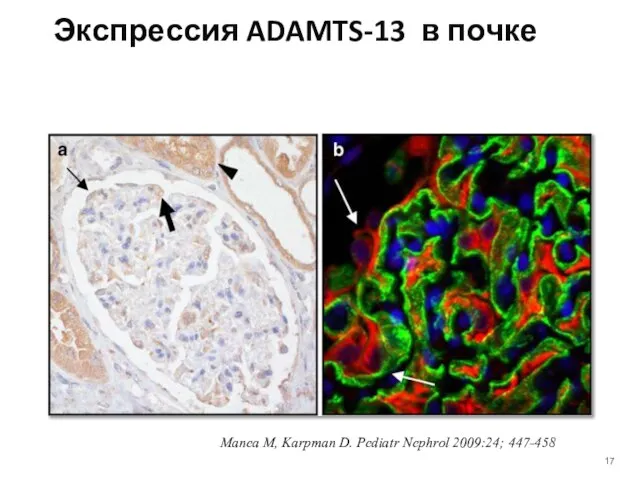
- 17. Экспрессия ADAMTS-13 в почке Manea M, Karpman D. Pediatr Nephrol 2009:24; 447-458
- 18. Гемолитико-уремический синдром
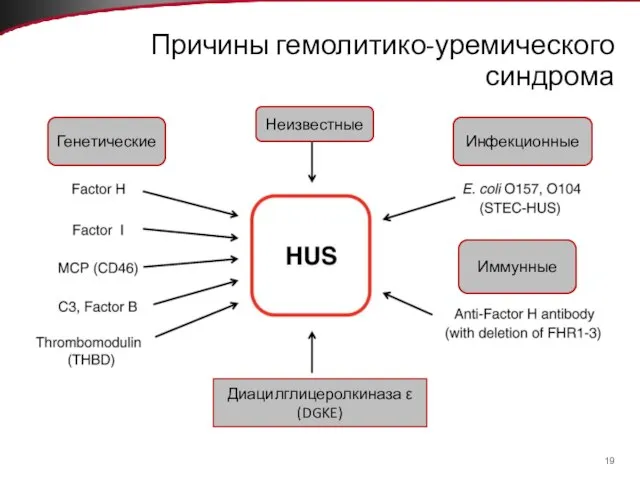
- 19. Причины гемолитико-уремического синдрома Генетические Неизвестные Инфекционные Иммунные Диацилглицеролкиназа ε (DGKE)
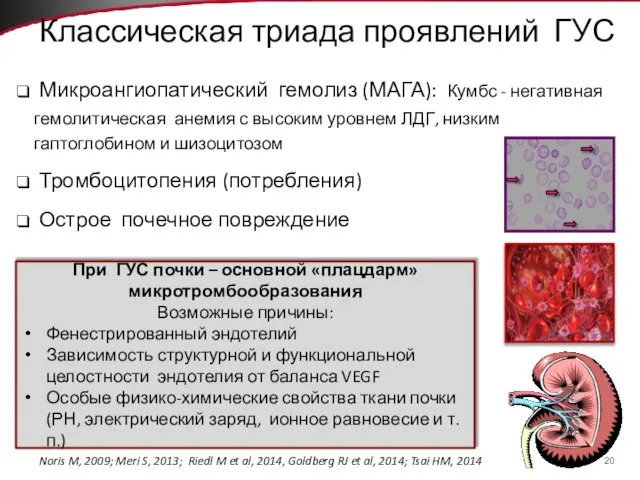
- 20. Классическая триада проявлений ГУС Микроангиопатический гемолиз (МАГА): Кумбс - негативная гемолитическая анемия с высоким уровнем ЛДГ,
- 21. Типичный ГУС Wolf 2004, NDT, 19:1687 STEC напрямую активирует комплемент Нарушает нормальную регуляцию комплемента Повреждает эндотелиальные
- 22. Атипичный гемолитико-уремический синдром: Распространенность аГУС составляет 2-7 случаев на 1 000 000 населения. Около 50 %
- 23. Заболевания почек, в развитии которых играет роль патология системы комплемента Мембранозная нефропатия Атипичный гемолитико-уремический синдром Анти-БМК-болезнь
- 24. Система комплемента: «всегда готова», быстро активируется, зависит от естественных регуляторов Важный компонент естественной защитной иммунной системы
- 25. Биологические функции системы комплемента Непосредственное уничтожение патологического агента (комплекс мембранной атаки – МАК) Индукция фагоцитоза (C5a)
- 26. Всегда активирован Комплемент – всегда активен, с возможностью дальнейшей активацией триггерами иммунной системы Figueroa JE, Densen
- 27. Факторы, контролирующие активность комплемента Регулируют активацию комплемента; Предотвращают чрезмерную активацию и повреждение собственных клеток и органов
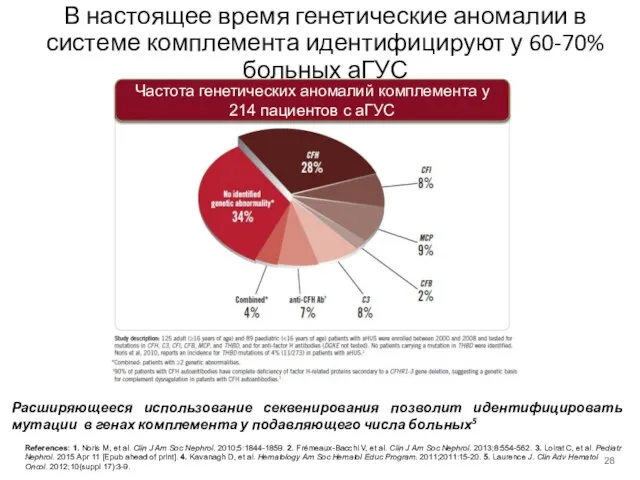
- 28. В настоящее время генетические аномалии в системе комплемента идентифицируют у 60-70% больных аГУС Расширяющееся использование секвенирования
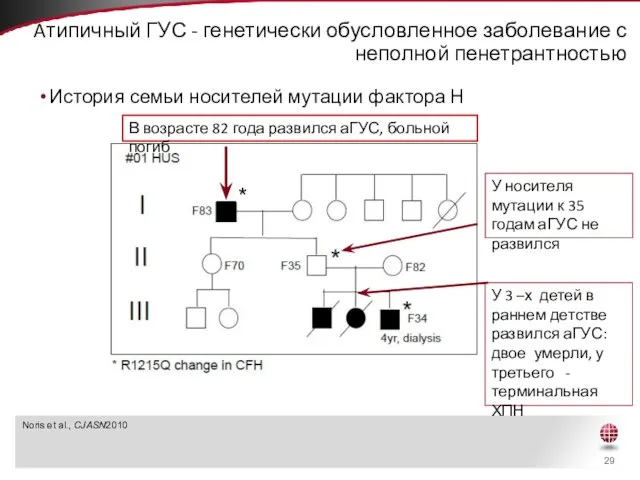
- 29. Aтипичный ГУС - генетически обусловленное заболевание с неполной пенетрантностью История семьи носителей мутации фактора Н Noris
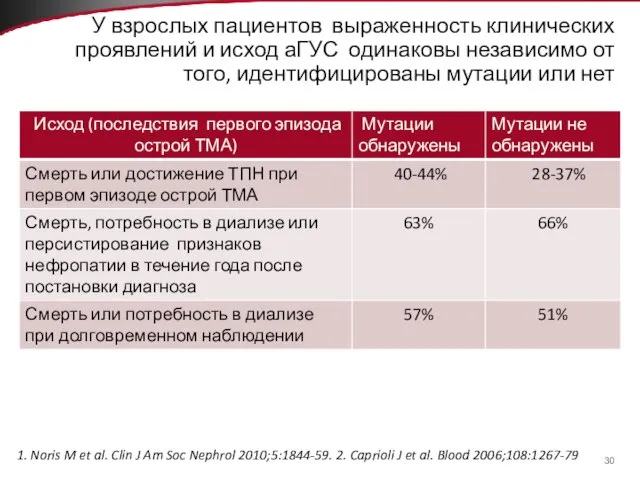
- 30. У взрослых пациентов выраженность клинических проявлений и исход аГУС одинаковы независимо от того, идентифицированы мутации или
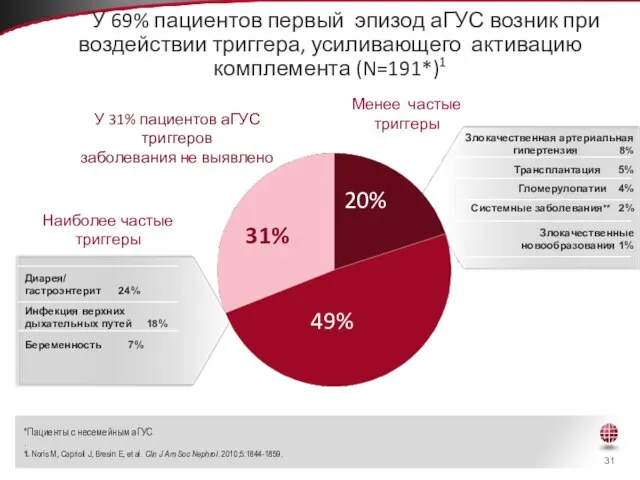
- 31. У 69% пациентов первый эпизод аГУС возник при воздействии триггера, усиливающего активацию комплемента (N=191*)1 Злокачественная артериальная
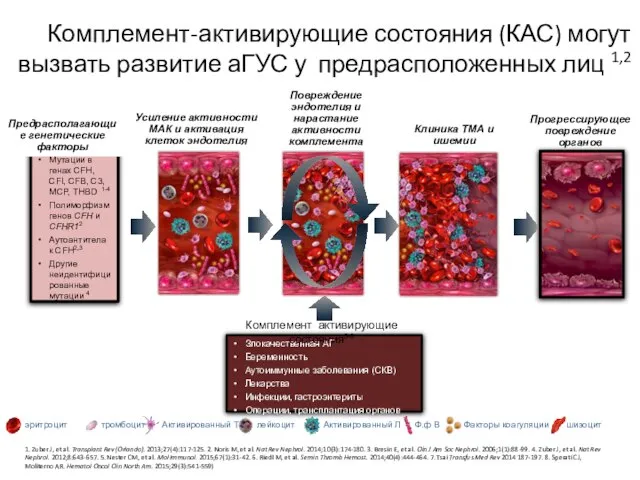
- 32. Комплемент-активирующие состояния (КАС) могут вызвать развитие аГУС у предрасположенных лиц 1,2 Мутации в генах CFH, CFI,
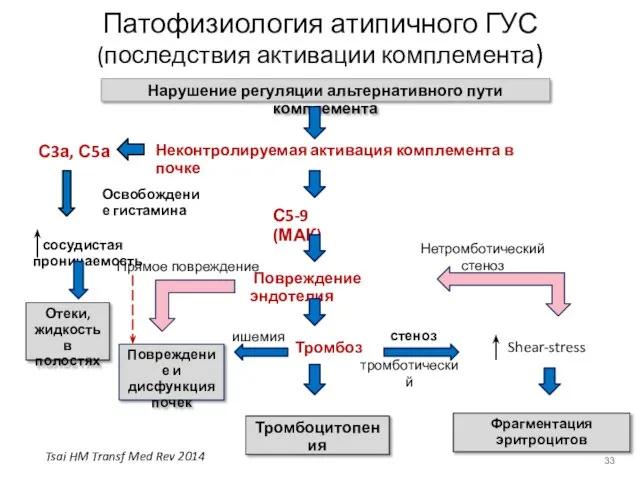
- 33. Патофизиология атипичного ГУС (последствия активации комплемента) Нарушение регуляции альтернативного пути комплемента Неконтролируемая активация комплемента в почке
- 34. Особенности поражения почек при хронической комплемент-опосредованной ТМА ОПН может не быть первым проявлением аГУС 1 17%
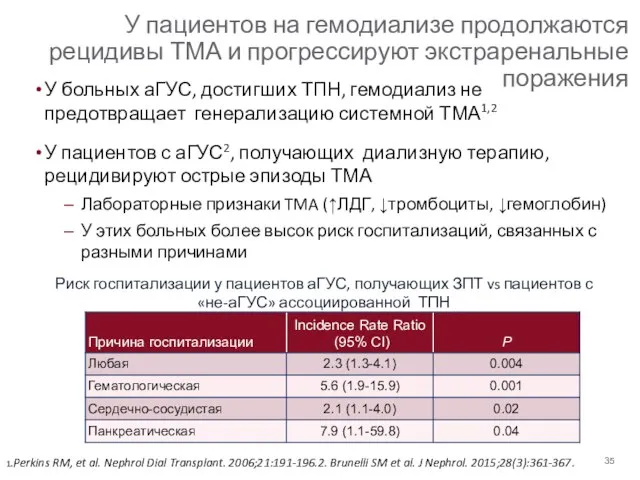
- 35. У пациентов на гемодиализе продолжаются рецидивы ТМА и прогрессируют экстраренальные поражения У больных аГУС, достигших ТПН,
- 36. aГУС : особенности заболевания Из-за генетического дефицита регуляторов комплемента aГУС следует рассматривать как длительно текущую хроническую
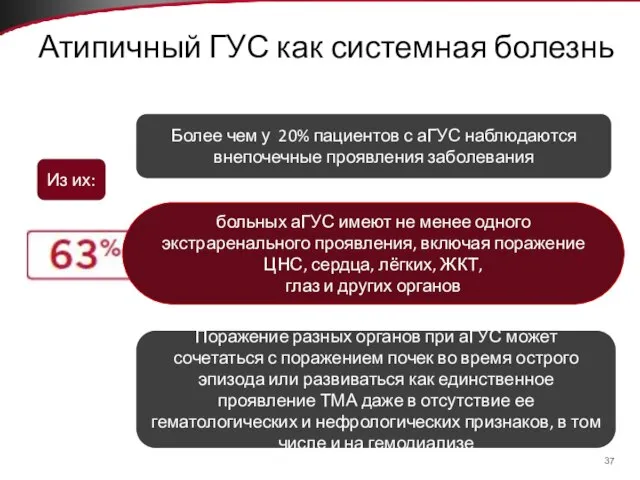
- 37. Атипичный ГУС как системная болезнь больных аГУС имеют не менее одного экстраренального проявления, включая поражение ЦНС,
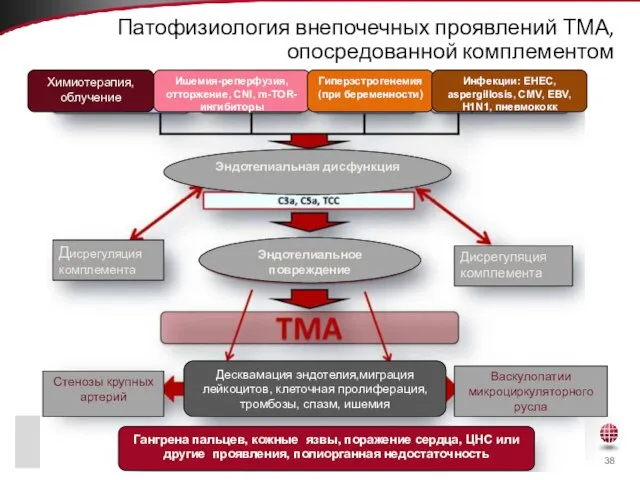
- 38. Патофизиология внепочечных проявлений ТМА, опосредованной комплементом Дисрегуляция комплемента Дисрегуляция комплемента Стенозы крупных артерий Васкулопатии микроциркуляторного русла
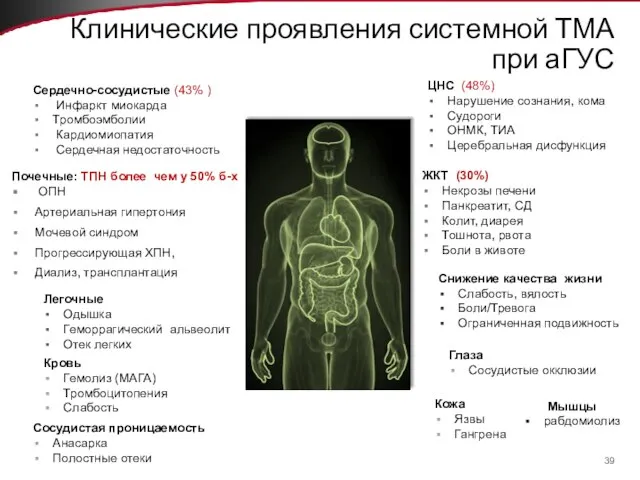
- 39. Клинические проявления системной ТМА при аГУС Сердечно-сосудистые (43% ) Инфаркт миокарда Тромбоэмболии Кардиомиопатия Сердечная недостаточность ЦНС
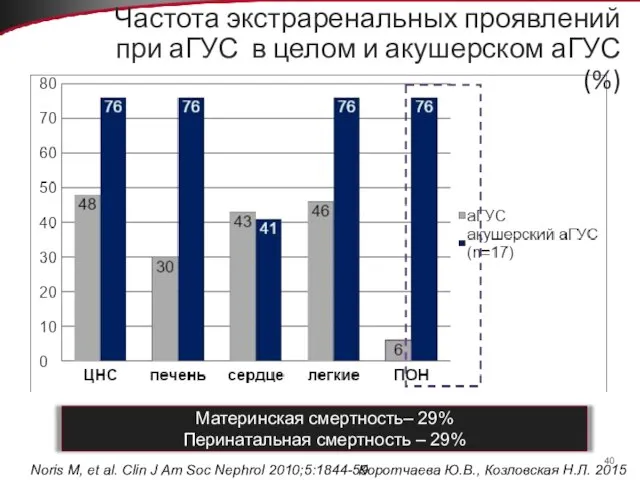
- 40. Частота экстраренальных проявлений при аГУС в целом и акушерском аГУС (%) Материнская смертность– 29% Перинатальная смертность
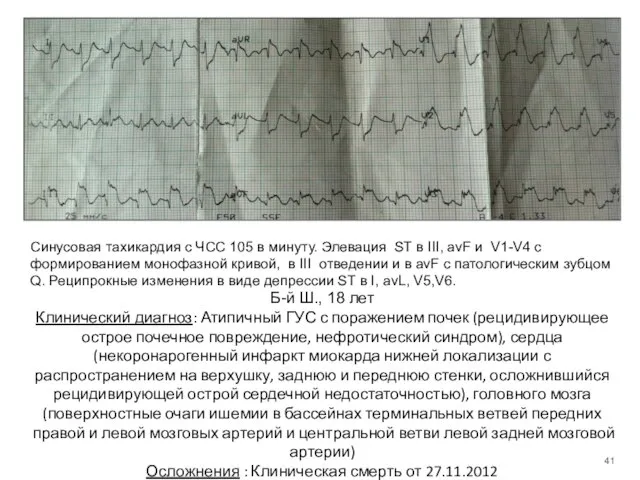
- 41. Синусовая тахикардия с ЧСС 105 в минуту. Элевация ST в III, avF и V1-V4 с формированием
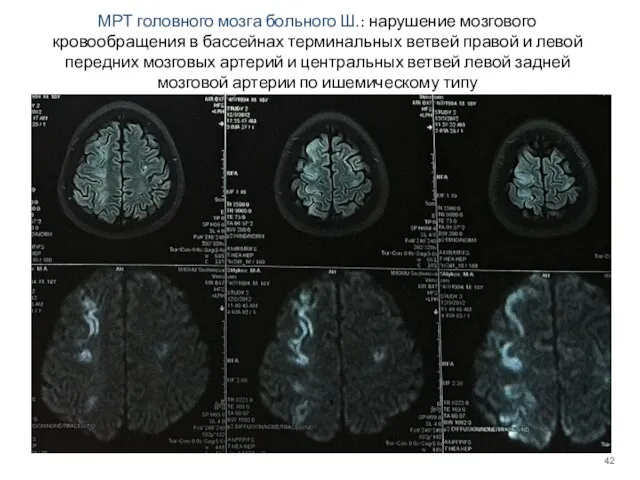
- 42. МРТ головного мозга больного Ш.: нарушение мозгового кровообращения в бассейнах терминальных ветвей правой и левой передних
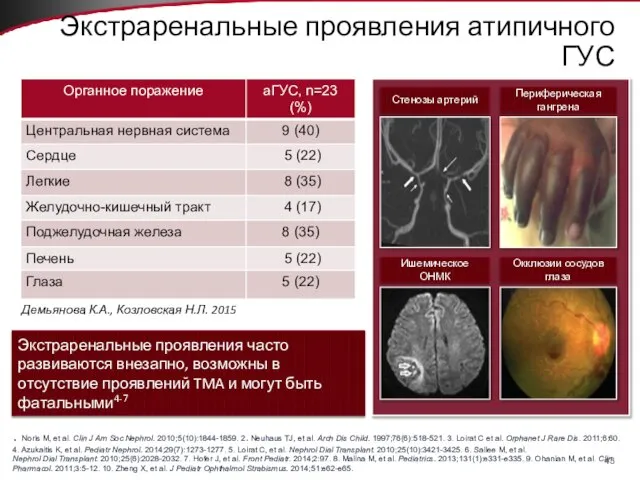
- 43. Экстраренальные проявления атипичного ГУС Демьянова К.А., Козловская Н.Л. 2015 Экстраренальные проявления часто развиваются внезапно, возможны в
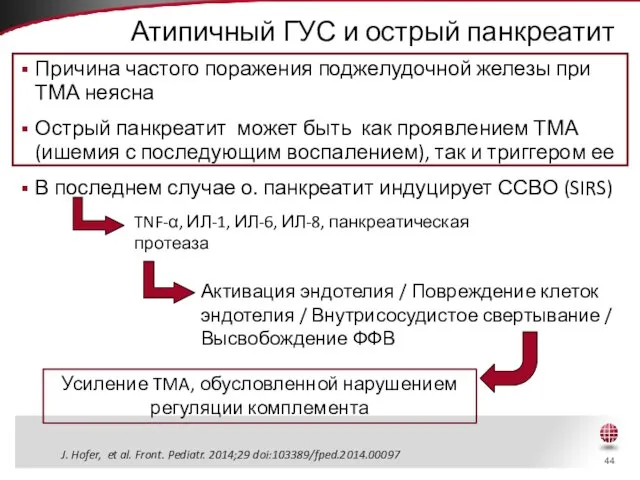
- 44. Атипичный ГУС и острый панкреатит Причина частого поражения поджелудочной железы при ТМА неясна Острый панкреатит может
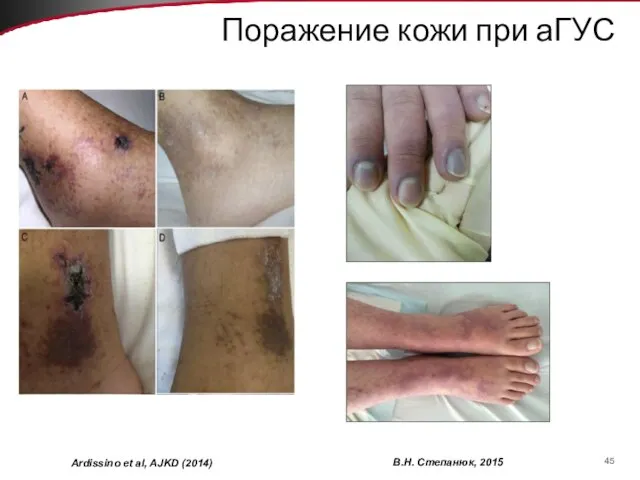
- 45. Поражение кожи при аГУС Ardissino et al, AJKD (2014) В.Н. Степанюк, 2015
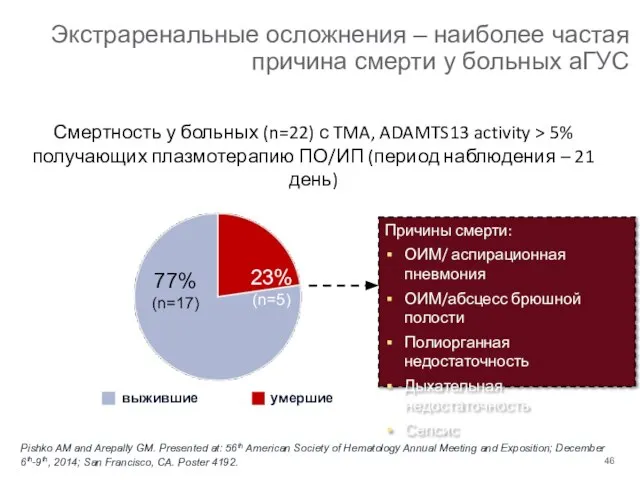
- 46. Экстраренальные осложнения – наиболее частая причина смерти у больных аГУС выжившие Смертность у больных (n=22) с
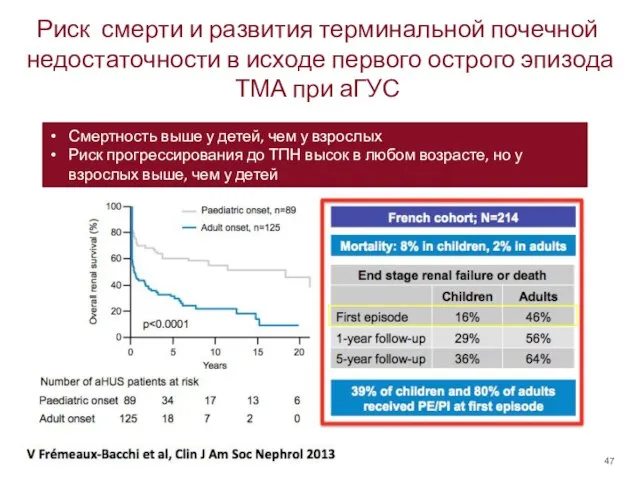
- 47. Риск смерти и развития терминальной почечной недостаточности в исходе первого острого эпизода ТМА при аГУС Смертность
- 48. Диагноз и дифференциальный диагноз при ТМА: основные принципы Диагностика должна быть быстрой – в течение 24
- 49. Трудности ранней диагностики аГУС обусловлены: Полиморфизмом и схожестью клинических проявлений ТМА Манифестацией ранними неспецифическими симптомами или
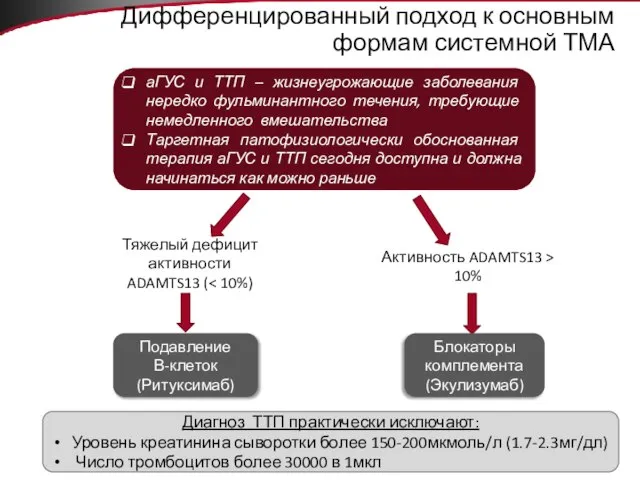
- 50. Дифференцированный подход к основным формам системной ТМА аГУС и ТТП – жизнеугрожающие заболевания нередко фульминантного течения,
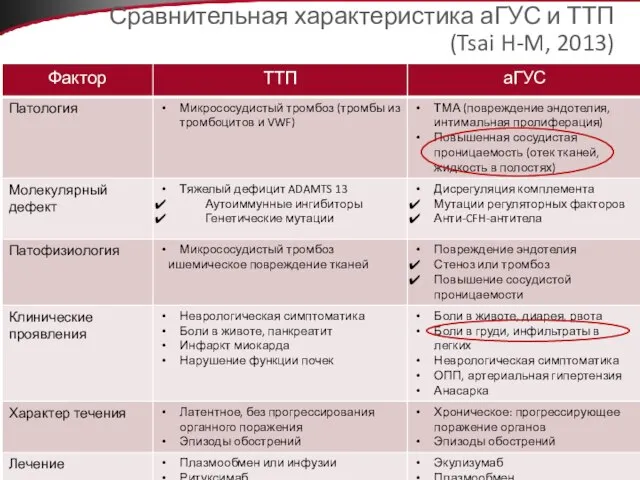
- 51. Сравнительная характеристика аГУС и ТТП (Tsai H-M, 2013)
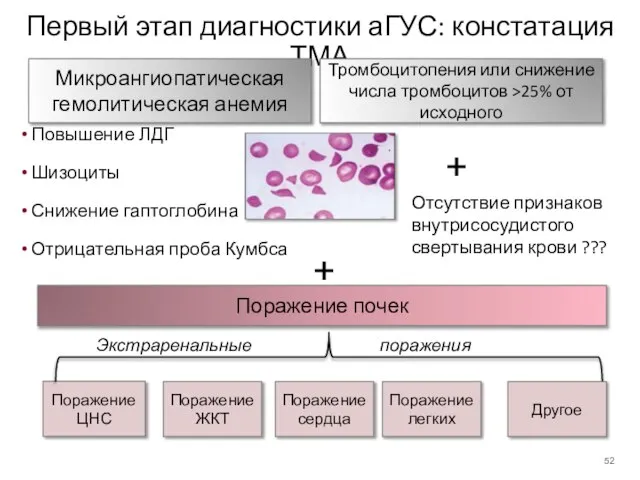
- 52. Первый этап диагностики аГУС: констатация ТМА Повышение ЛДГ Шизоциты Снижение гаптоглобина Отрицательная проба Кумбса Тромбоцитопения или
- 53. Второй этап: диагноз и дифференциальная диагностика аГУС Генетический скрининг Факторы комплемента ADАMTS13 Тесты на Шига-токсин C3,
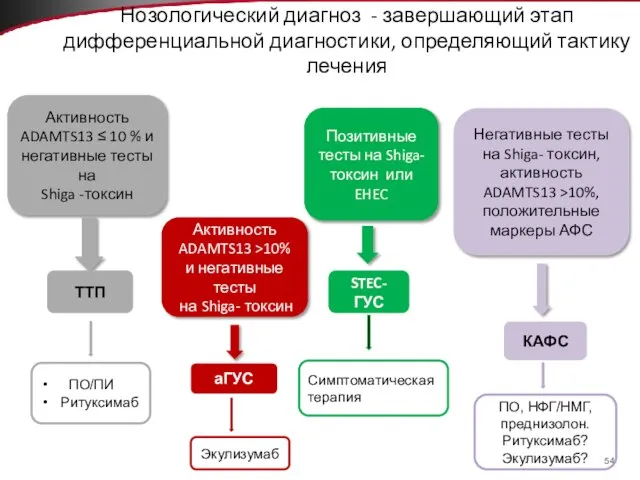
- 54. Активность ADAMTS13 ≤ 10 % и негативные тесты на Shiga -токсин Активность ADAMTS13 >10% и негативные
- 55. Алгоритм терапевтического действия при ТМА с подозрением на аГУС Начало с плазмообмена при любой ТМА (в
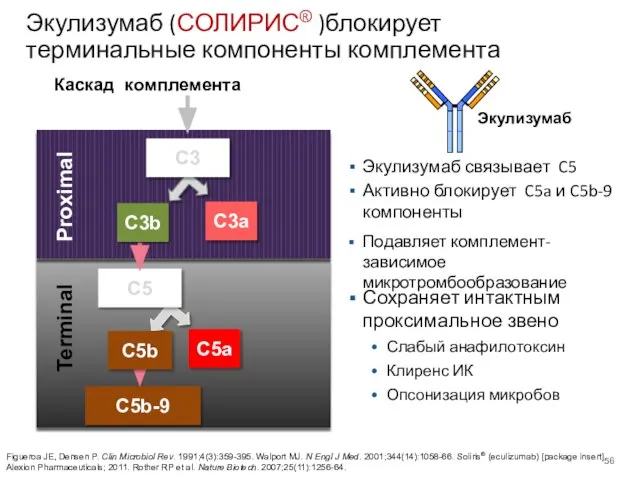
- 56. Экулизумаб (СОЛИРИС® )блокирует терминальные компоненты комплемента C5 Proximal Terminal Figueroa JE, Densen P. Clin Microbiol Rev.
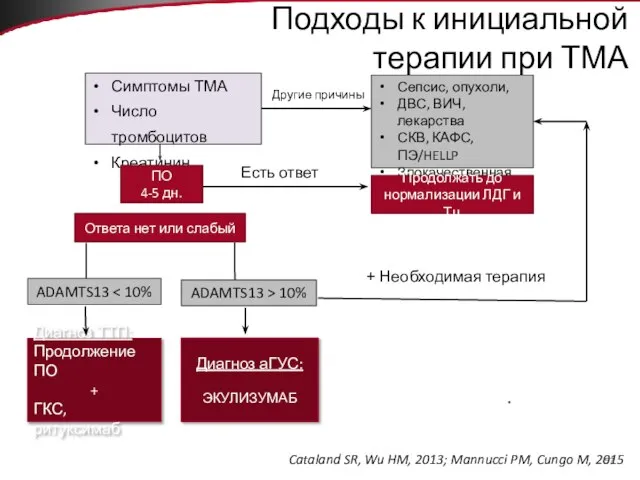
- 57. Симптомы ТМА Число тромбоцитов Креатинин Сепсис, опухоли, ДВС, ВИЧ, лекарства СКВ, КАФС, ПЭ/HELLP Злокачественная АГ ADAMTS13
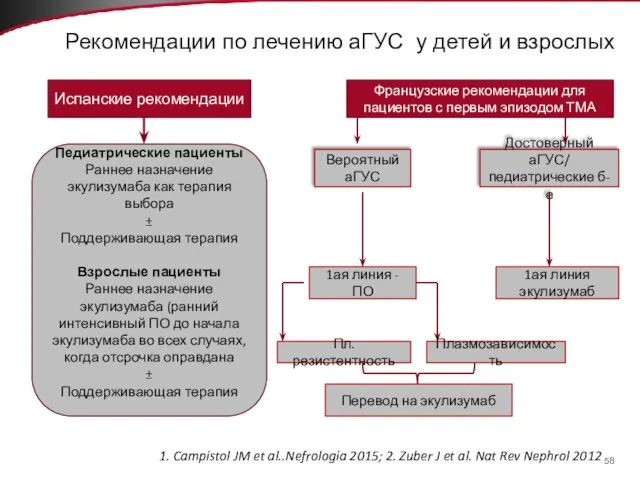
- 58. Рекомендации по лечению аГУС у детей и взрослых Испанские рекомендации Педиатрические пациенты Раннее назначение экулизумаба как
- 59. Атипичный ГУС как заболевание с полиорганным поражением нуждается в мультидисциплинарном подходе Data from the aHUS poll
- 61. Скачать презентацию

















 Сетевые программы повышения квалификации
Сетевые программы повышения квалификации Поиск Instagram-блогеров для рекламы
Поиск Instagram-блогеров для рекламы Что такое зоопарк (1 класс)
Что такое зоопарк (1 класс) Как наступает листопад
Как наступает листопад Computer Viruses
Computer Viruses Конкурс занимательной грамматики
Конкурс занимательной грамматики Питание и пищеварение 6 класс
Питание и пищеварение 6 класс Маркетинг_лекция 8_презентация
Маркетинг_лекция 8_презентация Индивидуальный предприниматель Богатко Антон Викторович
Индивидуальный предприниматель Богатко Антон Викторович Презентация на тему Англия в эпоху Тюдоров
Презентация на тему Англия в эпоху Тюдоров  Аммиак NH3
Аммиак NH3 Proyecto galeno
Proyecto galeno Уборка квартир. Стоимость услуг
Уборка квартир. Стоимость услуг Импровизация
Импровизация Биоэтика
Биоэтика Психолого-педагогическая адаптация детей, проживающих с приемными родителями
Психолого-педагогическая адаптация детей, проживающих с приемными родителями Задание 4. Строение кожи человека.
Задание 4. Строение кожи человека. ПОЛЬЗОВАТЕЛЬ – ОТНОШЕНИЯ К НОВЫМ СЕРВИСАМ БИБЛИОТЕКИ По материалам исследования
ПОЛЬЗОВАТЕЛЬ – ОТНОШЕНИЯ К НОВЫМ СЕРВИСАМ БИБЛИОТЕКИ По материалам исследования Царицына – Сталинграда – Волгограда
Царицына – Сталинграда – Волгограда МариМолоко - наслаждение доступное каждому
МариМолоко - наслаждение доступное каждому 111
111 BILLING as SERVICE
BILLING as SERVICE Ситуация на рынке недвижимости Беларуси
Ситуация на рынке недвижимости Беларуси Правовые и иные аспекты реализации инновационных проектов
Правовые и иные аспекты реализации инновационных проектов ВЗАИМОДЕЙСТВИЕ СЕМЬИ И ШКОЛЫ В ПРОФИЛАКТИКЕ АСОЦИАЛЬНЫХ ЯВЛЕНИЙ
ВЗАИМОДЕЙСТВИЕ СЕМЬИ И ШКОЛЫ В ПРОФИЛАКТИКЕ АСОЦИАЛЬНЫХ ЯВЛЕНИЙ Земельные ресурсы мира
Земельные ресурсы мира Жизненный цикл архитектурного проекта. Тема 10
Жизненный цикл архитектурного проекта. Тема 10 Презентация на тему Отношения и пропорции
Презентация на тему Отношения и пропорции