Содержание
- 2. Оглавление Введение 3 слайд Основная часть 4-9 слайд Вывод 10 слайд Список используемой литературы 11 слайд
- 3. Введение Цель: Исследовать и изучить свойства истинных растворов. Для достижения поставленной цели мы выявили следующие задачи:
- 4. Основная часть 1. Раствор – гомогенная (однородная) система, состоящая из частиц растворенного вещества, растворителя и продуктов
- 6. 2. Движущими силами образования растворов являются энтропийный и энтальпийный факторы. При растворении газов в жидкости энтропия
- 7. 3. Истинные растворы бывают ионно-дисперсными и молекулярно-дисперсными. Размер частиц в первых составляет менее 1 нм, а
- 8. 4. Рассмотрим размеры истинных веществ на примере хлорида натрия. Кристаллы любого вещества, например хлорид натрия, можно
- 9. 5. Истинными называются растворы, в которых растворенное вещество находится в ионной форме. Причиной разложения в воде
- 10. Вывод ✵Проведя исследования, я пришла к следующим выводам: 1. Растворы называют истинными, когда вещество находится в
- 12. Скачать презентацию
Слайд 2Оглавление
Введение 3 слайд
Основная часть 4-9 слайд
Вывод 10 слайд
Список используемой литературы 11
Оглавление
Введение 3 слайд
Основная часть 4-9 слайд
Вывод 10 слайд
Список используемой литературы 11

слайд
Слайд 3Введение
Цель: Исследовать и изучить свойства истинных растворов.
Для достижения поставленной цели мы
Введение
Цель: Исследовать и изучить свойства истинных растворов.
Для достижения поставленной цели мы

выявили следующие задачи:
Выяснить какие растворы называются истинными;
❷Определить движущие силы образования растворов;
❸Выяснить особенность истинных растворов;
❹Определить размеры истинных растворов на примере хлорида натрия;
❺Определить принцип разложения истинных растворов.
Выяснить какие растворы называются истинными;
❷Определить движущие силы образования растворов;
❸Выяснить особенность истинных растворов;
❹Определить размеры истинных растворов на примере хлорида натрия;
❺Определить принцип разложения истинных растворов.
Слайд 4Основная часть
1. Раствор – гомогенная (однородная) система, состоящая из частиц растворенного
Основная часть
1. Раствор – гомогенная (однородная) система, состоящая из частиц растворенного

вещества, растворителя и продуктов их взаимодействия.
Растворы все однофазны, то есть представляют собой однородный газ, жидкость или твердое вещество. Это связано с тем, что одно из веществ распределено в массе другого в виде молекул, атомов и ионов.
Когда вещество находится в окружающей среде в виде молекул или ионов, то такие растворы называют истинными, т.е. гомогенными однофазными растворами. В истинных растворах (часто называемых просто растворами) растворенное вещество диспергировано до атомного или молекулярного уровня, частицы растворенного вещества не видимы ни визуально, ни под микроскопом, свободно передвигаются в среде растворителя. Истинные растворы – термодинамически устойчивые системы, неограниченно стабильные во времени.
Растворы все однофазны, то есть представляют собой однородный газ, жидкость или твердое вещество. Это связано с тем, что одно из веществ распределено в массе другого в виде молекул, атомов и ионов.
Когда вещество находится в окружающей среде в виде молекул или ионов, то такие растворы называют истинными, т.е. гомогенными однофазными растворами. В истинных растворах (часто называемых просто растворами) растворенное вещество диспергировано до атомного или молекулярного уровня, частицы растворенного вещества не видимы ни визуально, ни под микроскопом, свободно передвигаются в среде растворителя. Истинные растворы – термодинамически устойчивые системы, неограниченно стабильные во времени.
Слайд 62. Движущими силами образования растворов являются энтропийный и энтальпийный факторы. При растворении
2. Движущими силами образования растворов являются энтропийный и энтальпийный факторы. При растворении

газов в жидкости энтропия всегда уменьшается ΔS < 0, а при растворении кристаллов возрастает (ΔS > 0). Чем сильнее взаимодействие растворенного вещества и растворителя, тем больше роль энтальпийного фактора в образовании растворов. Знак изменения энтальпии растворения определяется знаком суммы всех тепловых эффектов процессов, сопровождающих растворение, из которых основной вклад вносят разрушение кристаллической решетки на свободные ионы (ΔH > 0) и взаимодействие образовавшихся ионов с молекулами растворителя (сольтивация, ΔH < 0). При этом независимо от знака энтальпии при растворении (абсолютно нерастворимых веществ нет) всегда ΔG = ΔH – T·ΔS < 0, т. к. переход вещества в раствор сопровождается значительным возрастанием энтропии вследствие стремления системы к разупорядочиванию. Для жидких растворов (расплавов) процесс растворения идет самопроизвольно (ΔG < 0) до установления динамического равновесия между раствором и твердой фазой.
Слайд 7
3. Истинные растворы бывают ионно-дисперсными и молекулярно-дисперсными. Размер частиц в
3. Истинные растворы бывают ионно-дисперсными и молекулярно-дисперсными. Размер частиц в

первых составляет менее 1 нм, а растворенное вещество находится в виде отдельных гидратированных ионов и молекул в равновесных количествах. Истинные растворы всегда прозрачны, они не должны содержать взвешенных частиц и осадка. Особенностью истинных растворов является то, что они гомогенны даже при рассматривании в электронный микроскоп. Компоненты, входящие в их состав, не могут быть разделены никаким способом. Истинные растворы хорошо диффундируют. К этой группе относятся растворы электролитов и неэлектролитов, таких как глюкоза, натрия хлорид, спирт, магния сульфат и т.д.
Слайд 8
4. Рассмотрим размеры истинных веществ на примере хлорида натрия. Кристаллы любого
4. Рассмотрим размеры истинных веществ на примере хлорида натрия. Кристаллы любого
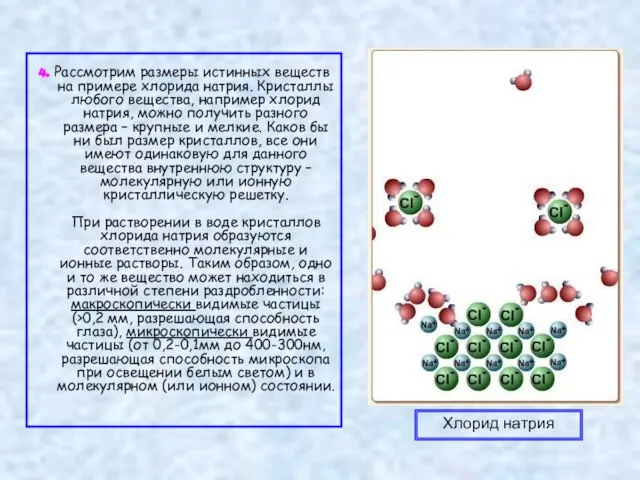
вещества, например хлорид натрия, можно получить разного размера – крупные и мелкие. Каков бы ни был размер кристаллов, все они имеют одинаковую для данного вещества внутреннюю структуру – молекулярную или ионную кристаллическую решетку.
При растворении в воде кристаллов хлорида натрия образуются соответственно молекулярные и ионные растворы. Таким образом, одно и то же вещество может находиться в различной степени раздробленности: макроскопически видимые частицы (>0,2 мм, разрешающая способность глаза), микроскопически видимые частицы (от 0,2-0,1мм до 400-300нм, разрешающая способность микроскопа при освещении белым светом) и в молекулярном (или ионном) состоянии.
Хлорид натрия
Слайд 95. Истинными называются растворы, в которых растворенное вещество находится в ионной форме.
5. Истинными называются растворы, в которых растворенное вещество находится в ионной форме.

Причиной разложения в воде молекул вещества на ионы является электролитическая диссоциация электролитов. Процесс электролитической диссоциации, например, соляной и угольной кислот можно выразить формулами:
НСl —› Н+ + Сl-
Н2СO3 —› Н+ + НСO3-;
НСO3- —› Н+ + СO32-;
В ионном растворе соблюдается принцип электронейтральности, поэтому в нем всегда находится равное число эквивалентов катионов и анионов. Катионы имеют положительный заряд и названы так потому, что при электролизе движутся к катоду. Анионы же имеют отрицательный заряд и при электролизе движутся к аноду.
Слайд 10Вывод
✵Проведя исследования, я пришла к следующим выводам:
1. Растворы называют истинными, когда
Вывод
✵Проведя исследования, я пришла к следующим выводам:
1. Растворы называют истинными, когда

вещество находится в окружающей среде в виде молекул или ионов.
2. Движущими силами образования растворов являются энтропийный и энтальпийный факторы.
3. Особенностью истинных растворов является то, что они гомогенны даже при рассматривании в электронный микроскоп. Компоненты, входящие в их состав, не могут быть разделены никаким способом. Истинные растворы хорошо диффундируют.
4. Одно и то же вещество может находиться в различной степени раздробленности: макроскопически видимые частицы (>0,2 мм, разрешающая способность глаза), микроскопически видимые частицы (от 0,2-0,1мм до 400-300нм, разрешающая способность микроскопа при освещении белым светом) и в молекулярном (или ионном) состоянии.
5. В ионном растворе соблюдается принцип электронейтральности, поэтому в нем всегда находится равное число эквивалентов катионов и анионов.
2. Движущими силами образования растворов являются энтропийный и энтальпийный факторы.
3. Особенностью истинных растворов является то, что они гомогенны даже при рассматривании в электронный микроскоп. Компоненты, входящие в их состав, не могут быть разделены никаким способом. Истинные растворы хорошо диффундируют.
4. Одно и то же вещество может находиться в различной степени раздробленности: макроскопически видимые частицы (>0,2 мм, разрешающая способность глаза), микроскопически видимые частицы (от 0,2-0,1мм до 400-300нм, разрешающая способность микроскопа при освещении белым светом) и в молекулярном (или ионном) состоянии.
5. В ионном растворе соблюдается принцип электронейтральности, поэтому в нем всегда находится равное число эквивалентов катионов и анионов.
 Государственный и муниципальный кредит
Государственный и муниципальный кредит Подготовка к ГИА. Знаки препинания в сложносочиненном и сложноподчиненном предложении
Подготовка к ГИА. Знаки препинания в сложносочиненном и сложноподчиненном предложении Что такое постдемократия
Что такое постдемократия Возникновение искусства тату и профессии татуировщика
Возникновение искусства тату и профессии татуировщика Рабочая инструкция сборки формы “Вилка стойки” 12300-2905515-01 KURTZ
Рабочая инструкция сборки формы “Вилка стойки” 12300-2905515-01 KURTZ Стратегическая модель Ж. -М. Дрю
Стратегическая модель Ж. -М. Дрю  Презентация на тему Измерение физических величин
Презентация на тему Измерение физических величин Чьи глаза?
Чьи глаза? «Шведский стол»
«Шведский стол» Иосиф Дик «Красные яблоки»
Иосиф Дик «Красные яблоки» Презентация на тему ПРОСТЕЙШИЕ
Презентация на тему ПРОСТЕЙШИЕ  Этикет 4 класс
Этикет 4 класс Произведения народного искусства
Произведения народного искусства Сравнительный анализ доходности индексных ПИФов и ПИФов акций
Сравнительный анализ доходности индексных ПИФов и ПИФов акций Presentation Title
Presentation Title  Die Geschichte des Fußballs
Die Geschichte des Fußballs Как мы общаемся с миром
Как мы общаемся с миром My favorite company
My favorite company Презентация
Презентация День правовой помощи детям
День правовой помощи детям Принятие решений в условиях существования рисков с низкими вероятностями реализации
Принятие решений в условиях существования рисков с низкими вероятностями реализации Письмо
Письмо Тактильная чувствительность
Тактильная чувствительность Инвестиция, как важнейшее условие для реализации проекта
Инвестиция, как важнейшее условие для реализации проекта Конструирование брюк
Конструирование брюк ПРОГРАМНЕ ЗАБЕЗПЕЧЕННЯ СПЕЦІАЛЬНИХ ІНФОРМАЦІЙНО-ТЕЛЕКОМУНІКАЦІЙНИХ СИСТЕМ
ПРОГРАМНЕ ЗАБЕЗПЕЧЕННЯ СПЕЦІАЛЬНИХ ІНФОРМАЦІЙНО-ТЕЛЕКОМУНІКАЦІЙНИХ СИСТЕМ Особенности продвижения транспортных услуг
Особенности продвижения транспортных услуг Священнослужители в рядах Русской армии
Священнослужители в рядах Русской армии