Содержание
- 2. Цели урока Образовательная -- рассмотрение строения атома, аллотропии углерода; формирование представлений о строении, свойствах и применении
- 3. +6С )2)4 +14Si )2)8)4 +32Ge )2)8)18)4 +50Sn )2)8)18)18)4 +82Pb )2)8)18)32)18)4 Общая электронная формула внешнего слоя S2
- 4. Изменение свойств в группе С Si Ge Sn Pb Металлические свойства увеличиваются
- 5. Порядковый номер – 6 Строение атома: протонов – 6, нейтронов – 6, электронов – 6 Энергетических
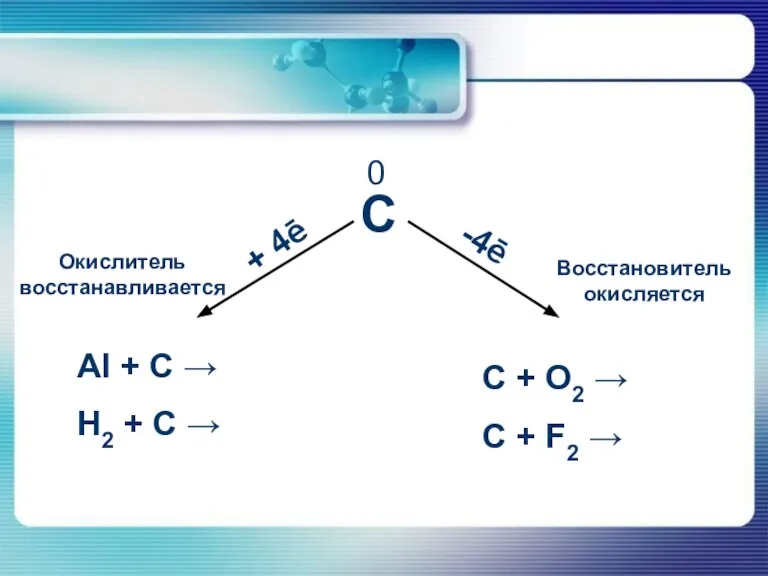
- 6. 0
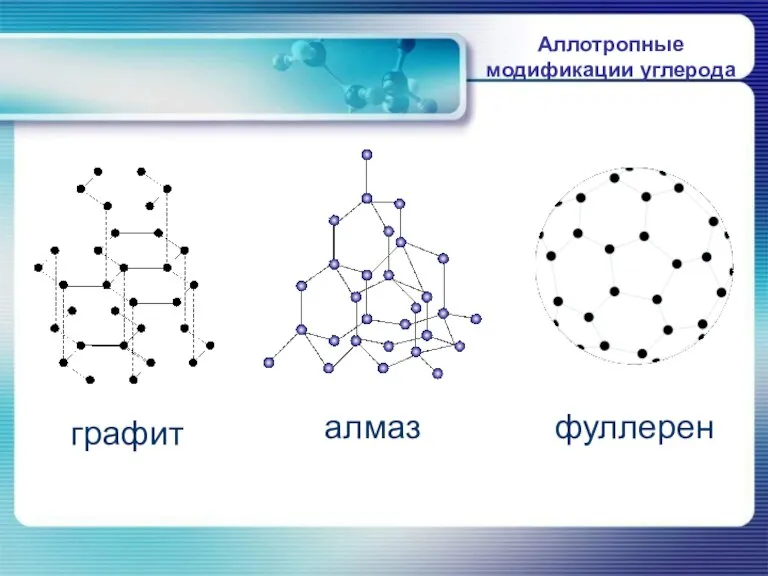
- 7. Аллотропные модификации углерода графит алмаз фуллерен
- 8. А Л М А З
- 10. Звезда ордена Св. Андрея Первозванного Алмаз «Шах» Скипетр императорский
- 11. Большая императорская корона Малая императорская корона
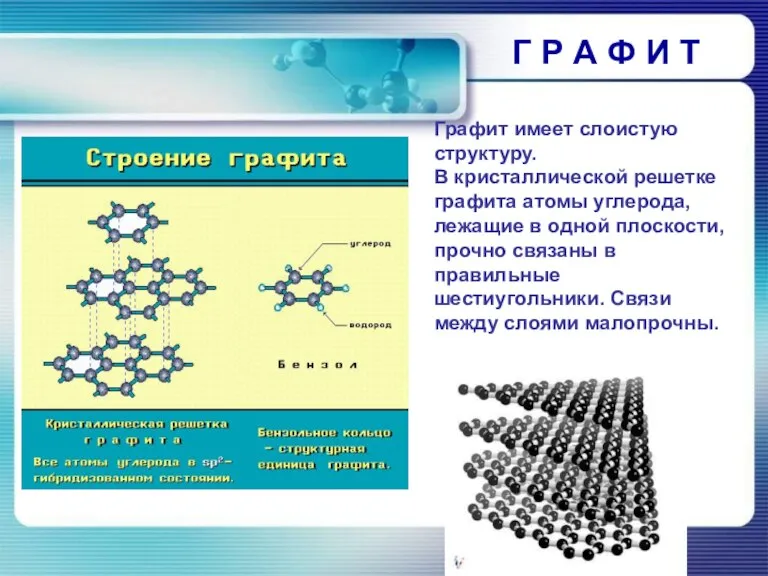
- 12. Г Р А Ф И Т Применение графита: Электроды для электролиза Облицовка сопел ракетных двигателей Смазка
- 13. П О Ч Е М У А Л М А З - очень твердый, Г Р
- 14. А Л М А З Алмаз имеет атомную кристаллическую решетку, в которой каждый атом углерода связан
- 15. Г Р А Ф И Т Графит имеет слоистую структуру. В кристаллической решетке графита атомы углерода,
- 16. Г Р А Ф И Т Сходное с графитом строение имеют: Сажа Древесный уголь Кокс типографская
- 17. Н.Д.Зелинский
- 18. Угольные фильтры В бытовых фильтрах, в промышленном производстве, на очистных сооружениях – уголь поглощает вредные вещества
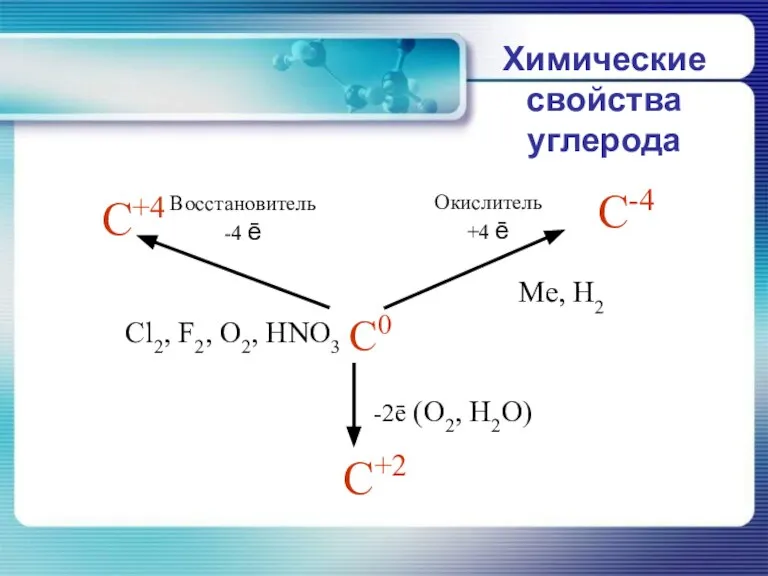
- 19. Химические свойства углерода
- 20. Химические свойства углерода В реакциях с активными неметаллами углерод легко окисляется: C+O2=CO2 2C+O2=2CO C+2S=CS2 C+2F2=CF4 Углерод
- 21. Т е с т 1. Конфигурация внешнего электронного уровня элементов подгруппы углерода: а) ns2np2 б) ns2np3
- 22. ПРОВЕРЬ ПОЛУЧЕННЫЕ ЗНАНИЯ Ответы к тесту 1.а; 2.в; 3.а; 4.б; 5.в; 6.а; 7.в
- 24. Скачать презентацию

















 Выбор способа обучения: модель обратного дизайна
Выбор способа обучения: модель обратного дизайна Адвокатура и ее функции
Адвокатура и ее функции Правописание разделительного Ъ
Правописание разделительного Ъ Международный коммерческий арбитраж Подготовила Гусева А.ю. МЭ081
Международный коммерческий арбитраж Подготовила Гусева А.ю. МЭ081 Дуговая и газовая сварка
Дуговая и газовая сварка Четырёхзначные числа
Четырёхзначные числа Системные платы
Системные платы Искусство и духовная жизнь (10 класс)
Искусство и духовная жизнь (10 класс) Презентация на тему: Первая помощь при повреждениях скелета
Презентация на тему: Первая помощь при повреждениях скелета Университеты Тарту и Варшавы. Учёба по обмену
Университеты Тарту и Варшавы. Учёба по обмену Афиша и плакат. Рисование на бумаге красками и карандашами
Афиша и плакат. Рисование на бумаге красками и карандашами Financial indicators_rus
Financial indicators_rus Школьные аксессуары
Школьные аксессуары Дети говорят телефону доверия «Да!» 17 мая – Международный день детского телефона доверия
Дети говорят телефону доверия «Да!» 17 мая – Международный день детского телефона доверия «Личностный рост каждого обучающегося как результат педагогического процесса»
«Личностный рост каждого обучающегося как результат педагогического процесса» Правовое регулирование налоговых отношений
Правовое регулирование налоговых отношений Формирование личности средствами физической культуры
Формирование личности средствами физической культуры инфа
инфа N4Cast
N4Cast My expectations at the
My expectations at the …На протяжении всей нашей жизни фотография показывает нам события, происходившие далеко от нас, сохраняя и удерживая облик тех, ко
…На протяжении всей нашей жизни фотография показывает нам события, происходившие далеко от нас, сохраняя и удерживая облик тех, ко Обучение одаренных детей
Обучение одаренных детей Авангардизм - новаторство в искусстве. Тема 8
Авангардизм - новаторство в искусстве. Тема 8 Женщины – Герои Советского Союза
Женщины – Герои Советского Союза Директор по направлению «Экология и энергоэффективность»ЗАО «АПБЭ» О.А. Новоселова
Директор по направлению «Экология и энергоэффективность»ЗАО «АПБЭ» О.А. Новоселова Урок: Синквейн по роману М. Булгакова «Мастер и Маргарита»
Урок: Синквейн по роману М. Булгакова «Мастер и Маргарита» Белорусский костюм (1)
Белорусский костюм (1) Промышленные клеи-аэрозоли
Промышленные клеи-аэрозоли