Слайд 2 План
1.Повторение пройденного:
а)Рассказ о строении и свойствах алкенов по
плану упр.2.
б)Решение задачи: Рассчитать

объем этилена,
полученный дегидрированием 30 л этана,
содержащего 10% неорганических примесей.
в)Вопрос к упр. 4 «Каким способом пропанол- -1 можно превратить в пропанол – 2?»
2.Гомологический ряд алкинов, изомерия,
номенклатура.
Слайд 33.Строение ацетилена, третье валентное
состояние углерода.
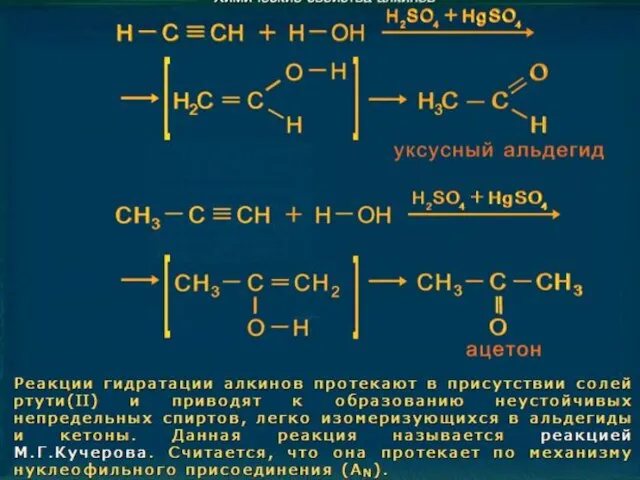
4.Свойства ацетилена.
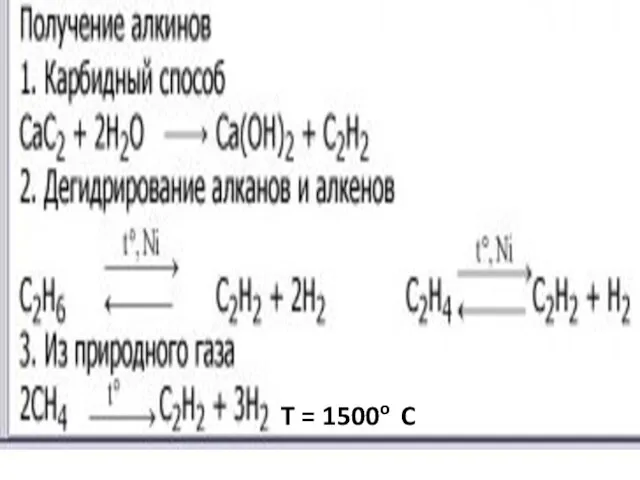
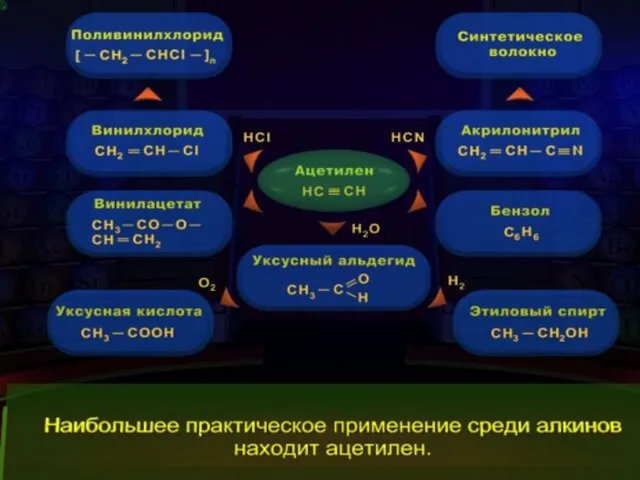
5.Получение и применение алкинов.
Д/з: №6, упр.4(б),6,

с.51.
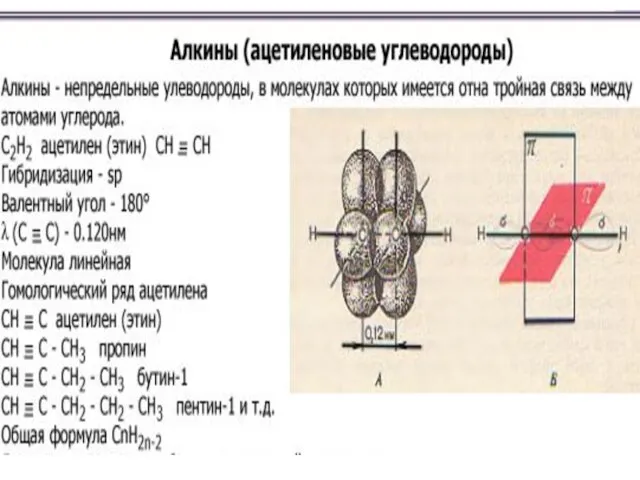
Слайд 71.Алкины – это непредельные УВ, которые имеют
одну тройную связь. Атомы углерода при

тройной
связи находятся в sp – гибридизации, которая
состоит из одной σ – связи и двух π – связей.
При этом π – связи располагаются взаимно
перпендикулярно.
Углеродные атомы стягиваются тройной связью
до 0,120 нм, валентный угол = 180о .
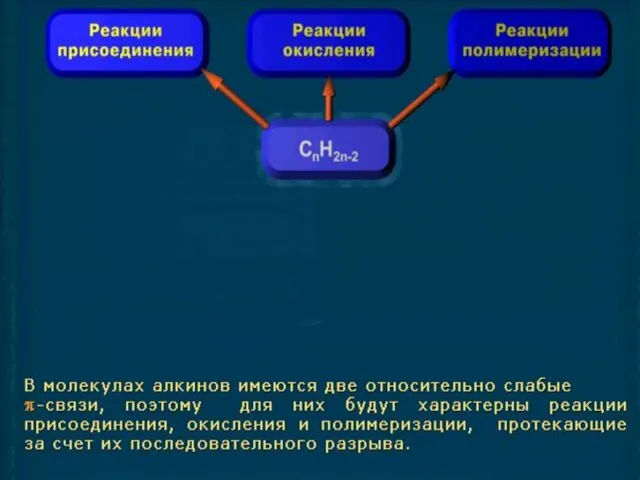
Слайд 9Алкины вступают в те же реакции присоединения и окисления, что и алкены.

Однако, скорость данных реакций меньше и протекают они в две стадии, так как
энергия тройной связи больше, чем двойной, а также
последовательно разрушаются две π – связи. Форма
молекулы меняется из линейной в плоскостную и затем -
в тетраэдрическую.
Слайд 11 На катализаторе CuCl атому углерода». образуется винилацетилен СН = С –
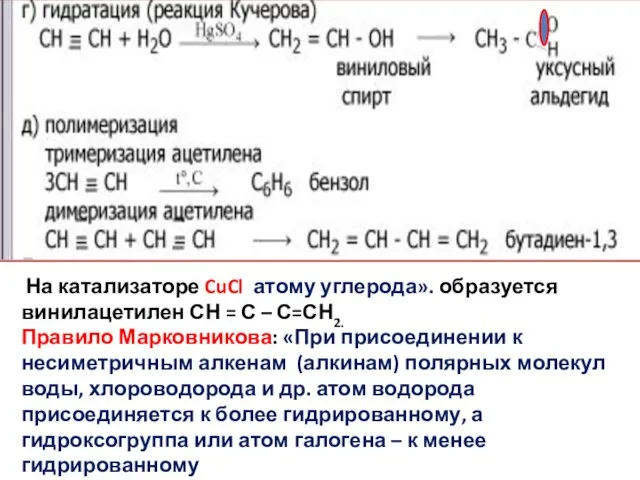
С=СН2.
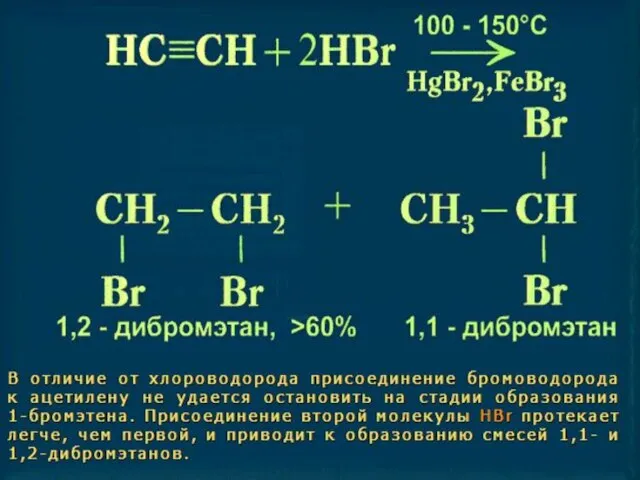
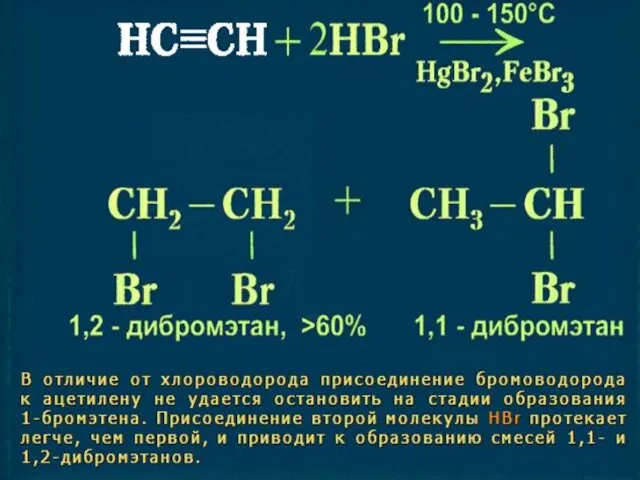
Правило Марковникова: «При присоединении к несиметричным алкенам (алкинам) полярных молекул воды, хлороводорода и др. атом водорода присоединяется к более гидрированному, а гидроксогруппа или атом галогена – к менее гидрированному
атому углерода.
Слайд 14Дополнение к элективному
курсу
1.Исследование присоединения полярных молекул по правилу Марковникова
2.











 Агентство ИТ-Фабрика. Техника безопасного пиара
Агентство ИТ-Фабрика. Техника безопасного пиара Альтернатива ипотеке. Уникальное предложение New Millennium Centre LTD
Альтернатива ипотеке. Уникальное предложение New Millennium Centre LTD Презентация на тему Органы дыхания человека
Презентация на тему Органы дыхания человека  Automotive Industry. Основы теории бережливого производства
Automotive Industry. Основы теории бережливого производства Корпоративная культура
Корпоративная культура Презентация на тему Дисперсные системы (11 класс)
Презентация на тему Дисперсные системы (11 класс) Статистика результатов хозяйственной деятельности
Статистика результатов хозяйственной деятельности ИЗВЛЕЧЕНИЕ ПОЛЬЗЫизинтернет статистики
ИЗВЛЕЧЕНИЕ ПОЛЬЗЫизинтернет статистики Практическая фразеология
Практическая фразеология 6 день презентация
6 день презентация Доказательное Ультразвуковое Исследование Плода.
Доказательное Ультразвуковое Исследование Плода. Кто в доме ядовит?
Кто в доме ядовит? Этнопсихологические особенности представителей казахской национальности
Этнопсихологические особенности представителей казахской национальности Презентация на тему Ступы. Древнейшие храмы мира
Презентация на тему Ступы. Древнейшие храмы мира 1 PEOPLE PERFORMANCE Управление персоналом: международные практики Ольга Ильина Старший Консультант SHL 2011.
1 PEOPLE PERFORMANCE Управление персоналом: международные практики Ольга Ильина Старший Консультант SHL 2011. Us posters
Us posters Слова подарки
Слова подарки автоматизированная система БИОТ - BAYTEREK
автоматизированная система БИОТ - BAYTEREK Презентация на тему Климат Африки Урок географии в 7 классе
Презентация на тему Климат Африки Урок географии в 7 классе Основная документация по проектированию генерального плана и транспорта ГТ
Основная документация по проектированию генерального плана и транспорта ГТ Несколько слов ПРО… Ваш корпоративный праздник…
Несколько слов ПРО… Ваш корпоративный праздник… Паркеты из правильных многоугольников
Паркеты из правильных многоугольников Торговый дом Убежище
Торговый дом Убежище 20171113_antarktida
20171113_antarktida Мечты и проекты
Мечты и проекты Презентация на тему Солнечная энергетика
Презентация на тему Солнечная энергетика Внедрение системы внешнего электронного документооборота с применением Усиленной квалифицированной электронной подписи
Внедрение системы внешнего электронного документооборота с применением Усиленной квалифицированной электронной подписи Курьерский сервис
Курьерский сервис