Содержание
- 2. Сегодня мы отправляемся в гости к кислотам. Наша задача как больше узнать о них.
- 3. 1. Повторить определение кислот, их состав и классификацию. 2. Выяснить значение кислот для человека и природы.
- 4. В природе существует множество различных кислот. Встречались ли вы где-нибудь с кислотами, кроме уроков химии? Выбери
- 5. Пора отправится в гости .Однако, чтобы попасть в дом, необходимо вспомнить адрес хозяев, их имена и
- 6. Ура! Мы определили адрес кислот! Теперь пришла пора познакомиться с ними поближе!
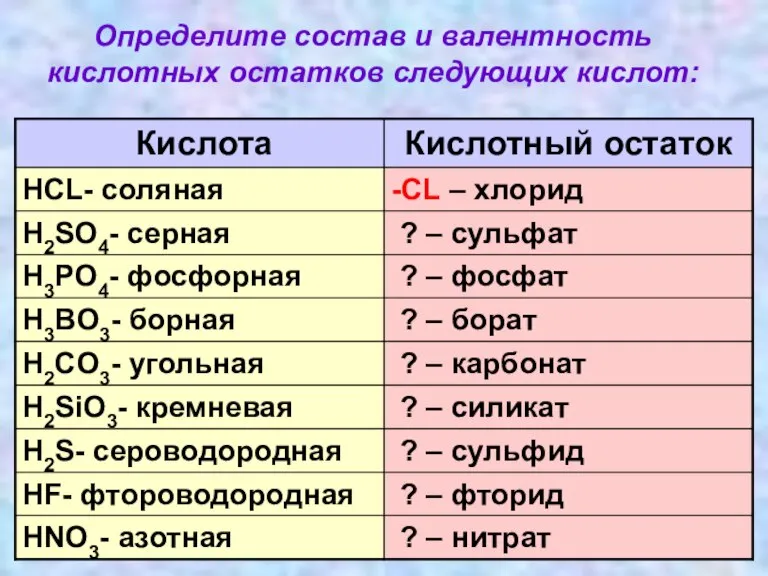
- 7. Определите состав и валентность кислотных остатков следующих кислот:
- 8. Мы попали в комнату, где много гостей. Необходимо найти хозяев и выделить их ( выписать формулы
- 9. Интересно, какие кислоты с какими веществами дружат? Однако, это очень своенравные вещества, и чтобы подружиться с
- 10. Химические свойства кислот: 1. Волшебные индикаторы 2. Отношение к металлам: (с разными металлами кислоты дружат по
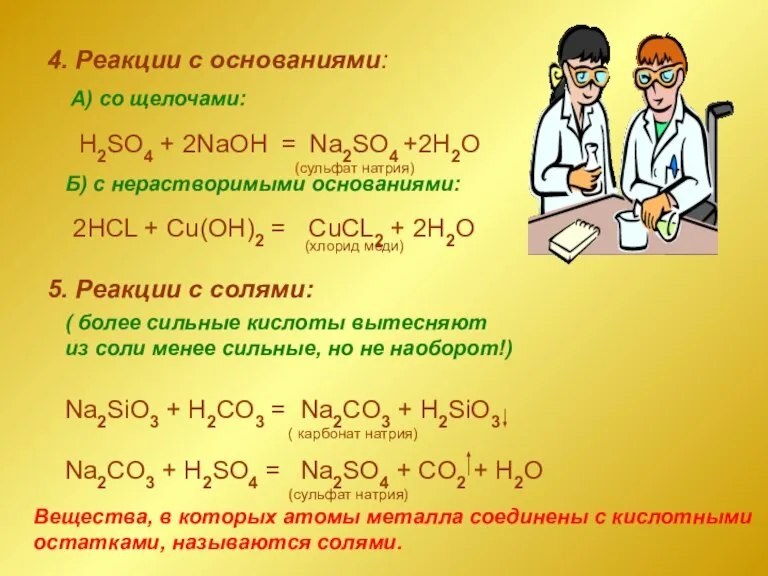
- 11. 4. Реакции с основаниями: H2SO4 + 2NaOH = Na2SO4 +2H2O 2HCL + Cu(OH)2 = CuCL2 +
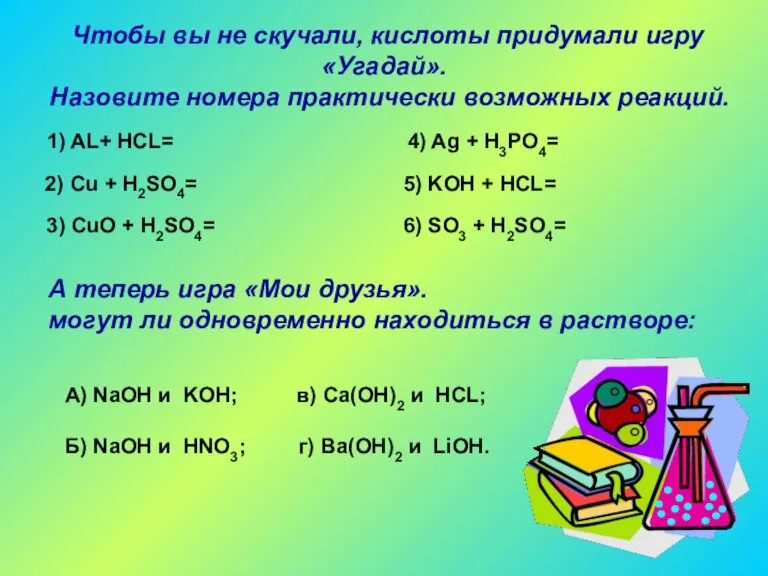
- 12. Чтобы вы не скучали, кислоты придумали игру «Угадай». Назовите номера практически возможных реакций. 1) AL+ HCL=
- 13. Один рассеянный человек писал уравнения реакций и потерял свои записи, остались в памяти только продукты реакции.
- 14. Время в гостях летит быстро, и надо прощаться с хозяевами. Однако неожиданно за окном пошел дождь
- 15. CO2 + H2O = H2CO3 H2SO4 SO2 + H2O = SO3 + H2O = H2SO3 3N02
- 16. Заполните таблицу, вставляя формулы и названия кислот, содержащихся в кислотном дожде, и формулы оксидов из которых
- 18. Скачать презентацию












 Знаковые модели. Моделирование и формализация
Знаковые модели. Моделирование и формализация УРОК ГОРОДА "ГОРОДА-ГЕРОИ"
УРОК ГОРОДА "ГОРОДА-ГЕРОИ" Технологии и инструменты решении проектных задач
Технологии и инструменты решении проектных задач Начальные классы (1-4) система Л.В.Занкова. Программа развивающего обучения.
Начальные классы (1-4) система Л.В.Занкова. Программа развивающего обучения. Эффективные коммуникации
Эффективные коммуникации Кодирование и обработка звуковой информации
Кодирование и обработка звуковой информации Брэйн
Брэйн Пневмонии у детей раннего возраста
Пневмонии у детей раннего возраста Модель Митчелла и Хауса
Модель Митчелла и Хауса Африка
Африка И
И Презентация на тему Сверхпроводимость
Презентация на тему Сверхпроводимость Технология выполнения облицовки поверхностей плитками.
Технология выполнения облицовки поверхностей плитками. ABARUS Market Research
ABARUS Market Research Пруд нашего детства
Пруд нашего детства Восточноукраинский национальный университет им. В. Даля , Луганск, УкраинаОПРЕДЕЛЕНИЯ УДЕЛЬНОЙ ГАММА-АКТИВНОСТИ ПОРОД ШАХТНЫХ
Восточноукраинский национальный университет им. В. Даля , Луганск, УкраинаОПРЕДЕЛЕНИЯ УДЕЛЬНОЙ ГАММА-АКТИВНОСТИ ПОРОД ШАХТНЫХ  Крестьянская реформа 1861 г.
Крестьянская реформа 1861 г. Клуб «Бемби» - школьное лесничество - «Зеленый патруль» - фотостудия - «Марш парков» - сотрудничество с газетой «Эльбрус +»
Клуб «Бемби» - школьное лесничество - «Зеленый патруль» - фотостудия - «Марш парков» - сотрудничество с газетой «Эльбрус +» Управление рисками проекта. Тема 1.6
Управление рисками проекта. Тема 1.6 Презентация на тему Родовые окончания имен существительных
Презентация на тему Родовые окончания имен существительных объединение совладельцев многоквартирных домов- единственный путь реформирования жилищно-коммунального хозяйства города
объединение совладельцев многоквартирных домов- единственный путь реформирования жилищно-коммунального хозяйства города Родительская общественность и органы власти на примере города Магнитогорска
Родительская общественность и органы власти на примере города Магнитогорска Shashki teachvs
Shashki teachvs Размышление учёного мужа, или Смеяться, право, не грешно
Размышление учёного мужа, или Смеяться, право, не грешно Методика: там за поворотом
Методика: там за поворотом Применение ИКТ на уроках в начальной школе
Применение ИКТ на уроках в начальной школе Термообработка стали и чугуна
Термообработка стали и чугуна 22 р.
22 р.