Содержание
- 2. Мы знаем, что вещества состоят из , а молекулы из молекул атомов. Чтобы атомы оставались вместе,
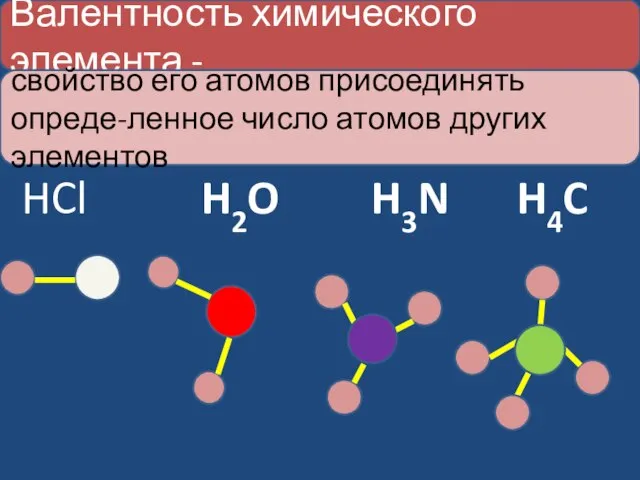
- 3. Валентность химического элемента - свойство его атомов присоединять опреде-ленное число атомов других элементов HCl H3N H2O
- 4. Как же можно узнать валентность элемента? Очень просто! Из таблицы Менделеева! Валентность элемента совпадает с номером
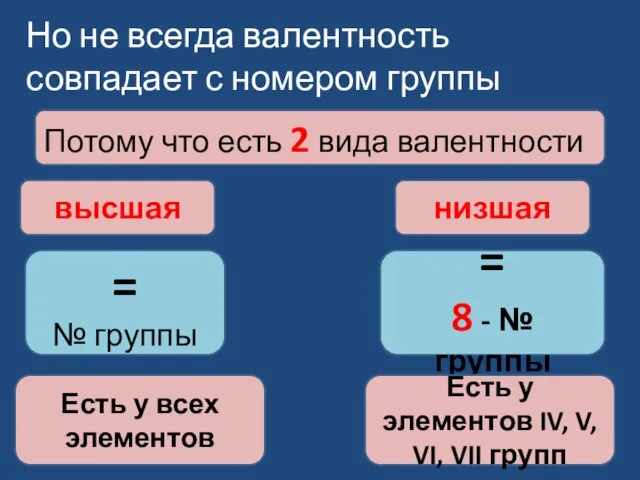
- 5. Но не всегда валентность совпадает с номером группы Потому что есть 2 вида валентности = №
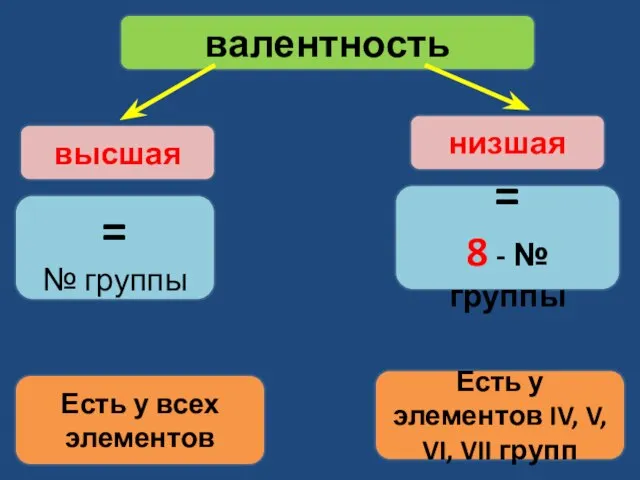
- 6. валентность = № группы высшая = 8 - № группы низшая Есть у всех элементов Есть
- 7. Как узнать, когда элемент обладает высшей валентностью, а когда низшей? Для этого вводят еще одно свойство
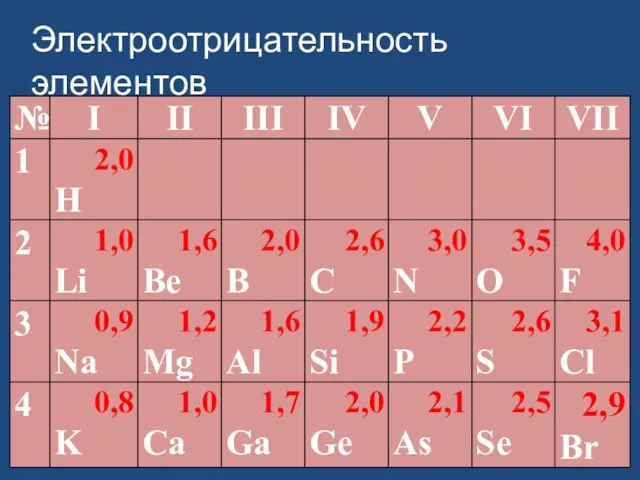
- 8. Электроотрицательность элементов
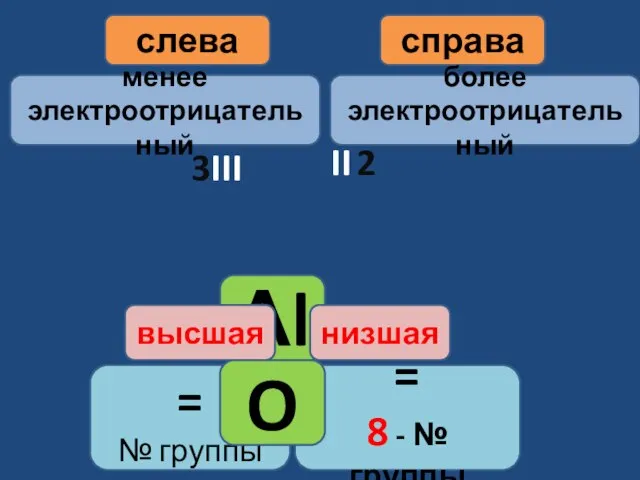
- 9. Договорились, что при составлении формул элемент с большей электро-отрицательностью надо записывать справа, а с меньшей -
- 10. Рядом записываем знаки химических элементов. Определяем валентность элементов: У элемента, который записан слева – она высшая
- 11. Аl = № группы высшая = 8 - № группы низшая слева O справа более электроотрицательный
- 12. Составить формулы соединений, образованных кислородом и натрием, серой и магнием, углеродом и кислородом, углеродом и водородом
- 13. С O IV II 2
- 14. Аl O III II 2 3
- 15. Составить формулы соединений с кислородом следующих элементов Na2O MgO Al2O3 SiO2 P2O5 SO3 Cl2O7
- 16. Составить формулы соединений с хлором следующих элементов NaCl MgCl2 AlCl3 SiCl4 PCl5 SCl6
- 17. Составить формулы соединений с азотом следующих элементов Na3N Mg3N2 Al N Si3N4 P3N5 SN2 NCl5
- 18. Составить формулы соединений с углеродом следующих элементов Na4С Mg2С Al4С3 Si С P4С5 S2С3 С Cl4
- 19. Составить формулы соединений с кислородом следующих элементов СaO В2O3 К2O ZnO CO2 FeO Fe2O3 (II) Железа
- 20. Составить формулы соединений, образованных: Н2O MgН2 Al Р Н3Р Zn3N2 К3N B2O3
- 22. Скачать презентацию














 Презентация на тему Километр (3 класс)
Презентация на тему Километр (3 класс) Известные имена. Софья Ковалевская
Известные имена. Софья Ковалевская Особенности кризиса 2008-2ХХХгг.
Особенности кризиса 2008-2ХХХгг. Графика
Графика Общие вопросы антибактериальной терапии
Общие вопросы антибактериальной терапии Составное глагольное сказуемое
Составное глагольное сказуемое Ch1 - Lecture2
Ch1 - Lecture2 Увеличительные приборы
Увеличительные приборы Болат өндірісінің теориясы мен технологиясы
Болат өндірісінің теориясы мен технологиясы Международные транспортные коридоры
Международные транспортные коридоры Гравюра
Гравюра Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци
Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци Кайнозойская эра
Кайнозойская эра Греция сегодня
Греция сегодня Алгоритм с ветвлением в среде программирования Turbo Pascal
Алгоритм с ветвлением в среде программирования Turbo Pascal ИСКУССТВО ОРИГАМИ
ИСКУССТВО ОРИГАМИ Параметры областного бюджета Тверской области на 2008-2010 годы
Параметры областного бюджета Тверской области на 2008-2010 годы 90 лет ГТО
90 лет ГТО Декоративные народные промыслы
Декоративные народные промыслы Возникновение и развитие логистики
Возникновение и развитие логистики PO
PO Композиция (от лат. compositio)
Композиция (от лат. compositio) Библиотека – как информационная база. Структура библиотеки ВГУЭС
Библиотека – как информационная база. Структура библиотеки ВГУЭС Психологические особенности младших школьников с общим недоразвитием речи
Психологические особенности младших школьников с общим недоразвитием речи Презентация на тему Эра космонавтики
Презентация на тему Эра космонавтики  Чернышов Вадим Геннадьевич. Сертификат участника
Чернышов Вадим Геннадьевич. Сертификат участника САПР ТП ВЕРТИКАЛЬ
САПР ТП ВЕРТИКАЛЬ История развития психопатологии в России
История развития психопатологии в России