Содержание
- 2. §§ Внутренняя энергия газа 02 В модели идеального газа силами взаимодействия молекул пренебрегают Внутренняя энергия газа
- 3. §§ Работа и теплота 03 Вычислим работу газа при расширении p – давление газа F =
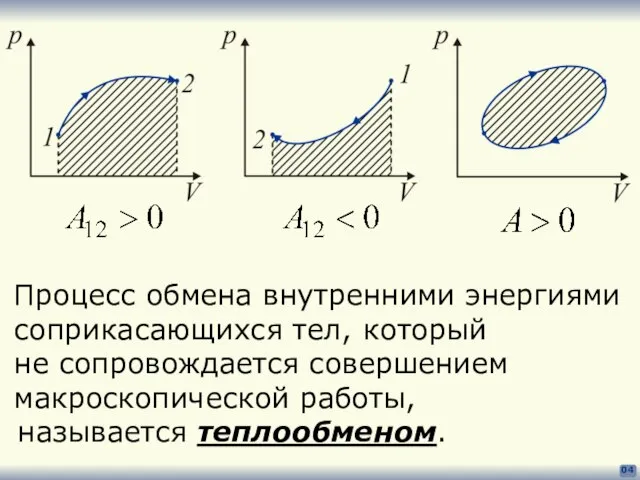
- 4. 04 Процесс обмена внутренними энергиями соприкасающихся тел, который не сопровождается совершением макроскопической работы, называется теплообменом.
- 5. §§ Первое начало 05 Термодинамическая система называется изолированной, если отсутствует всякий обмен энергией между ней и
- 6. 06 Пусть системой α совершена работа A, тогда Рассмотрим контакт систем в адиабатической оболочке. неподвижная теплопроводящая
- 7. идет на приращение ее внутренней энергии ΔU = U2 – U1 07 Получаем математическую формулировку I-го
- 8. §§ Теплоемкость 08 Теплоемкость вещества – физическая величина, равная количеству теплоты, необходимому для нагревания вещества на
- 9. 09 Удельная теплоемкость: Молярная теплоемкость: Из первого начала найдем молярную теплоемкость газа
- 10. 10 1) V = const 2) p = const рассмотрим уравнение М–К:
- 11. 11 Для идеального газа справедливо уравнение Майера Для твердых тел и жидкостей Cp ≈ CV
- 12. §§ Изотермический процесс 12 Это бесконечно медленный процесс, т.к. в системе должно установиться термодинамическое равновесие Закон
- 13. 13 1-е начало термодинамики т.е. вся переданная рабочему телу теплота идет на совершение телом работы Работа
- 14. чтобы не происходил обмен энергией с окружающей средой или он был бы несущественным §§ Адиабатический процесс
- 15. 15 1-е начало термодинамики т.е. работа совершается за счет убыли энергии системы Работа газа при адиабатическом
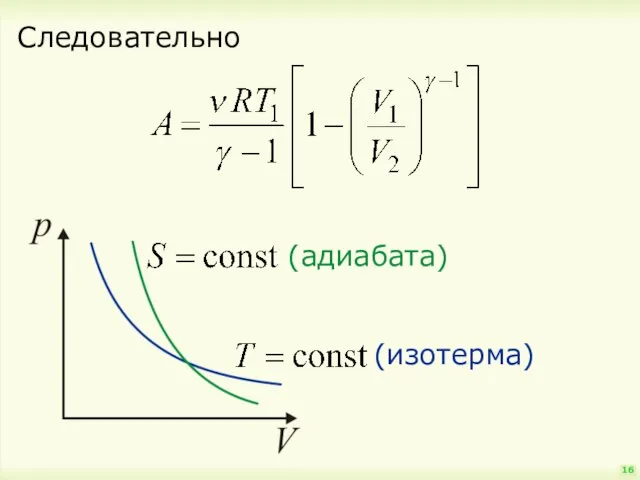
- 16. Следовательно 16
- 17. §§ Политропические процессы 17 Процесс, в котором теплоемкость остается постоянной величиной, называется политропическим (политропным). Рассмотренные процессы
- 18. 18 сделаем замену R = Cp–CV и выразим dT
- 19. 19 Интегрируя, получаем или – уравнение политропы
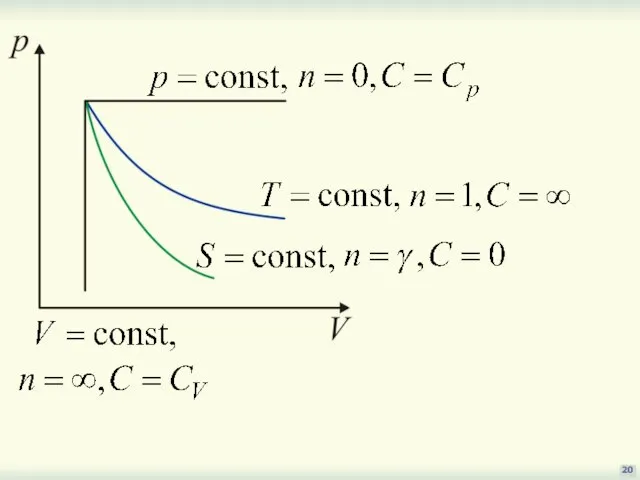
- 20. 20
- 22. Скачать презентацию
















 Презентация на тему Перевод целых чисел в 2, 8, 16-ую системы счисления
Презентация на тему Перевод целых чисел в 2, 8, 16-ую системы счисления Электризация в быту
Электризация в быту Монако
Монако ПАМЯТЬ КОМПЬЮТЕРА
ПАМЯТЬ КОМПЬЮТЕРА Адаптация детей к детскому саду
Адаптация детей к детскому саду Московский областной фонд микрофинансирования
Московский областной фонд микрофинансирования Презентация на тему Влияние шума на организм человека
Презентация на тему Влияние шума на организм человека  Критическое мышление
Критическое мышление  Небесные гости (2 класс)
Небесные гости (2 класс) Йоркширский пудинг
Йоркширский пудинг Наружная реклама для малого и среднего бизнеса
Наружная реклама для малого и среднего бизнеса «Гражданином быть обязан!»
«Гражданином быть обязан!» ПОСЛАНИЯ ВОДЫ
ПОСЛАНИЯ ВОДЫ Сложноподчинённые предложения с придаточным изъяснительным
Сложноподчинённые предложения с придаточным изъяснительным окружной семинар учителей технологии и учителей изобразительного искусства выставка-конкурс творческих работ учащихся "москва
окружной семинар учителей технологии и учителей изобразительного искусства выставка-конкурс творческих работ учащихся "москва  Техника безопасности
Техника безопасности Соматика Томаса Ханны и метод Фельденкрайза
Соматика Томаса Ханны и метод Фельденкрайза Мастер-класс по работе с природным материалом. Пейзажная зарисовка из осенних листьев
Мастер-класс по работе с природным материалом. Пейзажная зарисовка из осенних листьев 20180105_dalniy_vostok
20180105_dalniy_vostok Белорусский государственный университет Филологический факультет
Белорусский государственный университет Филологический факультет Организация работы по привитию культуры питания у школьников
Организация работы по привитию культуры питания у школьников “К информации – без барьеров” Номинация: Дизайнерские решения в библиотеках для людей с ограниченными возможностями
“К информации – без барьеров” Номинация: Дизайнерские решения в библиотеках для людей с ограниченными возможностями Ги Бурден
Ги Бурден Организация единой государственной системы предупреждения и ликвидации чрезвычайных ситуаций(1 урок по теме)
Организация единой государственной системы предупреждения и ликвидации чрезвычайных ситуаций(1 урок по теме) НАЗВАНИЕ ПРОЕКТА и наименование кластера туризм сельское хозяйство лесной комплекс ЖКХ, строительство и благоустройство социаль
НАЗВАНИЕ ПРОЕКТА и наименование кластера туризм сельское хозяйство лесной комплекс ЖКХ, строительство и благоустройство социаль Знаки химических элементов
Знаки химических элементов  Необычная судьба Ф.И. Тютчева – человека и поэта
Необычная судьба Ф.И. Тютчева – человека и поэта Личность и общество. Самоопределение. Типы личности по К. Юнгу
Личность и общество. Самоопределение. Типы личности по К. Юнгу