Содержание
- 2. Задачи урока: Изучить виды химической связи в теме «строение вещества», на данном уроке разобрать причины и
- 3. Этапы урока: Организационный момент: поставить цели и задачи урока. Изучение нового материала.(см. слайды) Закрепление нового материала.
- 4. Это взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы. 4 типа химических связей: Ионная
- 5. Это связь, образовавшаяся за счет электростатического притяжения катионов к анионам. Главный закон химической реакции - заполнение
- 6. Натрий - Na, щелочной металл (группа IA). Электронная конфигурация: 1s22s22p63s1 Как видим, натрий имеет один валентный
- 7. Хлор - Cl, галоген (группа VIIA). Электронная конфигурация: 1s22s22p63s23p5 Как видим, хлор имеет 7 валентных электронов
- 8. почему "дружны" атомы хлора и натрия?
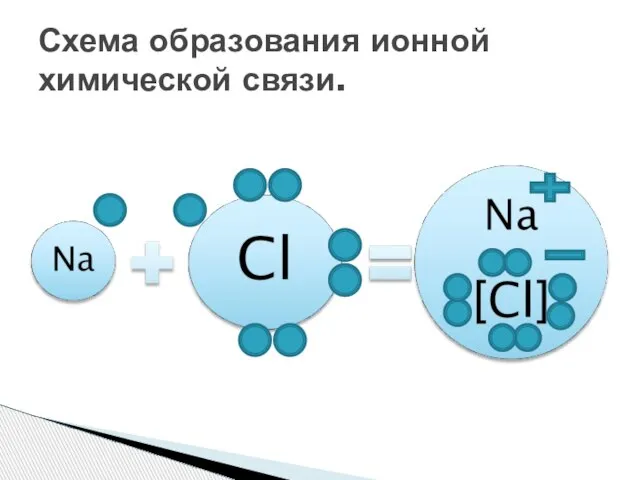
- 9. Схема образования ионной химической связи.
- 10. На внешнем энергетическом уровне атома натрия находится один электрон. Для перехода в стабильное состояние, натрий должен:
- 11. Так что же, натрий превратился в неон? Вовсе нет - не забывайте о протонах! Их по-прежнему;
- 12. Подведем итог: атом натрия и его катион отличаются одним электроном; катион натрия имеет меньший размер, поскольку
- 13. Хлор Cl У хлора ситуация прямо противоположная - на внешнем энергетическом уровне у него находится семь
- 14. Подведем итог: атом хлора примет один электрон и станет отрицательно заряженным анионом (17 протонов и 18
- 15. В результате перемещения электрона образуются ионы: катион натрия (Na+) и анион хлора (Cl-). Поскольку противоположные заряды
- 16. Другие соли образуются по аналогичному принципу, что и хлорид натрия. Металл отдает электроны, а неметалл их
- 17. элементы группы VIIA (галогены) принимают один электрон и образуют анион с зарядом 1-; элементы группы VIA
- 18. Li+ Катион лития Na+ Катион натрия K+ Катион калия Be2+ Катион бериллия Mg2+ Катион магния Ca2+
- 19. F- Анион фтора Cl- Анион хлора Br- Анион брома I- Анион йода O2- Анион кислорода S2-
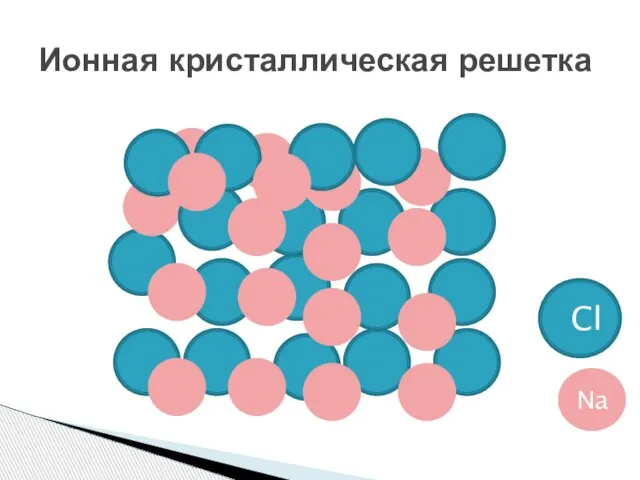
- 20. Ионная кристаллическая решетка Cl Na
- 21. Ионная кристаллическая решетка В кристалле хлорида натрия нельзя выделить отдельные молекулы соли. Их нет. Весь кристалл
- 22. Ионная кристаллическая решетка Плавление ионных кристаллов приводит к нарушению геометрически правильной ориентации ионов относительно друг друга
- 23. Ионная кристаллическая решетка Кальцит CaCO3 Галенит PbS Галит NaCl
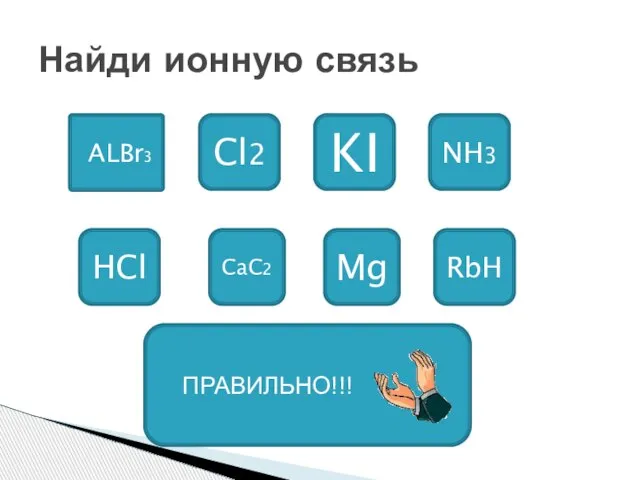
- 24. Найди ионную связь ALBr3 Cl2 KI NH3 HCl CaC2 Mg RbH ПРАВИЛЬНО!!!
- 25. Спасибо за внимание! Презентацию подготовила и провела учитель химии Бойкова А.А.
- 27. Скачать презентацию





















 Service_Training_safety
Service_Training_safety Предыстория информатики
Предыстория информатики Презентация на тему Здоровая нация – счастливая Россия 9-11 класс
Презентация на тему Здоровая нация – счастливая Россия 9-11 класс Библиотека виртуальных загадок и головоломок
Библиотека виртуальных загадок и головоломок Правописание корней с чередованием Е-И
Правописание корней с чередованием Е-И «О проводимой в Ростовской области профилактике социального сиротства среди несовершеннолетних»
«О проводимой в Ростовской области профилактике социального сиротства среди несовершеннолетних» Презентация на тему Как отличить глагол от других частей речи?
Презентация на тему Как отличить глагол от других частей речи? Построение урока на основе системно-деятельностного подхода
Построение урока на основе системно-деятельностного подхода ОРУЖИЕ ПОБЕДЫ
ОРУЖИЕ ПОБЕДЫ Кормление кроликов
Кормление кроликов Подход к инвентаризации углеродных выбросов и методология расчета углеродного следа для Олимпиады Сочи-2014
Подход к инвентаризации углеродных выбросов и методология расчета углеродного следа для Олимпиады Сочи-2014 AZ CLUB 2019
AZ CLUB 2019 Модернизация и развитие участка волочения тугоплавких металлов и сплавов
Модернизация и развитие участка волочения тугоплавких металлов и сплавов Несуществующие животные
Несуществующие животные Выборы в государственную думу РФ 2021г
Выборы в государственную думу РФ 2021г Презентация на тему Организация деятельности по формированию смыслового чтения в образовательном процессе посредством элементо
Презентация на тему Организация деятельности по формированию смыслового чтения в образовательном процессе посредством элементо Древние образы и символы в народном искусстве.Часть 1
Древние образы и символы в народном искусстве.Часть 1 Презентация на тему Творчество Чайковского
Презентация на тему Творчество Чайковского  20170601_prezentatsiya_microsoft_powerpoint
20170601_prezentatsiya_microsoft_powerpoint ВПР общ за 7 кл много
ВПР общ за 7 кл много Летний пейзаж карандашами
Летний пейзаж карандашами Презентация на тему Растения – производители. («Окружающий мир» А.А.Вахрушев и др., 3 класс)
Презентация на тему Растения – производители. («Окружающий мир» А.А.Вахрушев и др., 3 класс) Правила отношений
Правила отношений Настройка экспозиции в фотоаппарате
Настройка экспозиции в фотоаппарате Сочинение по художественному тексту в формате ЕГЭ(на примере текста А.П. Владимирова «Косуля»)
Сочинение по художественному тексту в формате ЕГЭ(на примере текста А.П. Владимирова «Косуля») СредаПромышленной Разработки Программного Обеспечения
СредаПромышленной Разработки Программного Обеспечения ВЫДАЮЩИЕСЯ ЛЮДИ КАФЕДРЫ
ВЫДАЮЩИЕСЯ ЛЮДИ КАФЕДРЫ Электронная почта
Электронная почта