Содержание
- 2. Представление команд
- 3. Я - газ легчайший и бесцветный, Неядовитый и безвредный, Соединяясь с кислородом, Я для питья даю
- 4. Он всюду и везде: В камне, в воздухе, в воде; Он и в утреней росе, И
- 5. В минеральной воде я бурлю, В топочном газе летаю, Растениям пользу несу, Пожар затухать заставляю. Разминка
- 6. Чаще черный я по цвету, Быть могу прозрачным Мною пишут и рисуют, Бываю я и мрачным.
- 7. Химические понятия 1. Электролитическая диссоциация –это... . 2. Неэлектролиты- это … . 3. Электролиты – это
- 8. 1. Щелочи – это … . 2. Кислоты – это … . 3. Соли – это
- 9. 2. Можно ли назвать гидроксид хрома щелочью? 1. Можно ли назвать гидроксид бария щелочью? 2. Можно
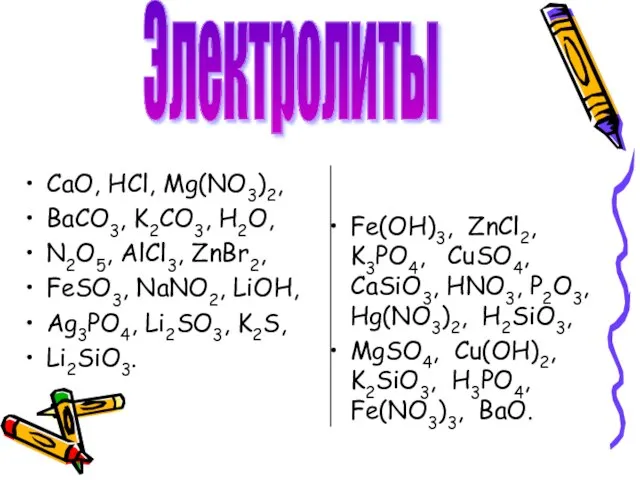
- 10. CaO, HCl, Mg(NO3)2, BaCO3, K2CO3, H2O, N2O5, AlCl3, ZnBr2, FeSO3, NaNO2, LiOH, Ag3PO4, Li2SO3, K2S, Li2SiO3.
- 11. Задания для капитанов у доски: 1. NaOH + H2SO4 = 2. Fe(OH)2 + HCL = 3.
- 12. Кроссворд на тему: «Окислительно-восстановительные реакции»
- 13. Решение задач Время выполнения работы 5 минут.
- 14. Ответы на задачи: Задача № 1 Задача № 2
- 16. Скачать презентацию












 Презентация на тему Политика и власть
Презентация на тему Политика и власть  6. СВН 2020
6. СВН 2020 The structure of the body
The structure of the body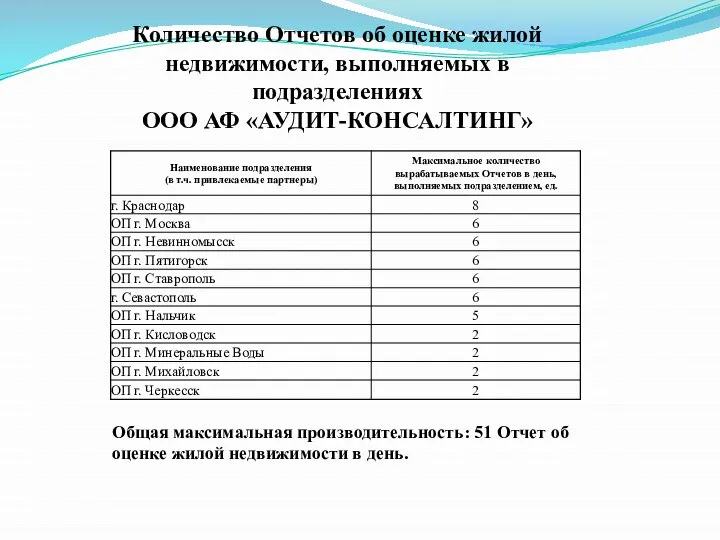 Количество Отчетов об оценке жилой недвижимости, выполняемых в подразделениях ООО АФ АУДИТ-КОНСАЛТИНГ
Количество Отчетов об оценке жилой недвижимости, выполняемых в подразделениях ООО АФ АУДИТ-КОНСАЛТИНГ УПРАВЛЕНЧЕСКИЙКОНСАЛТИНГ
УПРАВЛЕНЧЕСКИЙКОНСАЛТИНГ Презентация на тему орган зрения
Презентация на тему орган зрения Metodiki_yur_AKZS
Metodiki_yur_AKZS Пушкинская карта
Пушкинская карта Мой милый маг, моя Мария, - Мечтам мерцающий маяк. Мятежны марева морские, Мой милый маг, моя Мария, Молчаньем манит мутный мрак … Мне
Мой милый маг, моя Мария, - Мечтам мерцающий маяк. Мятежны марева морские, Мой милый маг, моя Мария, Молчаньем манит мутный мрак … Мне 3 года младший дошкольник
3 года младший дошкольник Правовая защита экологии в Беларуси
Правовая защита экологии в Беларуси Хирургическое_лечение_преждевременной_эякуляции
Хирургическое_лечение_преждевременной_эякуляции Столетие бедствий
Столетие бедствий Памятка по прямым выплатам ФСС
Памятка по прямым выплатам ФСС «Конституция –основной законгосударства»
«Конституция –основной законгосударства» Замечания заказчика
Замечания заказчика Презентация на тему Реализация ФГОС в работе школьной библиотеки. Воспитание культурного и гражданского самосознания учащихся.
Презентация на тему Реализация ФГОС в работе школьной библиотеки. Воспитание культурного и гражданского самосознания учащихся. Характерные особенности тактической подготовки баскетболистов при игре в защите
Характерные особенности тактической подготовки баскетболистов при игре в защите Презентация на тему Великий круговорот жизни 3 класс
Презентация на тему Великий круговорот жизни 3 класс (005)Pulser Test Form
(005)Pulser Test Form Культурные и сорные растения поля
Культурные и сорные растения поля Устное народное творчество Урала.
Устное народное творчество Урала. Презентация на тему Евглена Зеленая
Презентация на тему Евглена Зеленая  Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Землетрясения Подготовила презентацию студентка 1ого курса ЭФ Группы Э112Б Олефир Карина
Землетрясения Подготовила презентацию студентка 1ого курса ЭФ Группы Э112Б Олефир Карина Apģērbs. Apģērba materiāli
Apģērbs. Apģērba materiāli Евгений Гришковец
Евгений Гришковец Вахта памяти в канун 74-й годовщины великой победы
Вахта памяти в канун 74-й годовщины великой победы