Содержание
- 2. Характеристика элементов I-Б группы Электронная формула этих элементов: (n-1)d9nS2 Для стабилизации наблюдается «провал» электрона и электронная
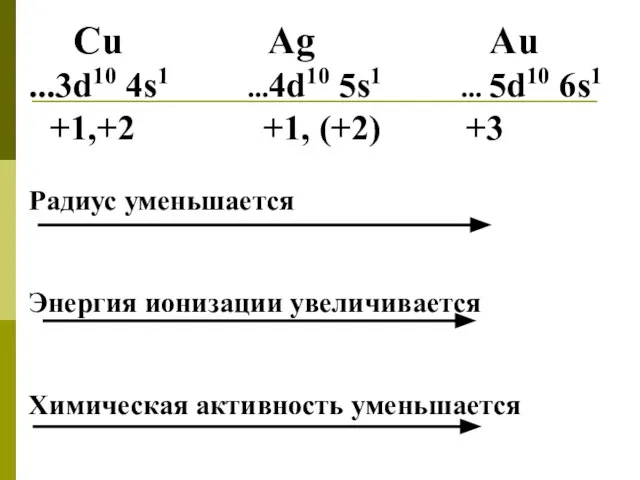
- 3. Cu Ag Au ...3d10 4s1 ...4d10 5s1 ... 5d10 6s1 +1,+2 +1, (+2) +3 Радиус уменьшается
- 4. ХИМИЧЕСКИЕ СВОЙСТВА CuCI + 2NH3 = [Cu(NH3)2]CI Au(OH)+NaOH→ Na[Au(OH)4]
- 5. Cu, Ag, Au – малоактивные металлы, стоят в ряду напряжения после водорода Cu, Ag – взаимодействуют
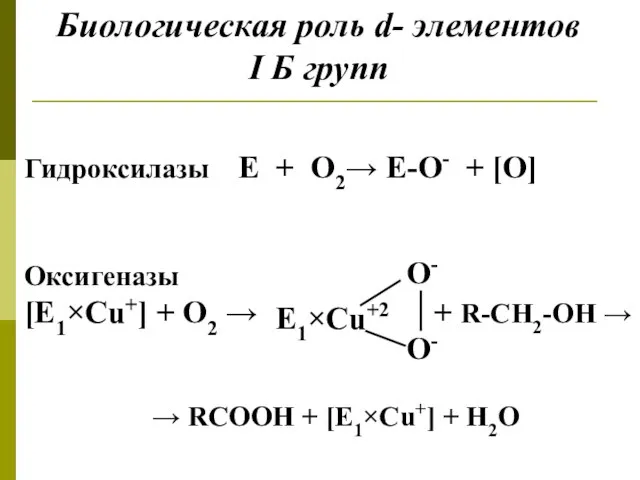
- 6. Биологическая роль d- элементов I Б групп Гидроксилазы Е + О2→ Е-О- + [O] Оксигеназы [E1×Cu+]
- 7. Биологическая роль d-элементов I-Б группы СОД (супероксиддисмутаза) [СОД×Сu2+]+ О2- → [СОД×Cu+] + O2 [СОД×Сu+]+O2- +2H+→[СОД×Сu+2] +H2O2
- 8. Биологическая роль d-элементов I-Б группы O2+4e-+4H+ Fe+2 + [ЦП×Сu+2] → Fe+3 + [ЦП×Cu+] → 2H2O ЦП
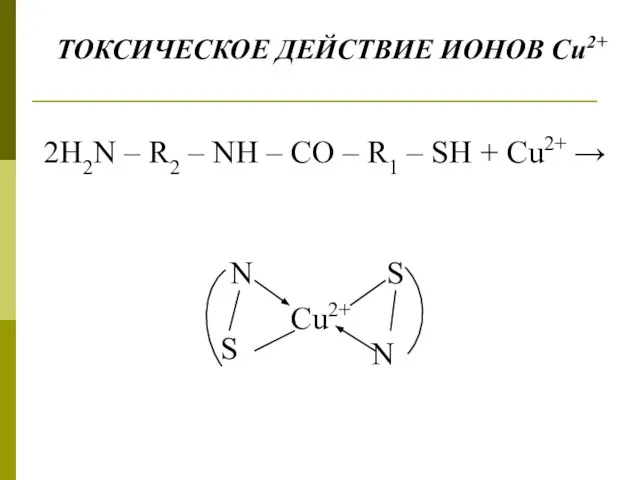
- 9. 2Н2N – R2 – NH – CO – R1 – SH + Cu2+ → ТОКСИЧЕСКОЕ ДЕЙСТВИЕ
- 10. Электронное строение элементов II-Б группы (n-1)d10 nS2
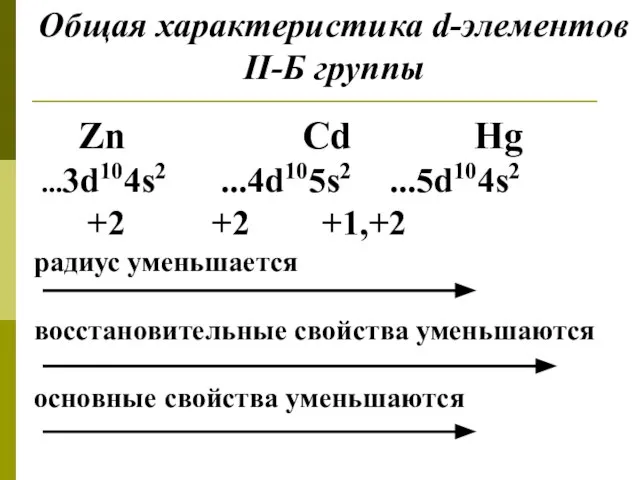
- 11. Общая характеристика d-элементов II-Б группы Zn Cd Hg ...3d104s2 ...4d105s2 ...5d104s2 +2 +2 +1,+2 радиус уменьшается
- 12. ХИМИЧЕСКИЕ СВОЙСТВА ZnO + 2HCI +3H2O = [Zn(H2O)4]CI2 ZnO + 2NaOH + H2O = Na2[Zn(OH)4] Cd(OH)2
- 13. Из солей ртути известны: Hg2Cl2 – каломель ( практически не растворима в воде) Hg+2Cl2 – сулема
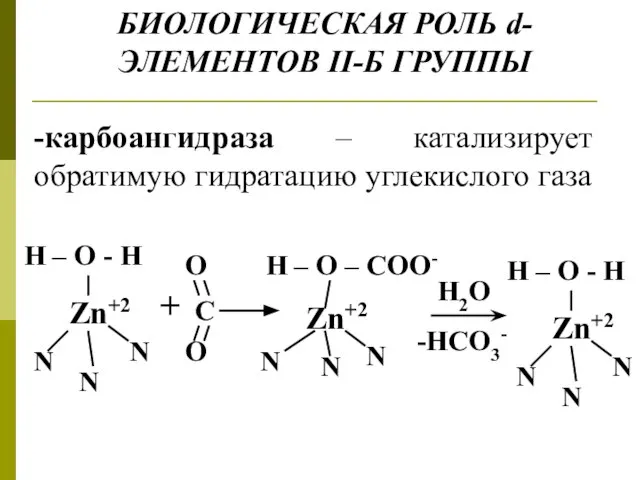
- 14. БИОЛОГИЧЕСКАЯ РОЛЬ d-ЭЛЕМЕНТОВ II-Б ГРУППЫ H2O -HCO3- -карбоангидраза – катализирует обратимую гидратацию углекислого газа
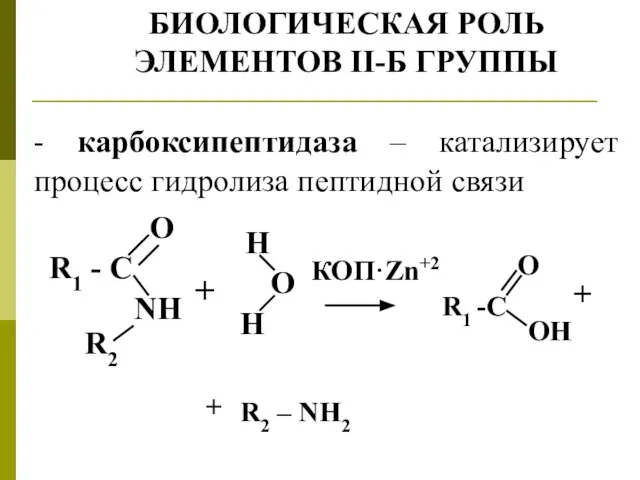
- 15. БИОЛОГИЧЕСКАЯ РОЛЬ ЭЛЕМЕНТОВ II-Б ГРУППЫ - карбоксипептидаза – катализирует процесс гидролиза пептидной связи + КОП·Zn+2 O
- 16. ОБЩАЯ ХАРАКТЕРИСТИКА d-ЭЛЕМЕНТОВ VI- Б ГРУППЫ (n – 1) danSb, где а = от 1 до
- 17. ОБЩАЯ ХАРАКТЕРИСТИКА d-ЭЛЕМЕНТОВ VI- Б ГРУППЫ Cr Mo W ̣̣̣̣̣̣̣̣̣̣̣̣̣̣ ̣̣...3d54s1 ...4d55s1 ...5d46s2 +2,+3,+6 +6 +6
- 18. Свойства соединений элементов VI-Б группы В низшей степени окисления – основные и восстановительные свойства – Cr+2O,
- 19. Свойства соединений VI –Б группы В промежуточой степени окисления –амфотерные свойства - Cr2O3 Cr(OH)3 – гидроксид
- 20. В высшей степени окисления – кислотные и окислительные свойства - CrO3 Свойства соединений VI –Б группы
- 21. БИОЛОГИЧЕСКАЯ РОЛЬ VI-Б ГРУППЫ R – COH + КОКС·Мо+6 +Н2О → →H3O ... OCR - КОКС·Мо+4
- 22. ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ VII –Б ГРУППЫ Mn Tc Re ...3d54s2 ...4d55s2 ...5d56s2 +2,+3,+4,+6,+7 +4,+7 Степень окисления Mn:
- 23. ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ VII-Б ГРУППЫ Степень окисления Mn: +4 MnO2, Mn(OH)4 H4MnO4- орто-марганцеватистая H2MnO3 – мета-марганцеватистая
- 24. ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ VII-Б ГРУППЫ Степень окисления : +6 MnO3 H2MnO4 –марганцовистая к-та К2MnO4- манганат калия соединения
- 25. ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ VII-Б ГРУППЫ Степень окисления : +7 Mn2O7 -оксид марганца (VII) HMnO4 –марганцовая к-та (соли
- 26. БИОЛОГИЧЕСКАЯ РОЛЬ МАРГАНЦА В организме находится в степени окисления Mn+2 1. Образует комплексы с нуклеиновыми кислотами
- 27. ПРИМЕНЕНИЕ СОЕДИНЕНИЙ МАРГАНЦА В МЕДИЦИНЕ KMnO4 – 5% дезинфицирующее средство, как кровоостанавливающее MnSO4 – при лечении
- 28. ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ VIII-Б ГРУППЫ Fe Co Ni ...3d64s2 ...3d74s2 ... 3d84s2 +2,+3,+6; +2,+3,+5; +2,+3,+4; В
- 29. ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ VIII-Б ГРУППЫ Степень окисления +3 Fe2O3, Co2O3, Ni2O3 Fe(OH)3 – амфотерное соединение Fe(OH)3
- 30. ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ VIII-Б ГРУППЫ Степень окисления : +6 FeO3 – оксид железа (VI) H2FeO4 –
- 31. Применение в медицине Железо восстановленное, при лечении анемии Ферамид [Fe(C6H5CONH2)2CI2] FeCI2 наружное –кровоостанавливающее и дезинфицирующее
- 33. Скачать презентацию

![ХИМИЧЕСКИЕ СВОЙСТВА CuCI + 2NH3 = [Cu(NH3)2]CI Au(OH)+NaOH→ Na[Au(OH)4]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/376521/slide-3.jpg)

![Биологическая роль d-элементов I-Б группы СОД (супероксиддисмутаза) [СОД×Сu2+]+ О2- → [СОД×Cu+] + O2 [СОД×Сu+]+O2- +2H+→[СОД×Сu+2] +H2O2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/376521/slide-6.jpg)
![Биологическая роль d-элементов I-Б группы O2+4e-+4H+ Fe+2 + [ЦП×Сu+2] → Fe+3 +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/376521/slide-7.jpg)

![ХИМИЧЕСКИЕ СВОЙСТВА ZnO + 2HCI +3H2O = [Zn(H2O)4]CI2 ZnO + 2NaOH +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/376521/slide-11.jpg)
















![Применение в медицине Железо восстановленное, при лечении анемии Ферамид [Fe(C6H5CONH2)2CI2] FeCI2 наружное –кровоостанавливающее и дезинфицирующее](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/376521/slide-30.jpg)
 Заболевания роговицы
Заболевания роговицы  Презентация на тему Международное сотрудничество в сфере уголовного судопроизводства
Презентация на тему Международное сотрудничество в сфере уголовного судопроизводства Духовное и физическое состояние молодёжи в Нерюнгринском районе
Духовное и физическое состояние молодёжи в Нерюнгринском районе Здоровый образ жизни: творчество и долголетие
Здоровый образ жизни: творчество и долголетие Оқы, еске түсір, айт
Оқы, еске түсір, айт Презентация на тему Королевство Норвегия
Презентация на тему Королевство Норвегия Презентация на тему Юганский заповедник
Презентация на тему Юганский заповедник Развивайка Природа
Развивайка Природа Влияние мультфильмов на психику детей
Влияние мультфильмов на психику детей Интерференция света в тонких пленках
Интерференция света в тонких пленках Презентация на тему Как человек использует свойства воды
Презентация на тему Как человек использует свойства воды  Святки. Традиции
Святки. Традиции Деление клетки.Митоз.Амитоз.Мейоз
Деление клетки.Митоз.Амитоз.Мейоз ПРАВИТЕЛЬСТВО САНКТ-ПЕТЕРБУРГАЖИЛИЩНЫЙ КОМИТЕТСанкт-Петербургское государственное учреждение «ГОРЖИЛОБМЕН»
ПРАВИТЕЛЬСТВО САНКТ-ПЕТЕРБУРГАЖИЛИЩНЫЙ КОМИТЕТСанкт-Петербургское государственное учреждение «ГОРЖИЛОБМЕН» Структура форм, пластика тела объекта. Фактура, текстура. Базовые упражнения
Структура форм, пластика тела объекта. Фактура, текстура. Базовые упражнения Структура компьютера и принципы его функционирования
Структура компьютера и принципы его функционирования PPF ЗВЕЗДОЧКА
PPF ЗВЕЗДОЧКА Ольга Парфенова - свадебный церемониймейстер
Ольга Парфенова - свадебный церемониймейстер Виды изобразительного искусства: живопись, графика, скульптура. 2 класс
Виды изобразительного искусства: живопись, графика, скульптура. 2 класс Одно решение для всех платежей или как еще получить деньги от клиента
Одно решение для всех платежей или как еще получить деньги от клиента Твой новый взгляд на свободу
Твой новый взгляд на свободу В районе Ясенево ведётся капитальный ремонт 4-х спортивных площадок по адресам: Вильнюсская ул., 17, Голубинская ул., 7-5, Литовский б-р.
В районе Ясенево ведётся капитальный ремонт 4-х спортивных площадок по адресам: Вильнюсская ул., 17, Голубинская ул., 7-5, Литовский б-р. ФИЗИКА – 9 класс
ФИЗИКА – 9 класс Строение и функции нервной системы
Строение и функции нервной системы  Презентация на тему БАКТЕРИИ
Презентация на тему БАКТЕРИИ  Выборочный контроль товаров на основе управления рисками Боб Олсон Консультант по таможенным вопросам Подготовлено Робертом Х
Выборочный контроль товаров на основе управления рисками Боб Олсон Консультант по таможенным вопросам Подготовлено Робертом Х Подвижные игры на уроке физической культуры
Подвижные игры на уроке физической культуры Система образов романа «Евгений Онегин»
Система образов романа «Евгений Онегин»