Содержание
- 2. Жизнь – это способ существования белковых тел. Ф.Энгельс
- 3. Белки – высокомолекулярные природные соединения (биополимеры), состоящие из остатков аминокислот, которые соединены пептидной связью. Белки Протеины
- 4. В состав белковых веществ входят: углерод, водород, кислород, азот, сера, фосфор. Гемоглобин – C3032H4816O872N780S8Fe4. Молекулярная масса
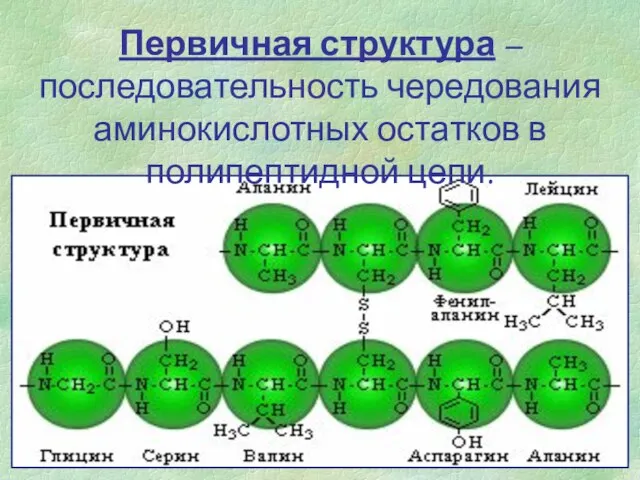
- 5. Первичная структура – последовательность чередования аминокислотных остатков в полипептидной цепи.
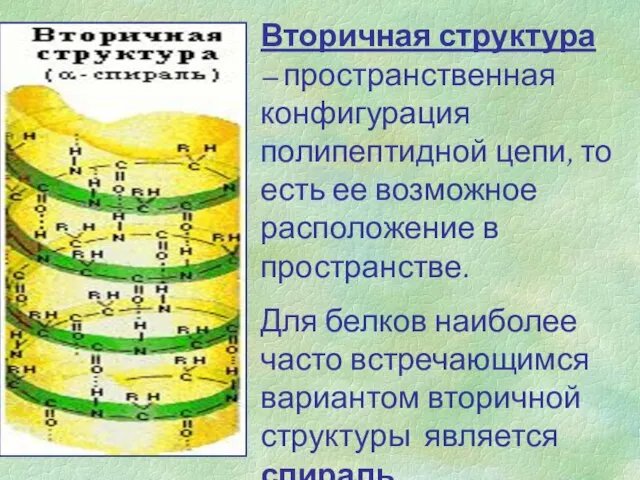
- 6. Вторичная структура – пространственная конфигурация полипептидной цепи, то есть ее возможное расположение в пространстве. Для белков
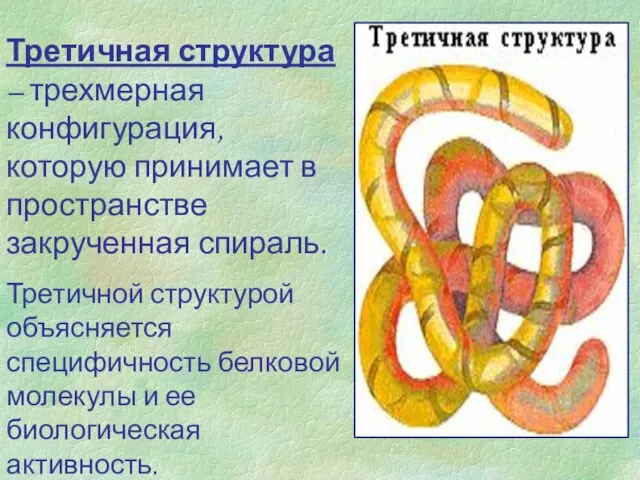
- 7. Третичная структура – трехмерная конфигурация, которую принимает в пространстве закрученная спираль. Третичной структурой объясняется специфичность белковой
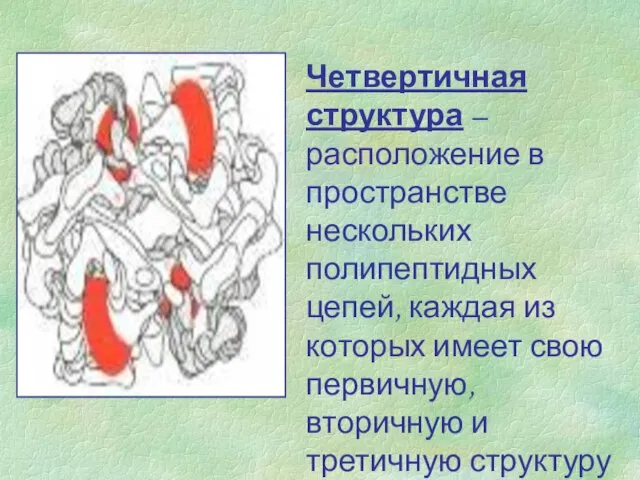
- 8. Четвертичная структура – расположение в пространстве нескольких полипептидных цепей, каждая из которых имеет свою первичную, вторичную
- 9. Химические свойства белков 1. Гидролиз (кислотно-основный, ферментативный), в результате которого образуются аминокислоты. 2. Денатурация – нарушение
- 10. Цветные реакции на белки 1. Ксантопротеиновая – взаимодействие с концентрированной азотной кислотой, которое сопровождается появлением желтой
- 12. Скачать презентацию




 Формы бактерий
Формы бактерий Центральный отдел слухового анализатора. Физиология слухового анализатора
Центральный отдел слухового анализатора. Физиология слухового анализатора Сказочный овощ тыква
Сказочный овощ тыква Земноводные или амфибии
Земноводные или амфибии Механизм нейрогуморальной регуляции на примере регуляции вдоха и выдоха. Сравнение нервной и гуморальной регуляции._Презента
Механизм нейрогуморальной регуляции на примере регуляции вдоха и выдоха. Сравнение нервной и гуморальной регуляции._Презента Двумембранные органоиды
Двумембранные органоиды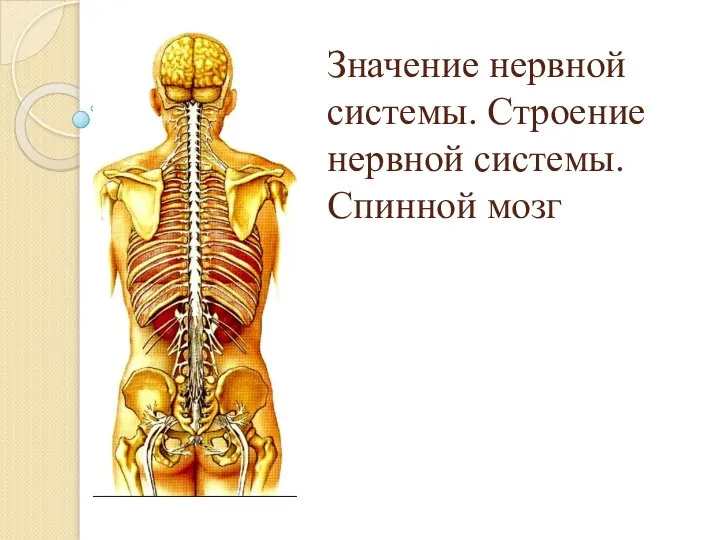 Значение нервной системы. Строение нервной системы. Спинной мозг
Значение нервной системы. Строение нервной системы. Спинной мозг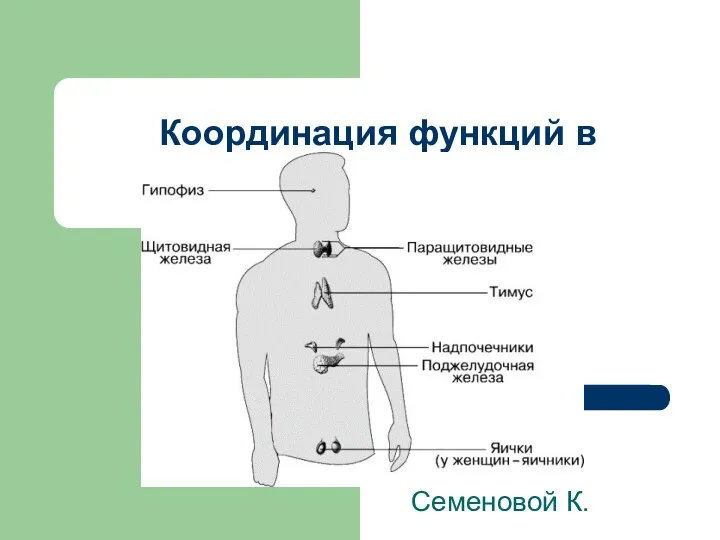 Координация функций в организме
Координация функций в организме Класс Пресмыкающиеся (Рептилии)
Класс Пресмыкающиеся (Рептилии) Генетика
Генетика Энергетический обмен (диссимиляция, катаболизм)
Энергетический обмен (диссимиляция, катаболизм) Зайцеподібні. Чим відрізняється заєць від кролика
Зайцеподібні. Чим відрізняється заєць від кролика 9 6 хим состав
9 6 хим состав Ферменты и их роль в организме человека. 8 класс
Ферменты и их роль в организме человека. 8 класс Антуриум - самый многочисленный род семейства Ароидных (Araceae)
Антуриум - самый многочисленный род семейства Ароидных (Araceae) Моногибридное скрещивание. Решение задач по генетике
Моногибридное скрещивание. Решение задач по генетике Плоские, круглые, кольчатые черви
Плоские, круглые, кольчатые черви Многообразие и экология грибов
Многообразие и экология грибов Збережемо першоцвіти!
Збережемо першоцвіти! Презентация на тему Отряд Аистообразные
Презентация на тему Отряд Аистообразные  Место человека в системе органического мира
Место человека в системе органического мира Презентация на тему Чарльз Дарвин и эволюционное учение
Презентация на тему Чарльз Дарвин и эволюционное учение  Лишайники Мурманской области
Лишайники Мурманской области Биологические функции и химический состав нуклеиновых кислот. Структура и уровни организации ДНК. Правило Чаргаффа
Биологические функции и химический состав нуклеиновых кислот. Структура и уровни организации ДНК. Правило Чаргаффа Валеология. Центральная проблема валеологии
Валеология. Центральная проблема валеологии Ядовитые растения
Ядовитые растения Закономерности роста и развития организма
Закономерности роста и развития организма Головной мозг: строение и функции. Часть №2
Головной мозг: строение и функции. Часть №2