Слайд 2ОБЩИЕ ПРЕДСТАВЛЕНИЯ О ФЕРМЕНТАХ
Ферменты, или энзимы, – это биологические катализаторы, ускоряющие химические

реакции.
Общее число известных ферментов составляет несколько тысяч.
Практически все химические реакции, протекающие в живых организмах, осуществляются при их участии.
Слайд 3Ферменты ускоряют химические реакции в 108 – 1020 раз.
Слово фермент произошло

от латинского fermentum – закваска, энзим в переводе с греческого означает «в дрожжах».
В 1926 году Джеймс Самнер впервые получил очищенный фермент в кристаллическом виде – уреазу:
Слайд 4
Большинство ферментов по своей природе являются белками.
У некоторых РНК обнаружена способность

осуществлять катализ; такие РНК получили название рибозимов, или РНК-ферментов.
Слайд 5Ферменты имеют ряд общих свойств с химическими небелковыми катализаторами:
не расходуются в

процессе катализа и не претерпевают необратимых изменений;
ускоряют как прямую, так и обратную реакции, не смещая при этом химического равновесия;
катализируют только те реакции, которые могут протекать и без них;
повышают скорость химической реакции за счет снижения энергии активации
Слайд 7
Ферменты от химических катализаторов отличаются по ряду параметров:
ферменты обладают более высокой

эффективностью действия;
ферменты обладают более высокой специфичностью в сравнении с небелковыми катализаторами, они ускоряют более узкий круг химических реакций;
Слайд 8
ферменты эффективно действуют в мягких условиях: при температуре 0 – 40 оС,

при атмосферном давлении, при значениях рН, близких к нейтральным, в более жестких условиях ферменты денатурируют и не проявляют своих каталитических качеств;
активность ферментов регулируется активаторами и ингибиторами.
Слайд 9Структура ферментов
Относительная молекулярная масса ферментов может колебаться от 104 до 106 и

более.
Ферменты – это, как правило, глобулярные белки.
Одни ферменты являются простыми белками - состоят только из аминокислотных остатков (рибонуклеаза, пепсин, трипсин),
активность других зависит от дополнительных химических компонентов - кофакторов.
Слайд 10В качестве кофакторов могут выступать ионы металлов Fe2+, Mn2+, Mg2+, Zn2+
или
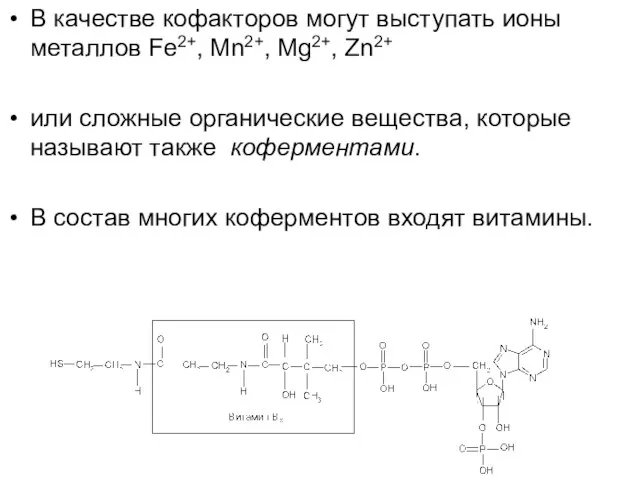
сложные органические вещества, которые называют также коферментами.
В состав многих коферментов входят витамины.
Слайд 11Если кофермент прочно связанный с ферментом называется простетической группой сложного белка.
Кофактор

легко диссоциируюет из комплекса с ферментом.
Кофакторы могут выполнять следующие функции:
участие в катализе;
осуществление взаимодействия между субстратом и ферментом;
стабилизация фермента.
Слайд 12
Каталитически активный комплекс фермент – кофактор называют холоферментом.
Отделение кофактора от холофермента

приводит к образованию неактивного апофермента:
Холофермент ↔ апофермент + кофактор.
Слайд 13В молекуле фермента присутствует активный центр.
Активный центр – это область молекулы

фермента, в которой происходит связывание субстрата и его превращение в продукт реакции.
В активном центре выделяют два участка:
якорный (контактный, связывающий) – отвечает за связывание и ориентацию субстрата в активном центре,
каталитический – непосредственно отвечает за осуществление реакции.
Слайд 14
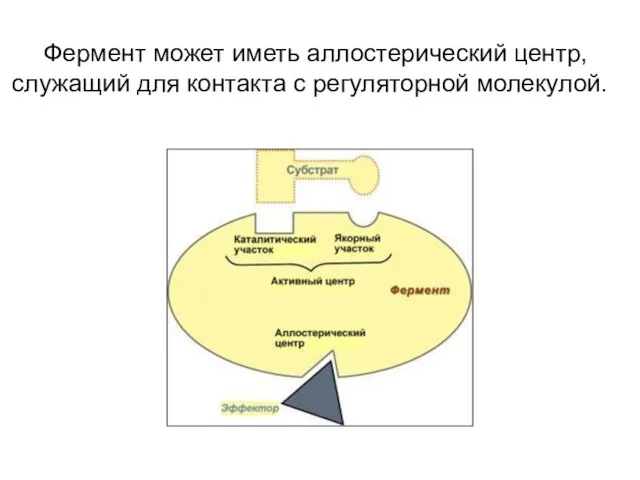
Фермент может иметь аллостерический центр, служащий для контакта с регуляторной молекулой.
Слайд 15
Активный центр образуют аминокислотные остатки полипептидной цепи.
В состав активного центра может

входить и небелковый компонент.
Наиболее часто в составе активного центра содержатся полярные (серин, треонин, цистеин) и заряженные (лизин, гистидин, глутаминовая и аспарагиновая кислоты) аминокислотные остатки.
Слайд 16Аминокислотные остатки, образующие активный центр, в полипептидной цепи находятся на значительном расстоянии
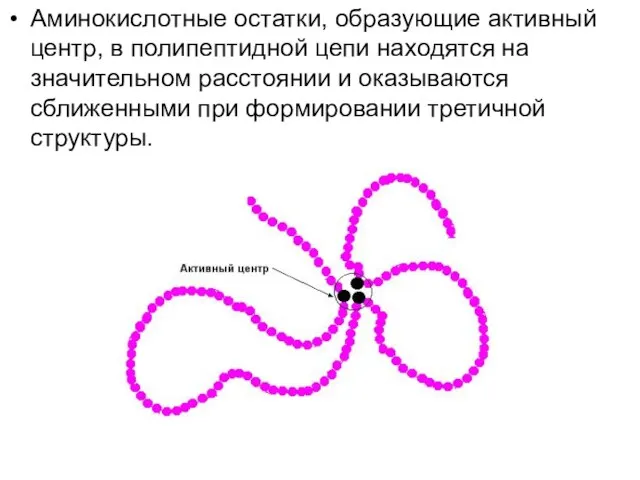
и оказываются сближенными при формировании третичной структуры.
Слайд 17
Некоторые ферменты синтезируются в неактивной форме в виде проферментов, которые затем под

действием определенных факторов активируются.
Например, пищеварительные ферменты химотрипсин и трипсин образуются в результате активации химотрипсиногена и трипсиногена.
Слайд 18Изоферменты – это группа ферментов, выполняющих идентичную каталитическую функцию у представителей одного

биологического вида, но отличающихся по структуре и физико-химическим свойствам (генетически детерминированы).
Множественные формы ферментов – это группа ферментов, выполняющих идентичную каталитическую функцию у представителей одного биологического вида, образовавшиеся в результате различных посттрансляционных модификаций.
Слайд 19Номенклатура и классификация ферментов
Тривиальная номенклатура.
Например,
пепсин (от греч. “пепсис” – “пищеварение”),

трипсин (от греч. “трипсис” – “разжижаю”),
папаин (от названия дынного дерева Carica papaja).
Слайд 20Рациональная номенклатура.
Название фермента составляется из названия субстрата и характерного окончания “-аза”.

Например,
амилаза - катализирует гидролиз крахмала (от греч. “амилон” – “крахмал”),
липаза - гидролиз липидов (от греч. “липос” – “жир”),
уреаза – гидролиз мочевины (от греч. “уреа” – “мочевина”) и т.д.
Слайд 21
Существуют и систематические названия ферментов, включающие названия субстратов и отражающие характер катализируемой

реакции:
АТФ + D-глюкоза ↔ АДФ + D-глюкоза – 6 – фосфат,
АТФ: гексоза 6-фосфотрансфераза.
Слайд 22В соответствии с катализируемой реакцией все ферменты делятся на 6 классов.
Оксидоредуктазы.
Катализируют

окислительно-восстановительные реакции
Трансферазы.
Катализируют реакции межмолекулярного переноса групп: АB + C = AC + B.
Гидролазы.
Катализируют реакции гидролиза:
АВ + Н2О = АОН + ВН.
Слайд 23Лиазы.
Катализируют реакции присоединения групп по двойным связям и обратные реакции.
Изомеразы.
Катализируют

реакции изомеризации (внутримолекулярный перенос групп).
Лигазы.
Катализируют реакции синтеза, сопряженные с распадом макроэргов (АТФ).
Слайд 24В свою очередь каждый класс подразделяют
на подклассы,
подклассы – на подподклассы.

Ферментам, образующим подподклассы, присваивается порядковый номер.
В итоге фермент имеет свой четырехзначный номер:
КФ 2.7.1.1. означает:
класс 2 – трансферазы;
подкласс 7 – перенос фосфата;
подподкласс 1 – алкогольная группа – акцептор фосфата. Название – гексокиназа, или АТФ:D-гексоза-6-фосфотрансфераза.
Слайд 25МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ
Последовательность стадий катализа:
Взаимодействие субстрата с ферментом в активном центре.
Химическое превращение

субстрата в продукт реакции.
Освобождение продукта реакции из активного центра фермента.
Слайд 26Взаимодействие фермента Е с субстратом S приводит к образованию промежуточного фермент-субстратного комплексаES.

При взаимодействии фермента с субстратом, реагирующие вещества сближаются и удерживаются в таком положении, чтобы реакционноспособные группы могли провзаимодействовать;
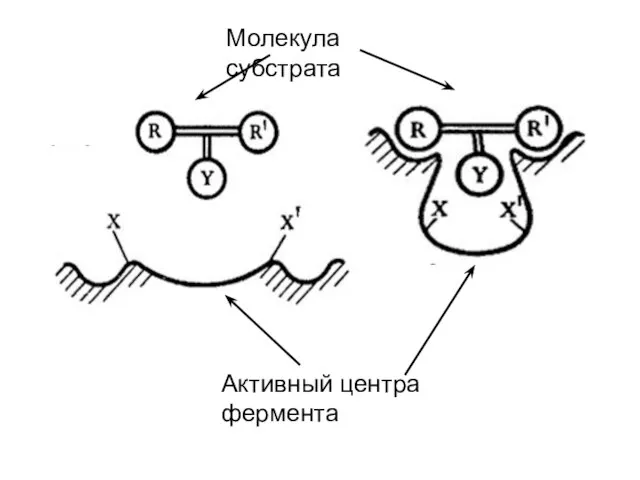
Слайд 27Модель жесткой матрицы Э. Фишера (1894) (модель «ключ-замок») основана на теории существования
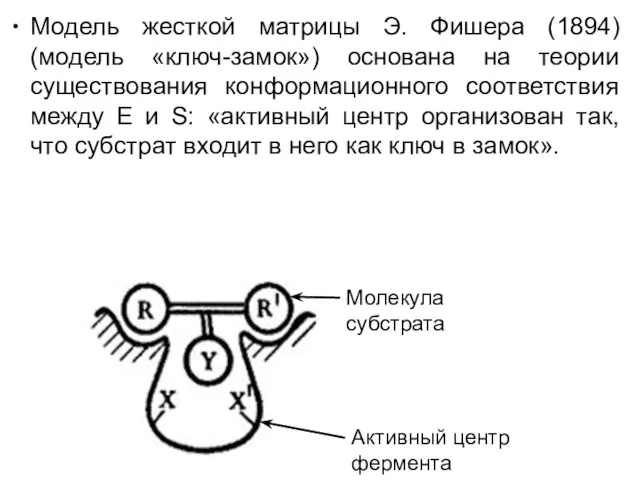
конформационного соответствия между Е и S: «активный центр организован так, что субстрат входит в него как ключ в замок».
Слайд 28Модель и теория индуцированного конформационного соответствия
между Е и S Д. Кошланда

(1958)
(модель «рука-перчатка»).
Взаимодействие субстрата с ферментом вызывает конформационные изменения в молекуле фермента: функциональные группы принимают ориентацию, необходимую для связывания субстрата и катализа.
Слайд 30
В катализе принимают участие:
функциональные группы, которые могут быть донорами или акцепторами Н+

(кислотами и основаниями);
группы, которые могут участвовать в образовании ковалентных связей с молекулами субстрата.
Слайд 31
КИНЕТИКА ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
Кинетика ферментативных реакций – наука о скоростях ферментативных реакций, их

зависимости от различных факторов.
Скорость ферментативной реакции:
v = Δс / t .
Скорость ферментативной реакции зависит от природы фермента, которая определяет его активность.
Слайд 32Способы выражения ферментативной активности:
Единица активности фермента – количество фермента, которое в стандартных

условиях катализирует превращение 1 мкмоль субстрата в 1 мин (1 МЕ = 1 мкмоль/мин).
1 КАТАЛ – количество фермента, способное в течение 1 с обеспечить превращение 1 моль субстрата в стандартных условиях.
1 КАТАЛ = 6 · 107 МЕ.
Слайд 33Удельная активность – число единиц ферментативной активности, приходящееся на 1 мг белка

(1 мкмоль/мин·мг белка).
Активность каталитического центра – число молекул субстрата, которые претерпевают превращение за 1 мин в расчете на 1 каталитический центр.
Число оборотов фермента – число молекул субстрата, претерпевающих превращение за 1 мин в расчете на 1 активный центр или 1 активную молекулу фермента.
Слайд 34
В процессе ферментативной реакции фермент (Е) взаимодействует с субстратом (S) с образованием

фермент-субстратный комплекс, который затем распадается с высвобождением фермента и продукта (Р) реакции:
E + S ←→ ES → E + P.
Скорость ферментативной реакции зависит от концентрации субстрата и фермента, температуры, рН среды, наличия различных регуляторных веществ.
Слайд 35Влияние концентрации субстрата на скорость ферментативной реакции
(Уравнение Михаэлиса-Ментен)
При низких концентрациях субстрата
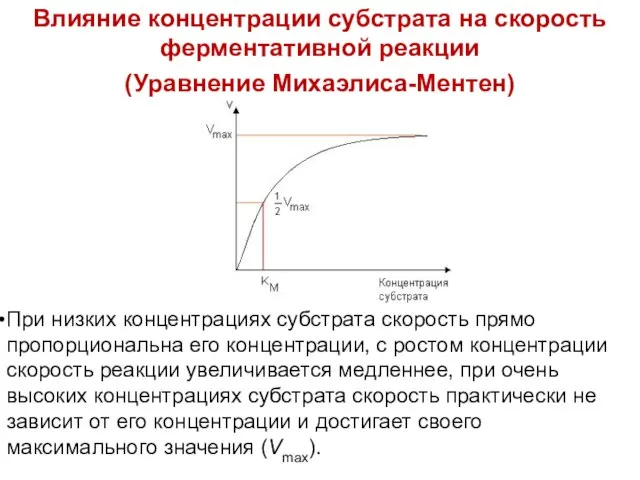
скорость прямо пропорциональна его концентрации, с ростом концентрации скорость реакции увеличивается медленнее, при очень высоких концентрациях субстрата скорость практически не зависит от его концентрации и достигает своего максимального значения (Vmax).
Слайд 36
При высоких концентрациях субстрата все молекулы фермента находятся в составе фермент-субстратного комплекса,

и достигается полное насыщение активных центров фермента, именно поэтому скорость реакции практически не зависит от концентрации субстрата.
Слайд 37График зависимости активности фермента от концентрации субстрата описывается уравнением Михаэлиса – Ментен,

которое получило название в честь выдающихся ученых Л.Михаэлиса и М.Ментен:
Vmax [S]
v = ___________,
KM + [S]
где v – скорость ферментативной реакции; [S] – концентрация субстрата; KM – константа Михаэлиса.
Слайд 38
Физический смысл константы Михаэлиса:
При условии, что v = ½ Vmax, получаем

KM = [S].
Константа Михаэлиса равна концентрации субстрата, при которой скорость реакции равна половине максимальной.
Слайд 39Зависимость скорости реакции
от концентрации субстрата
в двойных обратных
координатах (уравнение
Лайнуивера-Бэрка)
Определение
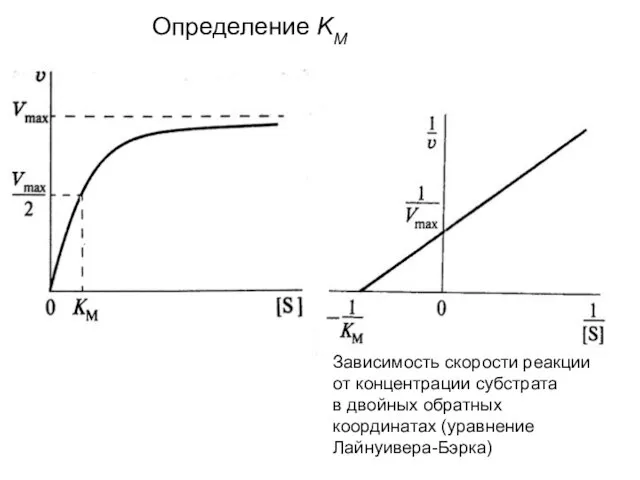
KM
Слайд 40Зависимость скорости реакции от концентрации фермента
Зависимость скорости реакции от концентрации фермента является
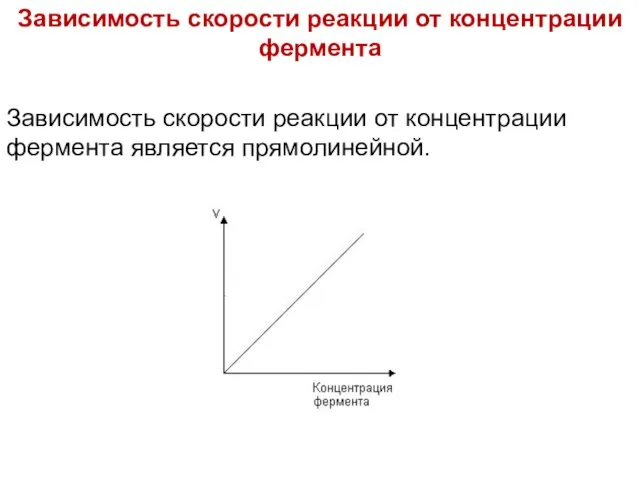
прямолинейной.
Слайд 41
Не прямолинейная зависимость
- при высоких концентрациях фермента наблюдается вследствие нехватки субстрата

или агрегации молекул фермента и др.,
- при небольших концентрациях фермента может быть результатом присутствия в инкубационной среде токсических примесей, связывающихся с ферментом и инактивирующих его.
Слайд 42Зависимость скорости ферментативной реакции от температуры
Зависимость скорости ферментативной реакции от температуры представлена
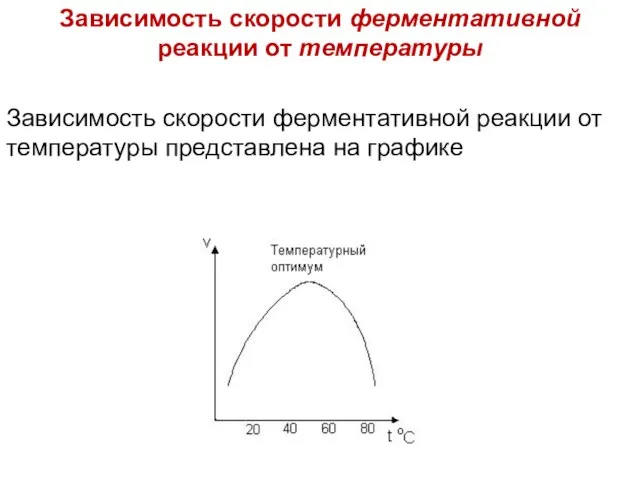
на графике
Слайд 43При низких температурах (приблизительно до 40 – 50 оС) повышение температуры на

каждые 10 оС в соответствии с правилом Вант-Гоффа сопровождается увеличением скорости химической реакции в 2 – 4 раза.
При высоких температурах более 55 – 60 оС активность фермента резко снижается из-за его тепловой денатурации.
Максимальная активность ферментов наблюдается обычно в пределах 40 – 60 оС.
Слайд 44
Температура, при которой активность фермента максимальна, называется температурным оптимумом.
Температурный оптимум ферментов

термофильных микроорганизмов находится в области более высоких температур.
Слайд 45Зависимость скорости ферментативной реакции от рН
График зависимости от рН имеет колоколообразную форму
Значение
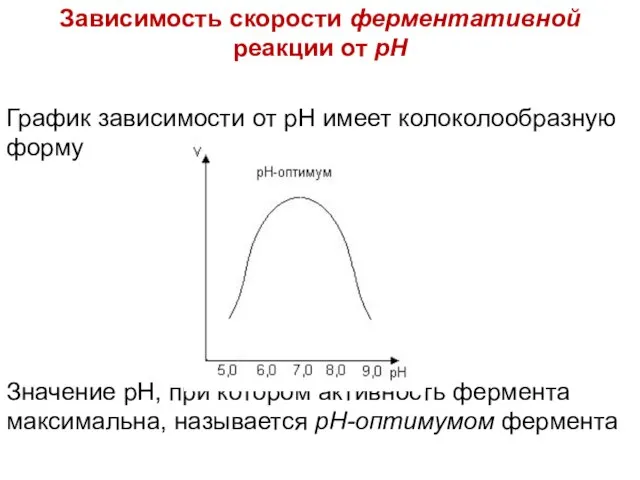
рН, при котором активность фермента максимальна, называется рН-оптимумом фермента
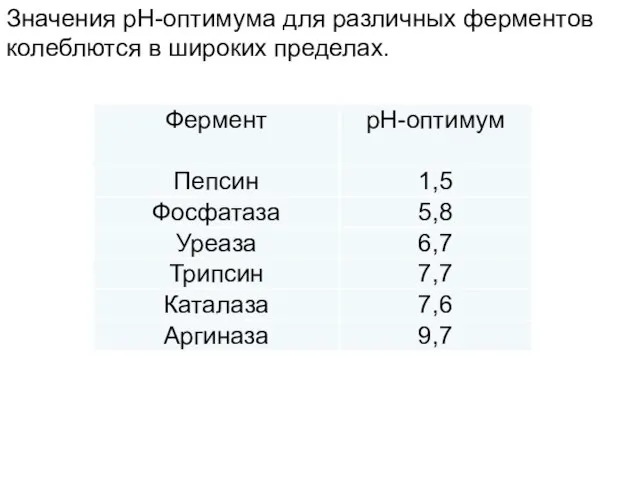
Слайд 46Значения рН-оптимума для различных ферментов колеблются в широких пределах.
Слайд 47Характер зависимости ферментативной реакции от рН определяется тем, что этот показатель оказывает

влияние на:
ионизацию аминокислотных остатков, участвующих в катализе,
ионизацию субстрата,
конформацию фермента и его активного центра.
Слайд 48Ингибирование ферментов
Скорость ферментативной реакции может быть снижена при участиии ингибиторов.
Ингибитор –

вещество, специфически уменьшающее скорость ферментативной реакции.
Различают ингибиторы:
связывающиеся с апоферментом,
образующие комплекс с субстратом,
связывающие кофермент,
связывающие активатор,
взаимодействующие с фермент-субстратными комплексами.
Слайд 49
Ингибиторы можно разделить на два основных типа: необратимые и обратимые.
Необратимые ингибиторы

(I) связываются с ферментом с образованием комплекса, диссоциация которого с восстановлением активности фермента невозможна:
E + I → EI.
Слайд 50
Примером необратимого ингибитора является диизопропилфторфосфат (ДФФ). ДФФ ингибирует фермент ацетилхолинэстеразу, играющего важную

роль в передаче нервного импульса. Этот ингибитор взаимодействует с серином активного центра фермента, блокируя тем самым активность последнего. Вследствие этого нарушается способность отростков нервных клеток нейронов проводить нервный импульс. ДФФ является одним из первых веществ нервно-паралитического действия. На его основе создан ряд относительно нетоксичных для человека и животных инсектицидов - веществ, ядовитых для насекомых.
Слайд 51
Обратимые ингибиторы при определенных условиях могут быть легко отделены от фермента.
Активность

последнего при этом восстанавливается:
E + I ←→ EI.
Обратимое ингибирование активности фермента подразделяется на: конкурентное, неконкурентное, бесконкурентное и смешанное.
Слайд 52Типы ингибирования
Конкурентное ингибирование.
Конкурентный ингибитор, являясь структурным аналогом субстрата, взаимодействует с активным центром

фермента и таким образом перекрывает доступ субстрата к ферменту.
При этом ингибитор не подвергается химическим превращениям и связывается с ферментом обратимо.
После диссоциации комплекса EI фермент может связаться либо с субстратом и преобразовать его, либо с ингибитором.
Поскольку и субстрат и ингибитор конкурируют за место в активном центре, такое ингибирование называется конкурентным.
Слайд 53
Конкурентные ингибиторы используются в медицине. Для борьбы с инфекционными болезнями ранее широко
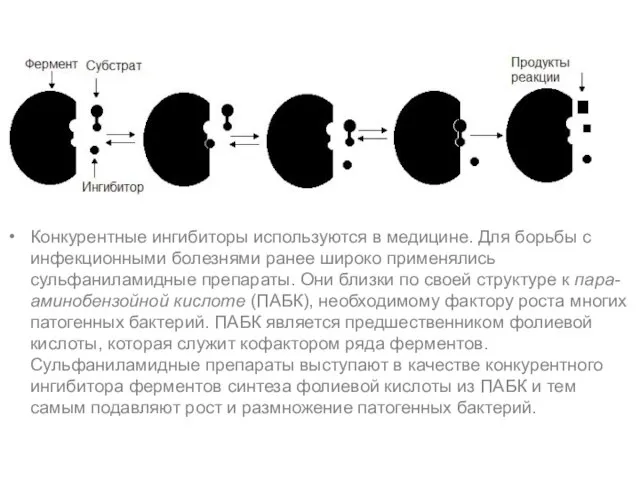
применялись сульфаниламидные препараты. Они близки по своей структуре к пара-аминобензойной кислоте (ПАБК), необходимому фактору роста многих патогенных бактерий. ПАБК является предшественником фолиевой кислоты, которая служит кофактором ряда ферментов. Сульфаниламидные препараты выступают в качестве конкурентного ингибитора ферментов синтеза фолиевой кислоты из ПАБК и тем самым подавляют рост и размножение патогенных бактерий.
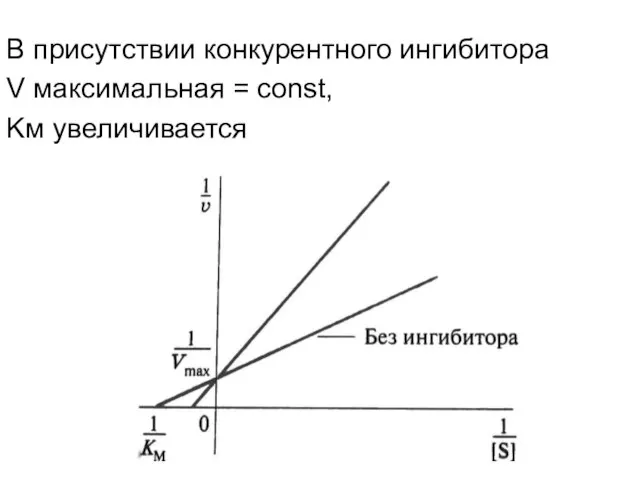
Слайд 54В присутствии конкурентного ингибитора
V максимальная = const,
Kм увеличивается
Слайд 55Неконкурентное ингибирование
Неконкурентные ингибиторы по структуре не сходны с субстратом и при образовании

EI взаимодействуют не с активным центром, а с другим участком фермента.
Взаимодействие ингибитора с ферментом приводит к изменению структуры последнего.
Образование EI-комплекса является обратимым, поэтому после его распада фермент вновь способен атаковать субстрат
Слайд 56
В качестве неконкурентного ингибитора может выступать цианид CN-. Он связывается с ионами
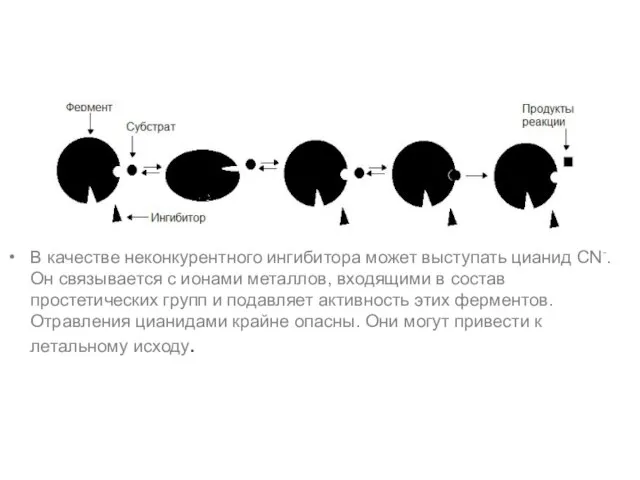
металлов, входящими в состав простетических групп и подавляет активность этих ферментов. Отравления цианидами крайне опасны. Они могут привести к летальному исходу.
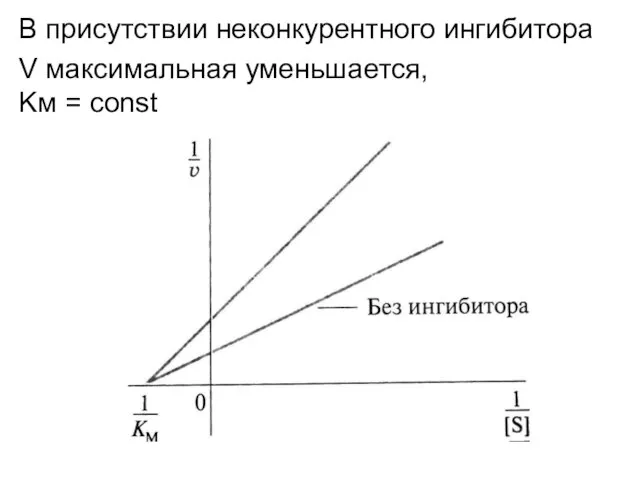
Слайд 57В присутствии неконкурентного ингибитора
V максимальная уменьшается,
Kм = const
Слайд 58
Бесконкурентное ингибирование
Ингибитор обратимо взаимодействует с ферментом только после образования фермент-субстратного комплекса.
Образующийся в

этом случае тройной комплекс фермент-субстрат-ингибитор не подвергается дальнейшему превращению.
Слайд 59Смешанное ингибирование
сочетает в себе конкурентное и неконкурентное торможение.
Ингибитор, присоединяется в

активном центре фермента, изменяет сродство фермента к субстрату и каталитическую активность фермента.
Слайд 60Регуляция каталитической активности ферментов
Регуляция путём посттрансляционной ковалентной модификации молекулы фермента (ограниченный протеолиз,

фосфорилирование, метилирование, гликозилирование и др.).
Изменение физико-химических условий внутриклеточной среды (рН, температура и др.).
Белок-белковое взаимодействие (регуляция специфическими белками).
Слайд 61Регуляция функционирования ферментных систем
Ферментные системы обладают способностью поддерживать необходимую скорость суммарного процесса

преобразования исходного субстрата в конечный продукт.
При накоплении конечного продукта он может оказывать ингибирующее действие на первый фермент системы. Происходит ингибирование по типу обратной связи, или ретро-ингибирование.
Слайд 62Регуляция биосинтеза ферментов
Индукция фермента (синтез de novo) происходит при повышении концентрации субстрата

в клетке.
Репрессия фермента (снижение скорости синтеза) происходит при повышении концентрации продуктов ферментативной реакции.
Сущность регуляции биосинтеза сводится к “включению” или “выключению” генов, ответственных за синтез фермента.
Слайд 63Аллостерические ферменты
Термин «аллостерический» происходит от греческих слов allo – другой, stereo –
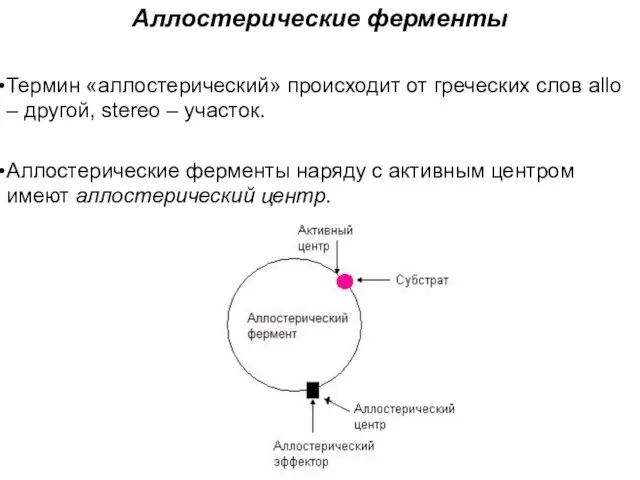
участок.
Аллостерические ферменты наряду с активным центром имеют аллостерический центр.
Слайд 64С аллостерическим центром связываются аллостерические эффекторы - вещества, способные изменять активность ферментов.

Эффекторы бывают
положительными, активирующими фермент,
отрицательными – ингибирующими фермент.
Некоторые аллостерические ферменты могут подвергаться действию двух и более эффекторов.
Слайд 65Регуляция мультиферментных систем
Некоторые ферменты действуют согласованно, объединяясь в мультиферментные системы, в которых

каждый фермент катализирует определенную стадию метаболитического пути:
Слайд 66В мультиферментной системе есть фермент, который определяет скорость всей последовательности реакций.
Этот

фермент, как правило, бывает аллостерическим и находится в начале матаболитического пути.
Он способен, получая различные сигналы, как повышать, так и понижать скорость катализируемой реакции, тем самым регулируя скорость всего процесса.
Слайд 67Применение ферментов
Отрасли промышленности, в которых применяются ферменты:
хлебопечение, пивоварение, виноделие, чайное, кожевенное и

меховое производства, сыроварение, кулинария (для обработки мяса) и т.д.;
в химической индустрии для разделения стереоизомеров;
сельском хозяйстве;
медицине.
Слайд 68Применение ферментов в медицине
Энзимопатология - изучает молекулярные основы развития патологического процесса, исходя

из данных о нарушениях механизмов регуляции активности или синтеза ферментов.
Энзимодиагностика– это использование ферментов в качестве избирательных реагентов для определения метаболитов, а также определение самих ферментов в биологических жидкостях при патологии.
Слайд 69Энзимотерапия – использование ферментов, активаторов и ингибиторов в качестве лекарственных средств.
Например: протеолитические

ферменты: пепсин, трипсин, химотрипсин и их смеси.


































































 Весна идет
Весна идет Ткани растений
Ткани растений § 46. Значение, строение и функционирование нервной системы 8 класс биология
§ 46. Значение, строение и функционирование нервной системы 8 класс биология Введение в ангиологию. Микроциркуляторное русло
Введение в ангиологию. Микроциркуляторное русло 基因表达调控
基因表达调控 Механические ткани. Колленхима
Механические ткани. Колленхима Класс Насекомые
Класс Насекомые Презентация на тему Городские птицы
Презентация на тему Городские птицы  Царство растений
Царство растений Биологическое значение митоза и мейоза. Формы размножения животных
Биологическое значение митоза и мейоза. Формы размножения животных Мы живём среди людей
Мы живём среди людей Минеральное питание растений
Минеральное питание растений Птицы России
Птицы России Эволюция. Антропогенез
Эволюция. Антропогенез Лизосомы. Типы лизосом
Лизосомы. Типы лизосом Основные закономерности наследования. Множественный аллелизм
Основные закономерности наследования. Множественный аллелизм Внутреннее строение корня, стебля
Внутреннее строение корня, стебля Окружающий мир. Животные
Окружающий мир. Животные Презентация на тему РЕФЛЕКС. РЕФЛЕКТОРНАЯ ДУГА
Презентация на тему РЕФЛЕКС. РЕФЛЕКТОРНАЯ ДУГА  Покровы позвоночных разных классов
Покровы позвоночных разных классов Царство Грибы (Mycota)
Царство Грибы (Mycota) Строение цветка
Строение цветка Prezentatsia_po_biologii_9_klass_na_temu_Somaticheskiy_i_vegetativny_otdely_nervnoy_sistemy
Prezentatsia_po_biologii_9_klass_na_temu_Somaticheskiy_i_vegetativny_otdely_nervnoy_sistemy Презентация на тему Элементарные факторы эволюции
Презентация на тему Элементарные факторы эволюции  Animal Idioms
Animal Idioms Презентация на тему "Липиды" - презентации по Биологии
Презентация на тему "Липиды" - презентации по Биологии Живые участники круговорота веществ в природе
Живые участники круговорота веществ в природе Щитовидная железа
Щитовидная железа